Amide
Définition
Un amide est tout composé organique qui possède le groupement amide CO–NH2, dérivant de l'ammoniac, mais très différents. Ce composé est formé conceptuellement ou chimiquement en remplaçant l'hydroxyle d'un acide oxydique par un substituant amine. La plupart du temps, les amides sont classés dans le groupe des composés organiques covalents, mais il existe également des amides inorganiques ioniques appelés amides métalliques.
Un amide (formamide) :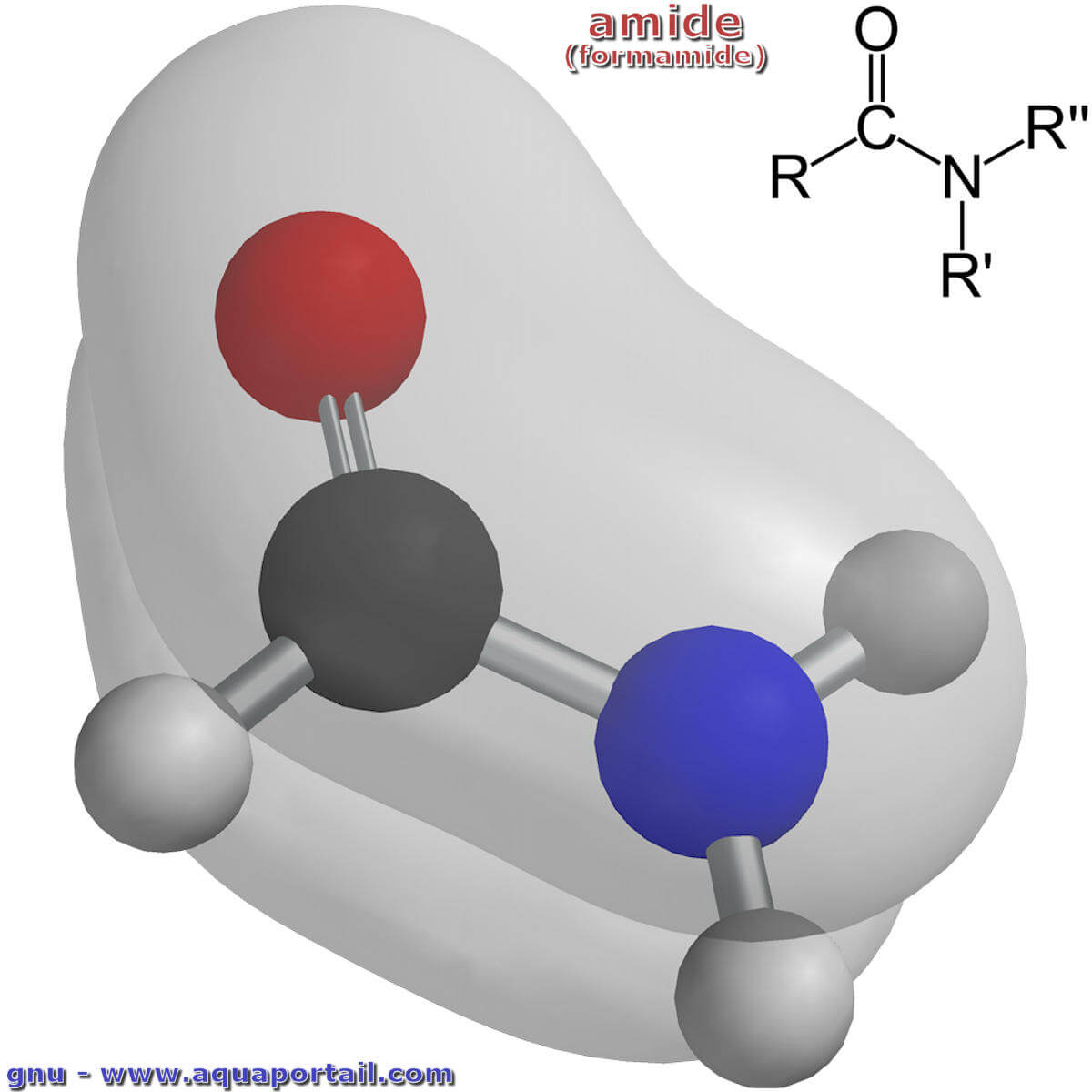
Les amides ont un système conjugué sur les atomes de O, C, N, constitué d'orbitales moléculaires occupées par des électrons délocalisés. Une des orbitales moléculaires π dans le formamide est présentée ci-dessus.
Explications
En chimie organique, les amides des acides carboxyliques (strictement, le carboxamide) sont appelés "amide". Il peut être considéré comme un dérivé d'un acide carboxylique en substituant le groupe –OH de l'acide à un groupe –NH2, –NHR ou –NRR' (appelé groupe amino). C'est pourquoi son groupe fonctionnel est du type RCONR'R''', CO étant un carbonyle, N un atome d'azote, et R, R' et R'' des radicaux organiques ou des atomes d'hydrogène.
Voir aussi l'amidase.
Une cyanamide est un amide de l'acide cyanhydrique.
Types
En termes formels, tous les amides sont dérivés de l'ammoniac en remplaçant un ou plusieurs atomes d'hydrogène dans la molécule d'ammoniac par d'autres atomes ou groupes d'atomes. Il y a :
- Les dérivés d'amides covalents d'acides carboxyliques organiques, d'acides sulfoniques ou d'oxoacides inorganiques (tels que l'acide sulfurique ou l'acide phosphorique) dans leurs molécules respectives, forment formellement un ou plusieurs des groupes hydroxy acides du groupe carboxy ou de l'oxoacide inorganique un groupe amino éventuellement substitué par des radicaux alkyle.
- Les amides ioniques (amides métalliques) en tant que sels d'ammoniac (NH3), qui sont causés par le fait qu'un proton de la molécule d'ammoniac est remplacé par un cation métallique. Des réactions interviennent pour produire de tels amides métalliques (en l'absence d'eau !) Avec dégagement d'hydrogène lorsque les métaux alcalins sont mis en contact avec de l'ammoniac liquide. Cela produit des amides de métaux alcalins, par exemple. Par exemple, l'amidure de sodium (NaNH2). Avec leur aide, d'autres amides métalliques, par exemple l'amide d'argent.
Description
Tous les amides, à l'exception du formamide (amide d'acide formique), sont solides à la température ambiante et leurs points d'ébullition sont élevés, supérieurs à ceux des acides correspondants. Ils ont d'excellentes propriétés de solvant et sont des bases très faibles.
L'un des principaux procédés d'obtention de ces composés consiste à faire réagir l'ammoniac (ou les aminés primaires ou secondaires) avec des esters. Les amides sont de nature courante et l'un des plus connus est l'urée, un diamide ne contenant pas d'hydrocarbures. Les protéines et les peptides sont formés par des amides. Un exemple de polyamide à longue chaîne est le nylon.
Les amides sont également largement utilisés dans l'industrie pharmaceutique.
Une structure tautomère, dans laquelle la double liaison n'est pas entre le carbone et l'oxygène, mais entre le carbone et l'azote et possède en même temps un groupe hydroxyle, forme les acides imides.
Polyamides
L'amide d'acide carbonique est appelé urée et ses dérivés sont le groupe fonctionnel uréide (uréidique). Les diacylamines sont désignées sous le nom de groupe fonctionnel imide et sont analogues aux anhydrides carboxyliques.
Les polyamides sont des composés contenant des groupes amides. Certains sont synthétiques, comme le nylon, mais on les trouve également dans la nature, dans des protéines, formées à partir d'acides aminés, en faisant réagir un groupe carboxyle d'un acide aminé avec un groupe amino de l'autre. Dans les protéines, le groupe amide est appelé liaison peptidique.
Le nylon est un polyamide en raison des groupes amides caractéristiques dans la chaîne principale de sa formulation. Par exemple, le nylon 6 est obtenu par polymérisation de l'e-caprolactame.
Certains polyamides de type nylon sont le polyamide-6, le polyamide-11, le polyamide-12, le polyamide-9,6, le polyamide-6,9, le polyamide-6,10 et le polyamide-6,12. On peut citer à titre d'exemple de polyamides non linéaires des exemples de condensation d'acides dimérisés d'huiles végétales avec des amines.
Les peptides, y compris les protéines telles que la soie, que le nylon a remplacées, sont également des polyamides. Ces groupes amides sont très polaires et peuvent être reliés entre eux par des ponts-ponts d'hydrogène. Pour cette raison, la chaîne de nylon étant si régulière et symétrique, le nylon est souvent cristallin et forme d'excellentes fibres.
Synthèse d'amides
La synthèse des amides peut être réalisée par différentes méthodes. La méthode la plus simple est la condensation d'un acide carboxylique avec une amine. Cette réaction est généralement thermodynamiquement favorable, mais a une énergie d'activation élevée, due principalement à la première déprotonation de l'acide carboxylique et à la protonation de l'amine, qui forme un produit stable, l'aminocarboxylate. Cela réduit la réactivité. De plus, des températures élevées sont nécessaires.
De nombreuses méthodes sont connues pour conduire la balance à droite. Pour la plupart, ces réactions impliquent "l'activation" de l'acide carboxylique en le rendant d'abord meilleur électrophile; tels que les esters, les chlorures d'acide (réaction de Schotten-Baumann) ou les anhydrides (méthode lumière-Barbier). Les méthodes classiques de synthèse peptidique utilisent des agents de couplage tels que HATU, l'hydroxybenzothiazole (HOBt) ou le PyBOP. Récemment, de nouveaux réactifs à base de bore pour la formation de liaisons CO-N sont apparus, notamment l'utilisation de catalyseurs à base d'acide 2-iodophénylboronique, de MIBA et de tris borate (2, 2,2-trifluoroéthyle).
Réactions d'amide
Les principales réactions des amides sont :
- hydrolyse acide ou basique : L'amide est hydrolysé en milieu basique formant un carboxylate de métal ou en milieu acide formant un acide carboxylique.
- déshydratation : Un nitrile est produit en présence d'un déshydrateur tel que le chlorure de thionyle ou le pentoxyde de phosphore.
- réduction : Les amides peuvent être réduits avec de l'hydrure d'aluminium lithium en amines.
- Transposition de Hofmann : En présence d'un halogène dans un milieu basique, une réaction complexe est obtenue qui permet d'obtenir une amine avec moins de carbone dans sa chaîne principale.
Exemples
L'acrylamide est utilisé dans différentes applications, bien qu'il soit mieux connu pour être probablement cancérogène et être présent dans de nombreux aliments lorsqu'il est formé par des processus naturels lors de la cuisson.
Ils sont une source d'énergie pour le corps humain.
Ils peuvent être des vitamines dans le corps ou des analgésiques.
Importance et utilisations
Les amides sont de nature courante et se trouvent dans des substances telles que les acides aminés, les protéines, l'ADN et l'ARN, les hormones et les vitamines.
L'urée est utilisée pour l'excrétion d'ammoniac (NH3) chez l'homme et les mammifères. Il est également largement utilisé dans l'industrie pharmaceutique et dans l'industrie du nylon.
Synonymes, antonymes
Voir tous les synonymes pour "amide".1 synonyme (sens proche) de "amide" :
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à AMIDE sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
Le mot AMIDE est dans la page 5 des mots en A du lexique du dictionnaire.
Mots en A à proximité
amiboïde amiboïsme amibozoaire amictique amidase amideamidon amidon floridéen amidon intraplastidial amination amine
En rapport avec "amide"
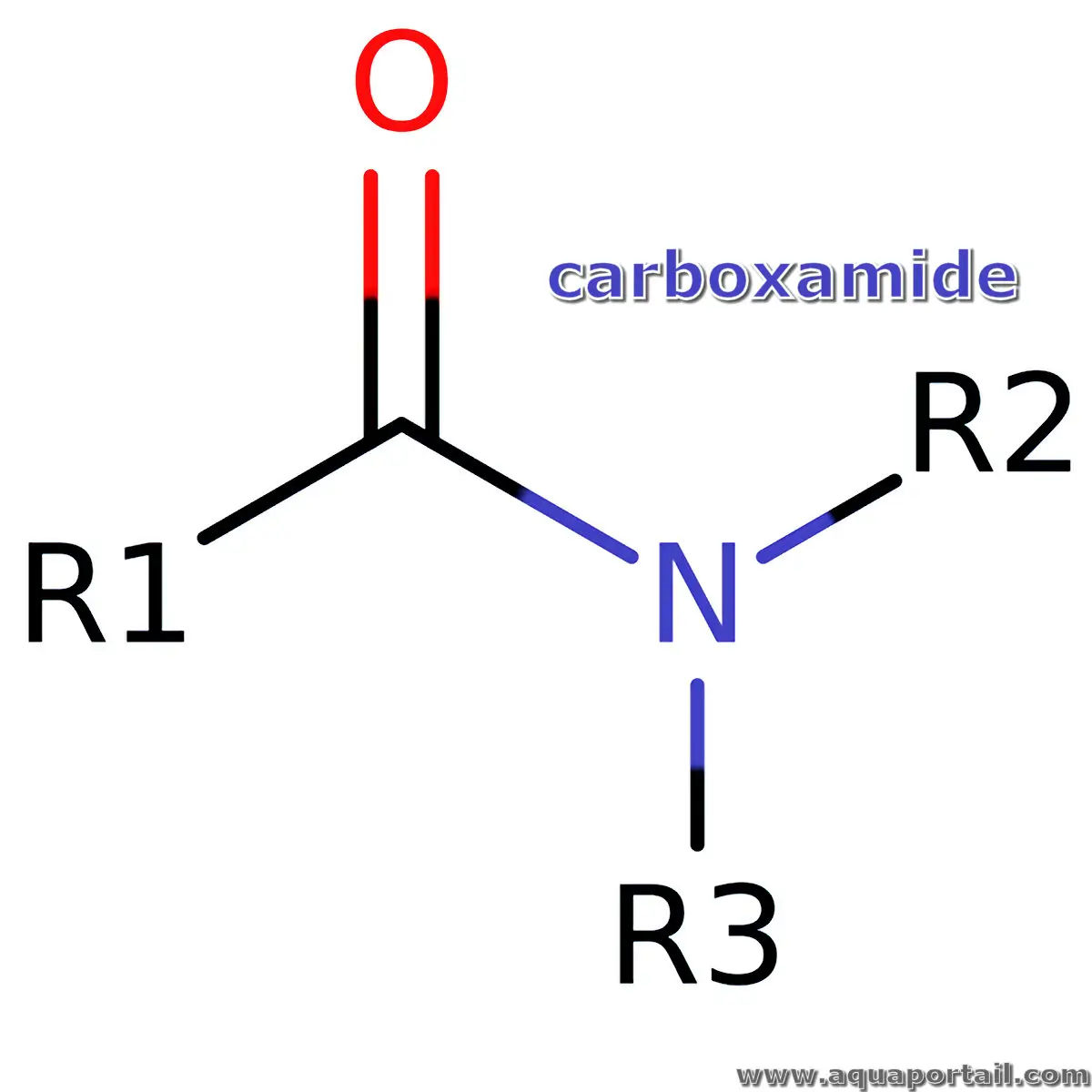
Le carboxamide est un amide d'acide carboxylique ayant la structure RC(=O)NR₂. Le terme est utilisé comme suffixe dans la formation systématique de noms pour...
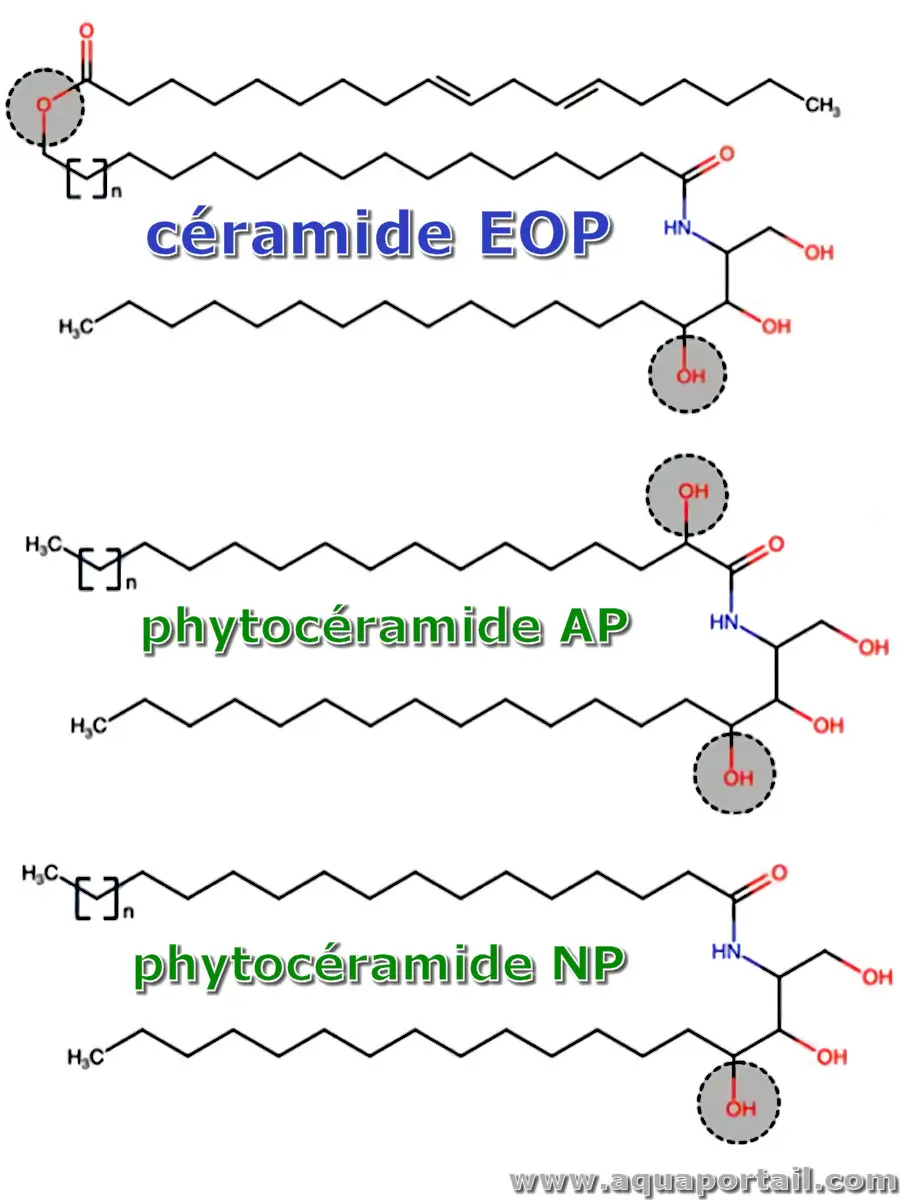
Un céramide est une molécule de la famille des sphingolipides présente en forte concentration dans la peau et des téguments végétaux.

Un cyanamide est l'amide de l'acide cyanique (acide cyanhydrique). Le composé, de formule chimique CN-NH₂, dérive de l'ammoniac par substitution du groupe...
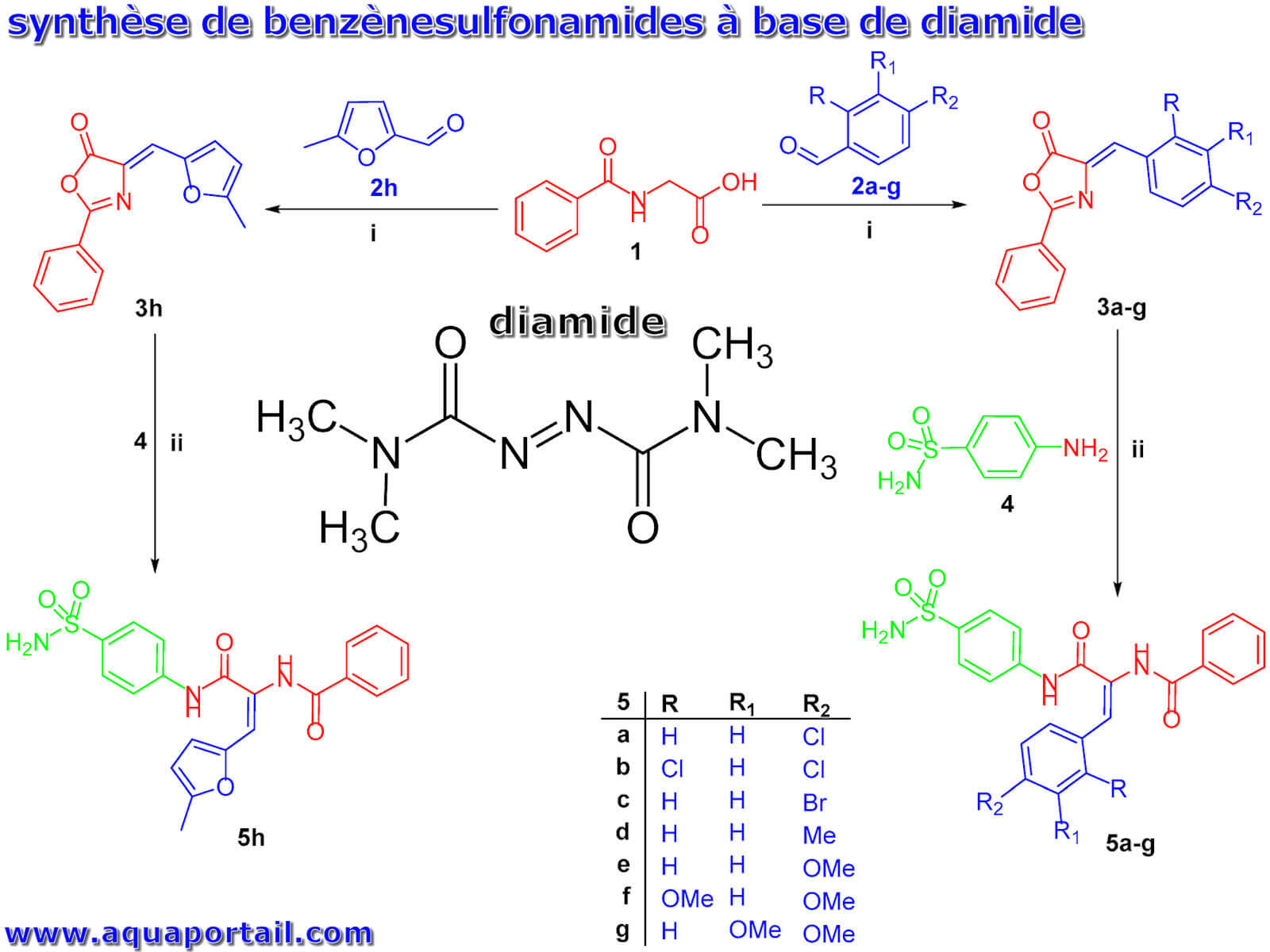
Un diamide est un composé chimique ayant deux radicaux amides. C'est un composé intermédiaire apparaissant lors de la fixation biologique de l'azote...
