Phosphore
Définition
Le phosphore est un élément chimique avec le numéro atomique 15 et le symbole P. C'est un non-métal multivalent appartenant au groupe de l'azote (groupe 15) présent dans la nature en combinaison avec des phosphates inorganiques et des organismes vivants mais jamais à l'état natif. Il est très réactif et s'oxyde spontanément au contact de l'oxygène atmosphérique émettant de la lumière.
Du phosphore blanc :
Le phosphore peut être incolore, blanc ou rouge.
Cet élément peut être trouvé en petites quantités dans la semence, ce qui fait que ce fluide se distingue par une couleur remarquable avant la lumière ultraviolette; Cela a permis de résoudre certaines affaires pénales impliquant une violation sexuelle.
Voir aussi le cycle du phosphore et le phosphore minéral dissous.
Explications générales
Le phosphore, molécule de Pi (phosphate inorganique), fait partie des molécules d'ADN et d'ARN, les cellules l'utilisent pour stocker et transporter l'énergie par l'adénosine triphosphate (ATP). En outre, l'addition et l'élimination des groupes phosphate aux protéines, respectivement la phosphorylation et la déphosphorylation, constituent le principal mécanisme de régulation de l'activité des protéines intracellulaires, et donc du métabolisme des cellules eucaryotes telles que le sperme.
C'est un cycle sédimentaire dont le réservoir est la croûte terrestre. L'élément est stocké dans des roches phosphatées et, à mesure qu'elles s'érodent, des composés phosphatés sont libérés dans le sol et l'eau. Ils sont ensuite absorbés par les plantes, à travers les racines et incorporés dans les composantes vivantes du système lorsqu'ils traversent les différents niveaux trophiques. Une fois que les organismes (plantes ou animaux) meurent, ils se décomposent et libèrent du phosphore contenu dans la matière organique.
Caractéristiques principales
Les principales caractéristiques du phosphore sont :
- Le phosphore est un composant essentiel des organismes.
- Il fait partie des acides nucléiques (ADN et ARN).
- Il fait partie des os et des dents des animaux.
- Chez les plantes, dans une portion de 0,2 % et chez les animaux, le phosphore représente 1 % de sa masse.
- Le phosphore commun est un solide.
- Blanc, mais pur est incolore.
- Une odeur désagréable caractéristique.
- C'est un non-métal.
- Emet de la lumière par phosphorescence.
Il existe plusieurs formes allotropes de phosphore, la plus courante étant le phosphore blanc et le phosphore rouge; les deux forment des structures tétraédriques de quatre atomes. Le phosphore blanc extrêmement toxique et inflammable a deux formes, alpha et bêta, avec une température de transition de -3,8 °C; exposé au soleil ou à la chaleur (300 °C) devient du phosphore rouge dans une réaction exothermique. Ceci est plus stable et moins volatil et toxique que le blanc et est ce qui se trouve normalement dans les laboratoires et avec lesquels les allumettes sont faites. Le phosphore noir a une structure similaire au graphite et conduit l'électricité, il est plus dense que les deux autres états et ne s'enflamme pas.
Fonction biologique
Les composés phosphorés interviennent dans les fonctions vitales pour les êtres vivants et sont donc considérés comme un élément chimique essentiel, bien que des expériences récentes suggèrent que certaines formes de vie pourraient le remplacer par de l'arsenic. Il fait partie de la molécule de phosphate inorganique, ainsi que des molécules d'ADN et d'ARN et des phospholipides dans les membranes lipidiques.
Les cellules l'utilisent pour stocker et transporter l'énergie à travers l'adénosine triphosphate. En outre, l'addition et l'élimination des groupes phosphate aux protéines, respectivement la phosphorylation et la déphosphorylation, constituent le principal mécanisme de régulation de l'activité des protéines intracellulaires, et donc du métabolisme des cellules eucaryotes telles que le sperme.
Abondance et obtention
En raison de sa réactivité, le phosphore n'est pas présent dans la nature, mais fait partie de nombreux minéraux. L'apatite est une source importante de phosphore, avec des gisements importants au Maroc, en Russie, aux États-Unis et dans d'autres pays.
La forme allotropique blanche peut être obtenue par différentes procédures; dans l'un d'entre eux, le phosphate tricalcique, obtenu à partir de roches, est chauffé dans un four à 1450 °C en présence de silice et de carbone, réduisant le phosphore libéré sous forme de vapeur.
Précautions
Attention aux empoisonnements au phosphore ! Le phosphore blanc est extrêmement toxique - une dose de 50 mg peut être fatale - et hautement inflammable, il doit donc être stocké immergé dans de l'huile ou de l'eau pour éviter tout contact avec l'oxygène. Le contact avec elle provoque une combustion immédiate et violente. Il provoque des brûlures si elle entre en contact avec la peau. L'exposition continue au phosphore provoque une nécrose de la mâchoire.
Phosphore rouge
Le phosphore rouge ne s'enflamme pas spontanément en présence d'air et n'est pas toxique, mais il doit être manipulé avec précaution car il peut produire du phosphore blanc et dégager des fumées toxiques lorsqu'il est chauffé.
Phosphore minéral dissous
Le phosphore minéral dissous est un élément nutritif dont la forme minérale majoritaire se rencontre sous orthophosphate, et qui est essentiel à la vie aquatique. Les teneurs en orthophosphate sont normalement assez faibles en surface en milieu océanique et côtier non pollué : 0 à 1 μmol/l.
Les teneurs augmentent avec la profondeur, au-dessous de la zone euphotique, ou lorsqu'on se rapproche des estuaires. Les eaux profondes ont une teneur de l'ordre de 3 μmol/l qui fluctue légèrement selon la zone océanique considérée.
Dans les estuaires, des concentrations très élevées peuvent être atteintes : plusieurs dizaines de micromoles par litre selon la salinité. Ces fortes concentrations, indice d'un enrichissement d'origine domestique et agricole, peuvent être responsables de phénomènes d'eutrophisation. Au moment du développement phytoplanctonique printanier, le phosphore est consommé et peut descendre à la limite de détection des méthodes courantes d'analyse (environ 0,01 μmol/l).
Dans les eaux saumâtres turbides, la concentration en phosphate dans la phase liquide dépend également de la concentration et de la nature des particules en raison des phénomènes d'adsorption. Les phosphates peuvent être présents dans les rejets urbains (effluents domestiques et lessives contenant des polyphosphates).
Synonymes, antonymes
Voir tous les synonymes pour "phosphore".0 synonyme (sens proche) pour "phosphore".
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à PHOSPHORE sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
Le mot PHOSPHORE est dans la page 3 des mots en P du lexique du dictionnaire.
Mots en P à proximité
phosphohexose phospholipase phospholipide phospholipidique phosphoprotéine phosphorephosphore minéral dissous phosphorescence phosphorisation phosphorylase phosphorylation
En rapport avec "phosphore"
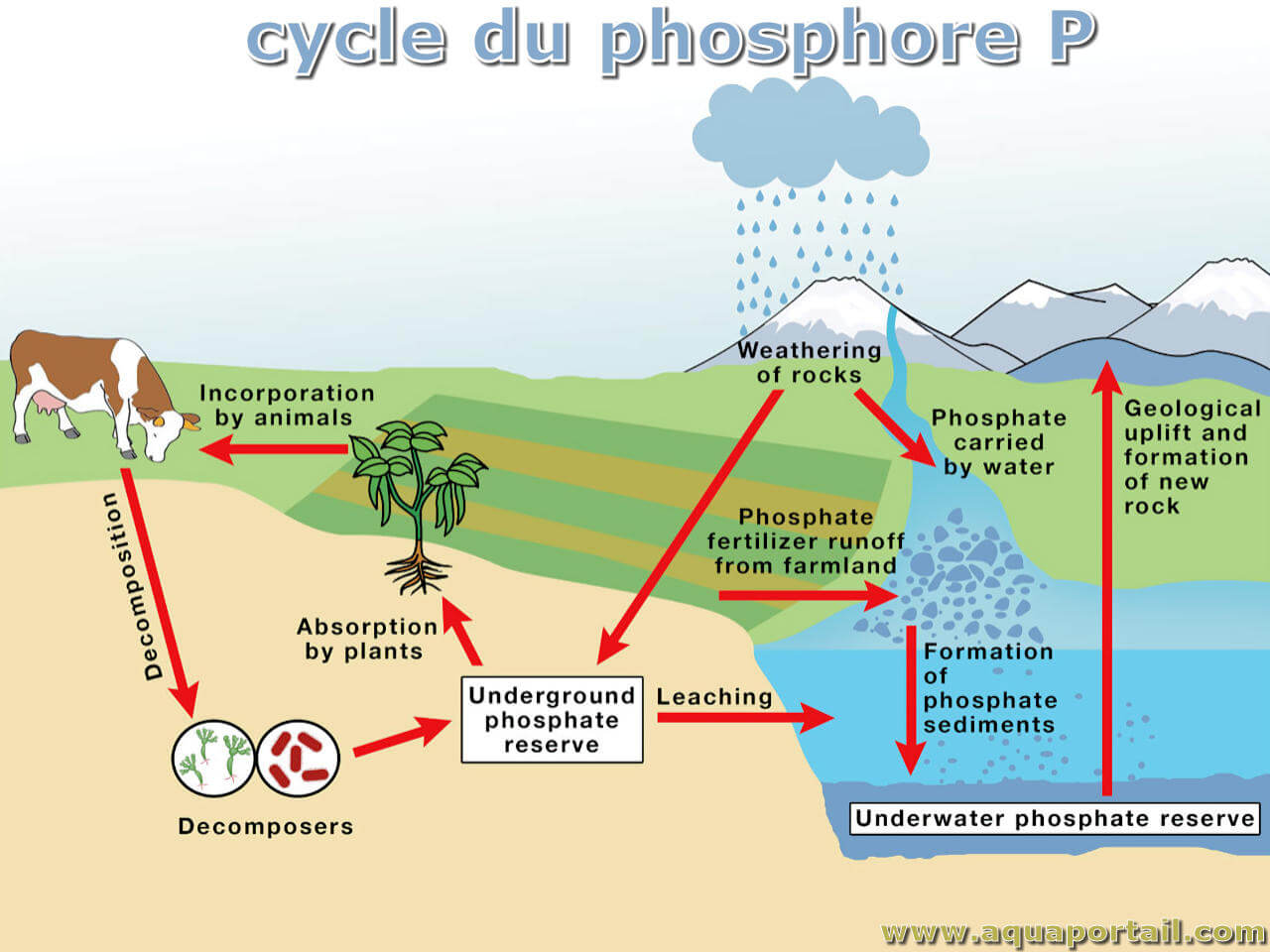
Le cycle du phosphore correspond aux diverses phases de solubilité du phosphore dans la nature.
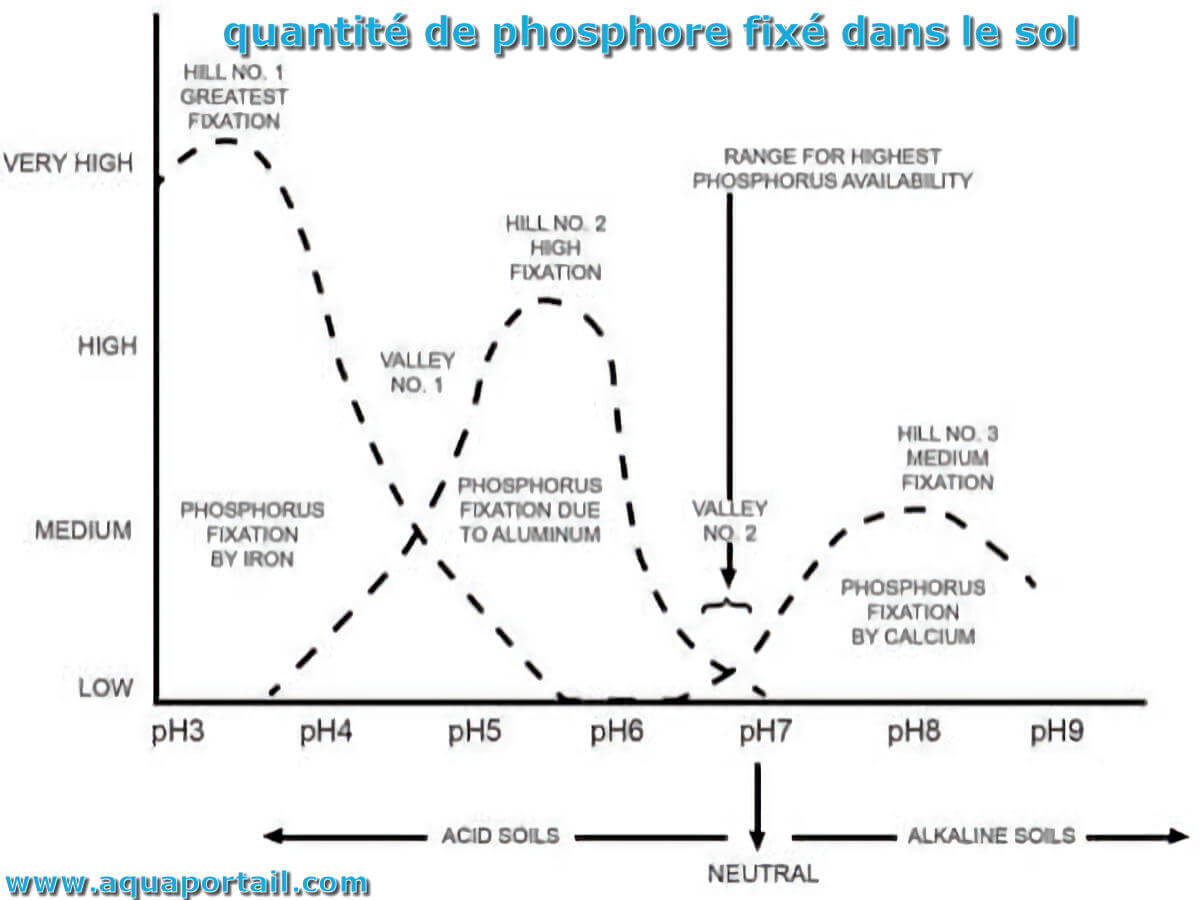
La fixation du phosphore (P) intervient lorsqu'il est appliqué au sol, quelle que soit la marque de l'engrais ou sa composition chimique.
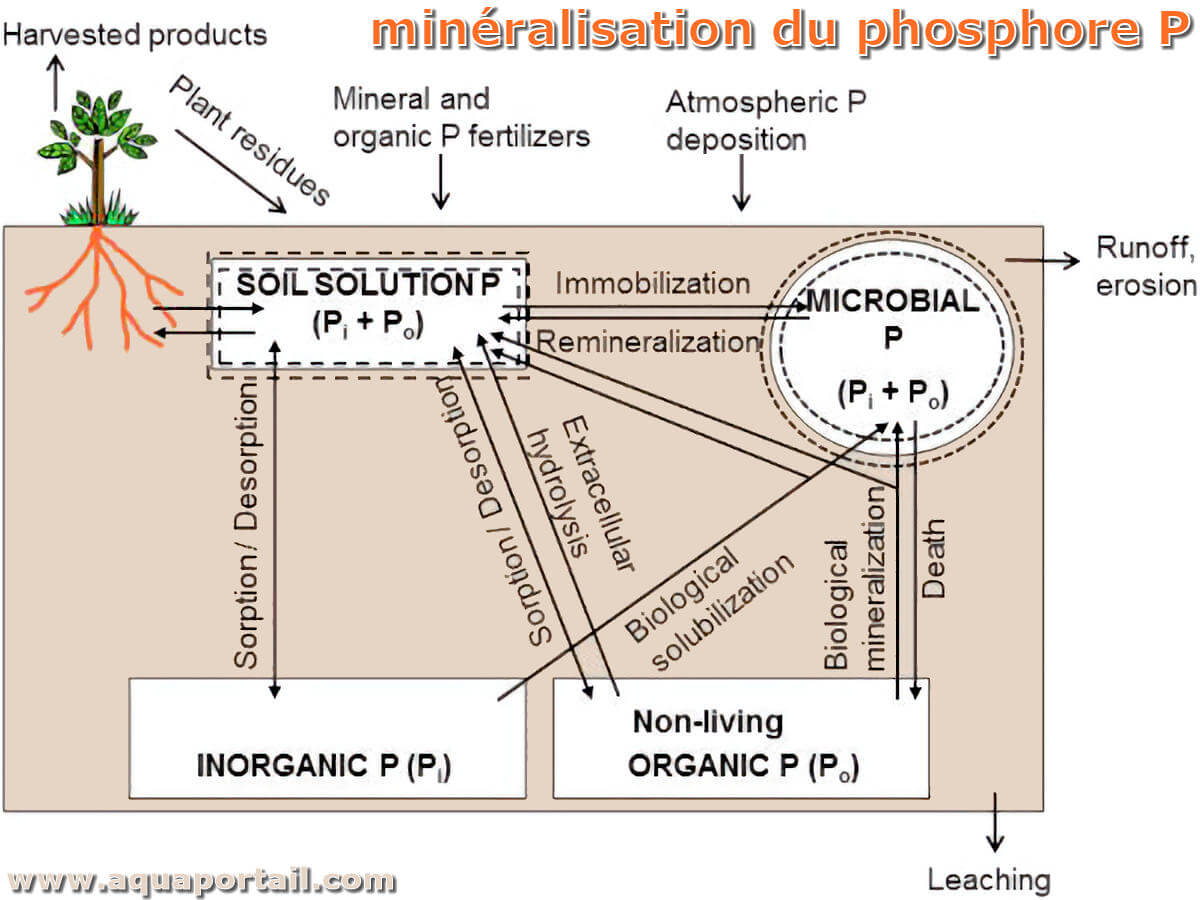
La minéralisation du phosphore précise le passage du phosphore (P) d'un état organique à une forme inorganique en raison de la décomposition microbienne...

La phosphorescence est la propriété d'une substance de visiblement briller dans l'obscurité.
