Triméthylamine
Définition
La triméthylamine est un gaz inflammable incolore qui dégage une odeur intense de poisson, même à forte dilution. À des concentrations plus élevées, il rappelle davantage celui de l'ammoniac lié chimiquement. Il est hautement hygroscopique, se dissout bien dans l'eau et forme une base forte dedans. C'est une amine tertiaire, inflammable et hygroscopique. Le gaz se présente sous la forme d'une solution aqueuse à 40 %, d'une solution à 33 % dans l'éthanol et d'un gaz liquéfié sous pression sur le marché.
Une molécule de triméthylamine :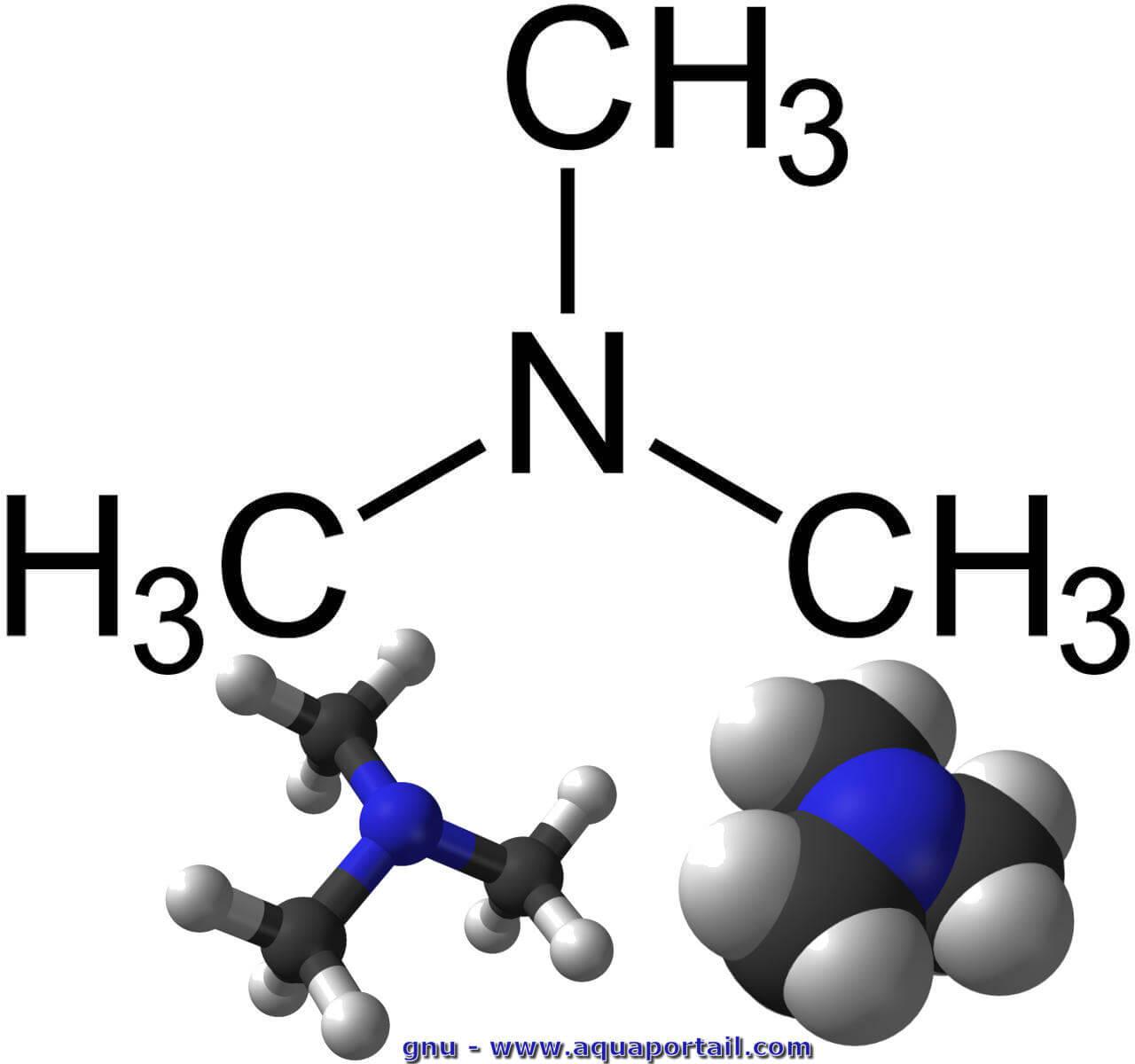
Le triméthylamine a pour formule chimique moléculaire C3H9N. La masse molaire est de 59,11 g/mol. Le point de fusion est à -117,1 °C quand le point d'ébullition est de 2,9 °C.
Explications
L'oxyde de triméthylamine est un des composants de l'urine, et il est également présent dans le sang des poissons marins, où il pourrait intervenir pour le maintien de la pression osmotique. La triméthylamine, ou son oxyde, existe également dans les muscles des poissons marins, et est responsable de l'odeur de poissons frais.
Voir aussi la triméthylaminurie, syndrome de "l'odeur de poisson". Voir aussi la plante appelée la vulvaire dont les feuilles dégagent une odeur nauséabonde.
Extraction et présentation
La production industrielle de triméthylamine est réalisée par la réaction de méthanol et d'ammoniac à des températures de 370 à 430 °C et à des pressions de 20 à 30 bars. La réaction est effectuée en phase gazeuse sur des catalyseurs hétérogènes acides à base d'oxydes de silicium et d'aluminium. Outre la triméthylamine et l'eau, les produits de la réaction sont la méthylamine CH3NH2 et la diméthylamine (CH3)2NH.
La purification et le traitement final du mélange réactionnel sont réalisés par distillation sous pression à plusieurs étapes.
Avec des agents de méthylation plus réactifs tels que l'iodure de méthyle ou le sulfate de diméthyle, l'ammoniac peut être méthylé à basse température. Cependant, on obtient également des mélanges d'étages possibles de méthylation comprenant les tétraméthylammoniumions quaternaires.
Propriétés physiques
À la température ambiante, la triméthylamine est un gaz incolore. Il peut être liquéfié en refroidissant ou en augmentant la pression. La triméthylamine est facilement soluble dans l'eau et les alcools aliphatiques tels. Par exemple le méthanol. Il a une odeur désagréable, de poisson ou de transonique en ammoniac, qui est perceptible même à des concentrations de 0,0005 à 4,2 mg/m3.
Propriétés chimiques
La triméthylamine se dissout très facilement dans l'eau, la solution réagit comme une base. La molécule se dissocie en solution aqueuse.
La valeur de pK s la plus élevée (9,81) par rapport à l'ammoniac (9,25) s'explique par l'effet + I des trois groupes méthyle. La basicité encore plus faible que les "intermédiaires" méthyle et diméthylamine (pK 10,66 et 10,73) peut être expliquée par l'encombrement stérique de la paire isolée sur l'atome d'azote, responsable de la basicité.
La triméthylamine, comme toutes les amines, est une base faible. Avec les acides, il forme des sels ioniques, à partir desquels il peut être libéré avec des bases plus fortes.
Caractéristiques de sécurité
La triméthylamine forme des mélanges air-vapeur hautement inflammables. Le composé a un point d'éclair à -7 °C. La plage d'explosion est comprise entre 2,0 % en volume (49 g/m3) en tant que limite inférieure d'explosion (LEL) et 11,6 % en volume (285 g/m3) en tant que limite supérieure d'explosion (OEG). Il a été déterminé que la largeur de l'intervalle est de 1,05 mm. Il en résulte une affectation au groupe d'explosion IIA. La température d'inflammation est de 190 °C. La substance entre donc dans la classe de température T4.
Utilisations
Le principal produit séquentiel de la triméthylamine est le chlorure de choline, qui peut être préparé en faisant réagir de l'oxyde d'éthylène avec une solution aqueuse de sel de chlorhydrate de triméthylamine ou en faisant réagir de la triméthylamine avec du 2-chloroéthanol (éthylène chlorhydrine). De plus, la triméthylamine trouve une application dans la production de régulateurs de croissance, de résines échangeuses d'ions et comme catalyseur dans la synthèse organique.
Dans la nature
En tant que métabolite du métabolisme de la choline, la triméthylamine peut être détectée dans de nombreux organismes. Des concentrations plus élevées surviennent dans la dégradation microbienne du triméthylamine-N-oxyde, qui est abondant notamment chez les poissons d'eau de mer, par exemple chez les bactéries des genres Pseudomonas et Shewanella. Le parfum intense de triméthylamine ("saumure de hareng") est donc un signe certain du manque de fraîcheur. La triméthylamine continue d'être produite dans les sécrétions vaginales et l'éjaculat masculin décomposé. Parmi les champignons, les champignons brûlés tels que la Tilletia caries sont capables de produire de la triméthylamine et de gâcher les grains si le blé est impliqué. Enfin, certaines plantes produisent de la triméthylamine, telles que le chénopode odorant Chenopodium vulvaria et l'herbe de bois Mercurialis perennis. Les fleurs de châtaignier, d'aubépine, de poirier et d'autres plantes apparentées à la rose, ainsi que l'épine d'épine-vinette, contiennent l'amine. Dans ce dernier cas, il s'agit probablement de l'attraction des Coléoptères en tant qu'insectes pollinisateurs (Cantharophilie). Enfin, la triméthylamine est contenue dans les faines. Dérivée du nom de genre du hêtre Fagus, la substance est donc également appelée Fagine. En grillant les fruits, l'effet poison est réduit.
La triméthylamine est également produite dans les intestins humains, en tant que métabolite après absorption de la phosphatidylcholine, de la choline et de la carnitine, que l'on trouve notamment dans les oeufs et la viande. La triméthylamine est bien absorbée et métabolisée dans le foie par les monooxygénases contenant de la flavine (FMO3) en N-oxyde de triméthylamine (TMAO). L'enzyme FMO3 est un régulateur central du métabolisme du cholestérol dans le foie et son élimination a empêché le développement de l'hyperglycémie, de l'hyperlipidémie et de l'artériosclérose chez des souris en surpoids insulinorésistantes. Le taux de TMAO chez l'homme est associé à un risque accru de maladie cardiovasculaire, en particulier de crise cardiaque et d'accident vasculaire cérébral. Le TMAO a des propriétés pro- artériosclérotiques et augmente la concentration de cholestérol spécifique aux macrophages et la formation de cellules spumeuses dans la paroi des vaisseaux. De plus, le TMAO augmente l'activité des plaquettes. Lors de l'administration d'antibiotiques, le taux sanguin de TMAO avait chuté. La formation de TMA peut être inhibée par le 3,3-diméthyl-1-butanol.
Effet sur le corps humain
La triméthylamine est considérée comme légèrement toxique. Il est irritant pour les yeux et le système respiratoire. La perception des odeurs peut déjà présenter une concentration nocive pour la santé. En cas d'ingestion, les vomissements accompagnés de douleurs abdominales peuvent provoquer des brûlures. Les brûlures chimiques peuvent entraîner la destruction de la peau, des yeux, des voies respiratoires et du tube digestif.
Synonymes, antonymes
Voir tous les synonymes pour "triméthylamine".0 synonyme (sens proche) pour "triméthylamine".
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à TRIMÉTHYLAMINE sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
Le mot TRIMETHYLAMINE est dans la page 4 des mots en T du lexique du dictionnaire.
Mots en T à proximité
trillion trilobé trilobite triloculaire trimère triméthylaminetrimonoécie trimonoïque trimorphe trioïque triongulin
En rapport avec "triméthylamine"

En anatomie, vulvaire est relatif à la vulve. La zone vulvaire est symétriquement divisée en deux par une fente médiane (fente vulvaire) et comporte...

Le diméthylsulfoxyde (DMSO) est un produit d'oxydation du diméthylsulfure. Le DMSO est un liquide organique incolore de formule chimique CH₃SOCH₃ contenant...
Le diméthylsulfure (DMS, sulfure de diméthyle) est un composé chimique volatile, un thioéther, de formule moléculaire (CH₃)₂S.

La méthylation est la fixation par addition d'un groupe méthyle -CH₃ sur une molécule. En biologie du développement, la méthylation est le principal mécanisme...
