Thioester
Définition
Un thioester est un produit de condensation qui peut s'être formé par la voie des peptides au cours des origines de la vie. Un rôle général des thioesters dans la chimie prébiotique montre leur importance et leur large distribution dans le métabolisme contemporain. Les intermédiaires thioesters permettent l'anabolisme et le catabolisme des peptides, des acides gras, des stérols et des porphyrines.
Comparaison entre ester et thioester :
Les thioesters sont des agents acylants efficaces. Un agent acylant est une molécule capable de transférer un groupement acyle (RCO) à une autre espèce. La liaison CS est plus faible que la liaison CO, et le thiolate (ou thiol, s'il est protoné) est un meilleur groupe partant qu'alcoxyde (ou alcool). Ces facteurs font tous d'un thioester en général un meilleur agent acylant qu'un ester.
Explications
La condensation des blocs de construction en oligomères et polymères est considérée comme un processus précoce et important dans les origines de la vie. Cependant, les obstacles à la condensation abiotique des acides aminés pour former des peptides comprennent des énergies d'activation élevées, une thermodynamique défavorable et des réactions secondaires.
Les intermédiaires thioester dans le cycle humide-sec fournissent une résolution possible. De plus, on pense que les thiols ont été abondants sur la Terre prébiotique, en particulier près des sources de sulfure d'hydrogène.
Toutes les réactions abiotiques rapportées jusqu'à présent pour la formation de liaisons peptidiques via des intermédiaires thioesters reposaient sur des molécules à haute énergie, qui souffrent généralement d'une demi-vie courte dans des conditions aqueuses et nécessitent donc un réapprovisionnement constant.
Un thioester directement lié à une protéine via un résidu cystéine est généré au cours de la réaction catalysée par la glycéraldéhyde 3-phosphate déshydrogénase (GAPDH), une enzyme de la glycolyse.
Les acides aminés liés au thioester sont les précurseurs immédiats du processus d'oligomérisation ultérieur via la 4'-phosphopantéthéine conduisant à la formation des pentapeptides liés à l'enzyme.
Dans l'étape d'amorçage de leur catabolisme, les acides gras sont activés en leur dérivé CoA, en utilisant l'ATP comme source d'énergie. Le groupe carboxyle est d'abord activé en un intermédiaire acyl-adénylate à haute énergie lié à une enzyme formé par réaction du groupe carboxyle de l'acide gras avec l'ATP. Le groupe acyle est ensuite transféré à CoA par la même enzyme, l'acyl-CoA synthétase grasse. Cette enzyme est communément appelée thiokinase d'acide gras car l'ATP est consommé dans la formation de la liaison thioester dans l'acyl-CoA.
Chimie des acyles
La chimie du groupe acyle et de ses divers dérivés occupe une place prépondérante en chimie organique, et elle est également importante dans les réactions métaboliques. Contrairement aux divers dérivés acylés utilisés dans la synthèse organique, un dérivé clé - le thioester - joue un rôle disproportionné dans le métabolisme. Les thioesters les plus courants sont à base de phosphopantéthéine (qui est la forme biochimiquement active du pantothénate), qui comprend la coenzyme A ("A" pour acylation).
Certaines biomolécules servent de porteurs de groupes acyle. La coenzyme A entre dans cette catégorie, tout comme la protéine porteuse d'acyle, une petite protéine qui participe à la synthèse des acides gras en aidant la navette de la chaîne acyle en croissance entre les sites actifs enzymatiques. La synthèse de protéines non ribosomales implique également la formation d'amino-acyl-thioester.
Les thiols biochimiquement importants à base de phosphopantéthéine comprennent la coenzyme A (CoA) et la protéine porteuse d'acyle (ACP). Les thioesters formés par combinaison de ces thiols avec des espèces portant des groupes acyle - tels que les acides gras - ont des rôles importants dans le métabolisme. La phosphopantéthéine est la combinaison de 2-mercaptoéthylamine, de pantothénate et d'un groupe phosphate. Le pantothénate est une vitamine - il doit être inclus dans notre alimentation ou suffisamment acquis grâce à l'activité synthétique de la flore intestinale.
Les thioesters proviennent généralement ou sont interconvertis avec une espèce de phosphate d'acyle ou un adénylate d'acyle. Ces deux derniers ont une plus grande énergie libre standard biochimique pour le transfert de groupe acyle, de sorte que l'ATP peut être utilisé pour phosphoryler ou adényler d'abord un groupe carboxylate lorsque la production nette d'un thioester est nécessaire. La réaction du phosphate d'acyle est un moyen de générer un thioester. La réaction fonctionne également en sens inverse - l'énergie d'une liaison thioester (ΔG °′ = -7,5 kcal/mol pour l'hydrolyse) peut être conservée dans la liaison phosphoanhydride terminale de l'ATP.
Formation
La conversion d'un groupe carboxyle en thioester intervient dans les réactions biochimiques par quatre voies principales :
- estérification d'un groupe carboxyle, entraînée par l'hydrolyse de l'ATP;
- décarboxylation oxydative d'un acide α-céto. Il existe deux exemples étroitement liés de ce type de conversion, à savoir dans les réactions catalysées par le complexe pyruvate déshydrogénase et le complexe α-cétoglutarate déshydrogénase (partie du cycle de l'acide citrique;
- échange de thiols;
- échange du groupe acyle.
(1) et (2) aboutissent à la synthèse nette d'un thioester, tandis que dans (3) et (4), il n'y a pas de synthèse nette de thioester, mais simplement un échange de groupes.
Réactions
Les thioesters participent à diverses réactions. Les mécanismes comportent une attaque au niveau du carbone carbonyle pour produire un état de transition tétraédrique, qui peut conduire à un échange de thiol ou à une conversion en phosphate d'acyle; addition conjuguée à un thioester α,β-insaturé; réactions au niveau du carbone α, telles que l'énolisation catalysée par une base, suivie d'une attaque de l'énol sur un autre carbone carbonyle, comme dans la formation d'acétoacétate ou de citrate.
Les thioesters jouent un rôle important dans le métabolisme. Cela est particulièrement vrai du métabolisme des acides gras. Le métabolite central, l'acétyl-CoA, est un thioester produit principalement par décarboxylation oxydative du pyruvate ou par dégradation des acides gras. Les principaux destins de l'acétyl-CoA sont d'entrer dans le cycle de l'acide citrique ou de contribuer à la synthèse des acides gras.
Protéines contenant des thioesters (TEP)
Les protéines contenant des thioesters (TEPs) sont des protéines accessoires du système du complément, homologues aux protéines telles que C3, C4, a2M et CD109s. Les TEP favorisent l'opsonisation des microorganismes et leur élimination par phagocytose chez certains invertébrés en activant la voie de signalisation Toll.
Synonymes, antonymes
0 synonyme (sens proche) pour "thioester".
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à THIOESTER sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
Le mot THIOESTER est dans la page 2 des mots en T du lexique du dictionnaire.
Mots en T à proximité
thigmotactisme thigmotaxie thigmotropisme thigmotropogenèse Thiobacillus thioesterthiol thiolase thiolate thiosulfate d'ammonium thixotrope
En rapport avec "thioester"

L'acétyl-coenzyme A, ou acétyl-CoA, est une molécule fondamentale dans le métabolisme de tous les organismes vivants.
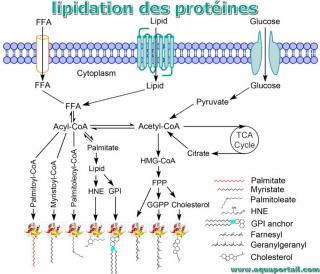
La lipidation est une modification traductionnelle importante des protéines dans laquelle les fractions lipidiques sont attachées de manière covalente...
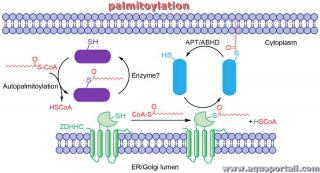
La palmitoylation (palmitylation) est la modification post-traductionnelle des protéines avec de l'acide palmitique (acide gras saturé à 16 carbones) et régule...

La thiolase est une enzyme qui catalyse la scission d'un composé par un thiol. Le clivage thiolytique du thioester est catalysé par la bêta-cétoacyl...
