Thiol
Définition
Un thiol est un composé chimique organique similaire à un alcool et à un phénol (organooxygénés) mais un atome de soufre (organosulfuré, R–SH) remplace l'atome d'oxygène des alcools (R–OH). Les thiols sentent mauvais, ce qui permet leur détection olfactive.
Un thiol est un composé organique dérivé d'un alcool dans lequel l'atome d'oxygène du groupe alcool a été remplacé par un atome de soufre. Le groupe fonctionnel lui-même est également nommé avec thiol ou sulfhydryle.
Structures de thiols :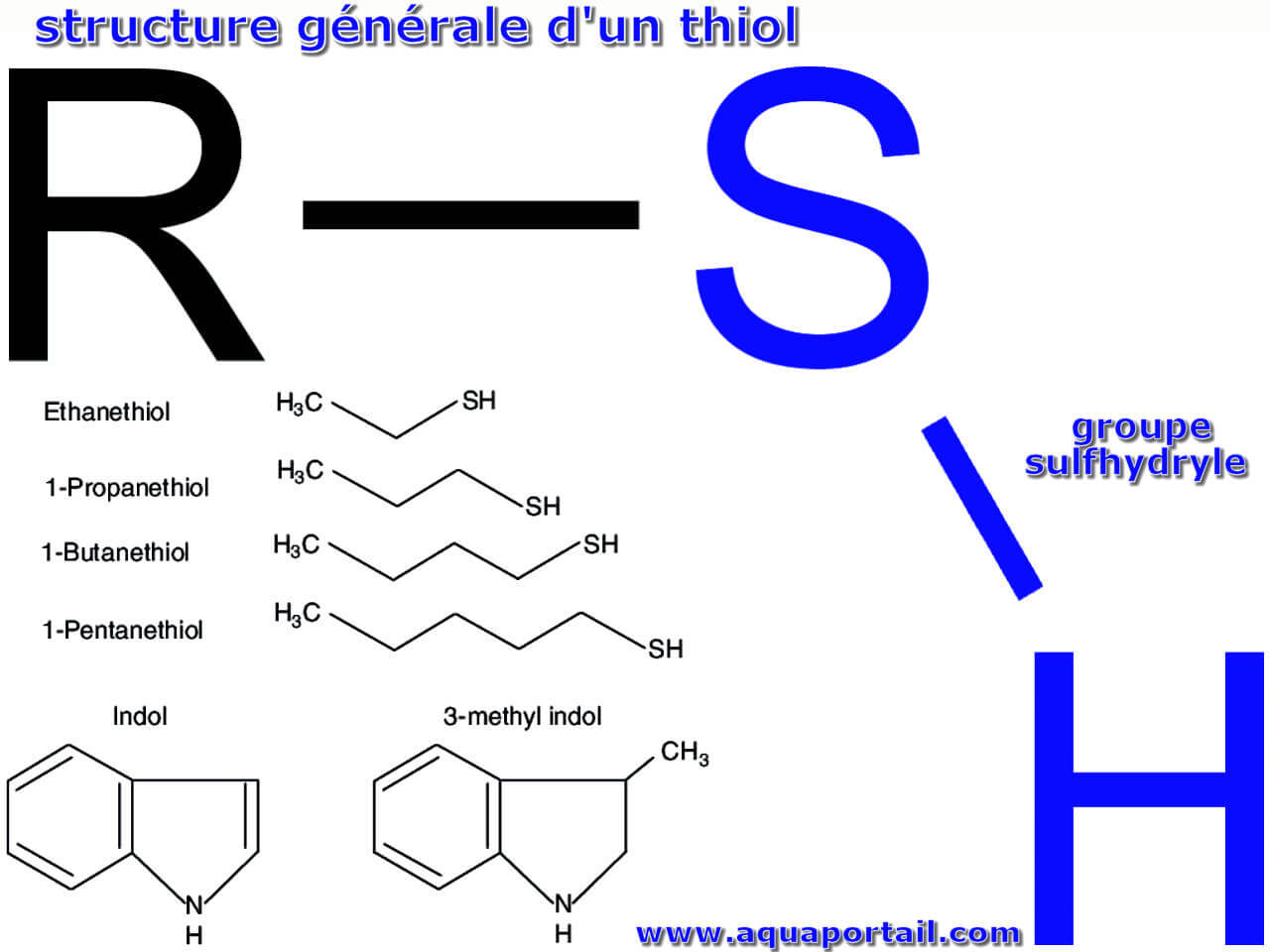
Le thiol est un composé de formule générale R–SH, où R est un radical organique (alkyle ou aryle) et –SH le groupe sulfhydryle (indiqué en bleu). En plus, le schéma intègre la structure chimique des thiols (éthanethiol, butanethiol...) et des indols utilisés comme stimuli olfactifs.
Explications
Les thiols contiennent un composé sulfuré qui leur donne une vilaine puanteur. Le sulfure d'hydrogène (H2S) est responsable de l'odeur des oeufs pourris et de la mauvaise haleine, entre autres choses désagréables. Les thiols contribuent à l'odeur des mouffettes et de certaines bières. Le meilleur ami des chimistes du soufre est l'eau de javel, qui oxyde les thiols puants en sulfoxydes relativement inodores.
Les thiols sont plus nucléophiles que les alcools et les thiolates sont plus nucléophiles que les alcoxydes. Étant donné que la nucléophilie est mesurée par la vitesse de réaction, cela signifie que ces nucléophiles soufrés ont tendance à réagir plus rapidement avec les électrophiles typiques (comme les halogénures d'alkyle) que leurs cousins à base d'oxygène.
Caratéristiques
Les alcools sont relativement acides (pKa d'environ 16–17). Les thiols sont plus acides que les alcools en moyenne d'environ 5 unités de pKa environ (pKa d'environ 11 pour le thiol). N'oubliez pas que pKa est logarithmique, ce qui signifie qu'ils sont environ 105 fois plus acides.
Lors de la compréhension des tendances de l'acidité, il est très utile de penser à la stabilité de la base conjuguée. Rappelez-vous que l'acidité sera augmentée par tout facteur qui stabilise la base conjuguée. Puisque les réactions acido-basiques sont des équilibres, si on stabilise le produit (base conjuguée), on rend donc plus favorable l'équilibre où le matériau de départ (acide) perd un proton, augmentant Ka. Autrement dit, on augmente l'acidité. Dans le cas du soufre, la charge négative sera portée sur un atome plus gros (soufre → oxygène) et cette charge négative sera dispersée sur un plus grand volume. Plus de volume = plus de charge diffuse = plus de stabilité.
Un corollaire du fait que la base conjuguée est plus stable est que les thiolates (les bases conjuguées des thiols) sont des bases plus faibles que les alcoxydes. Plus l'acide est fort, plus la base conjuguée est faible.
Si vous pouvez aller au-delà de leurs odeurs nauséabondes, les thiols ont beaucoup de caractéristiques similaires aux alcools :
- Comme les alcools, ils peuvent être déprotonés avec une base et subir des réactions S N 2 avec des halogénures d'alkyle pour donner des thioéthers (sulfures).
- Les thiols ont tendance à être considérablement plus acides que les alcools car l'atome de soufre est plus polarisable.
- Leurs bases conjuguées, les thiolates, sont d'excellents nucléophiles.
- Les thiols peuvent subir une oxydation pour donner des disulfures.
Mercaptan
Mercaptan est un terme obsolète synonyme de thiol, découvert par le chimiste organicien danois William Christopher Zeise (1789–1847), mais il est encore un peu utilisé. Cet ancien nom des thiols est dérivé du fait que ces composés ont une excellente capacité à lier le mercure. Cela est dû à la nature douce du soufre et du mercure. Le terme mercaptan est dérivé du latin mercurium captans (capteur de mercure).
Synonymes, antonymes
Voir tous les synonymes pour "thiol".2 synonymes (sens proche) de "thiol" :
- groupe thionyle
- mercaptan
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à THIOL sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
Le mot THIOL est dans la page 2 des mots en T du lexique du dictionnaire.
Mots en T à proximité
thigmotaxie thigmotropisme thigmotropogenèse Thiobacillus thioester thiolthiolase thiolate thiophène thiorédoxine thiosulfate d'ammonium
En rapport avec "thiol"
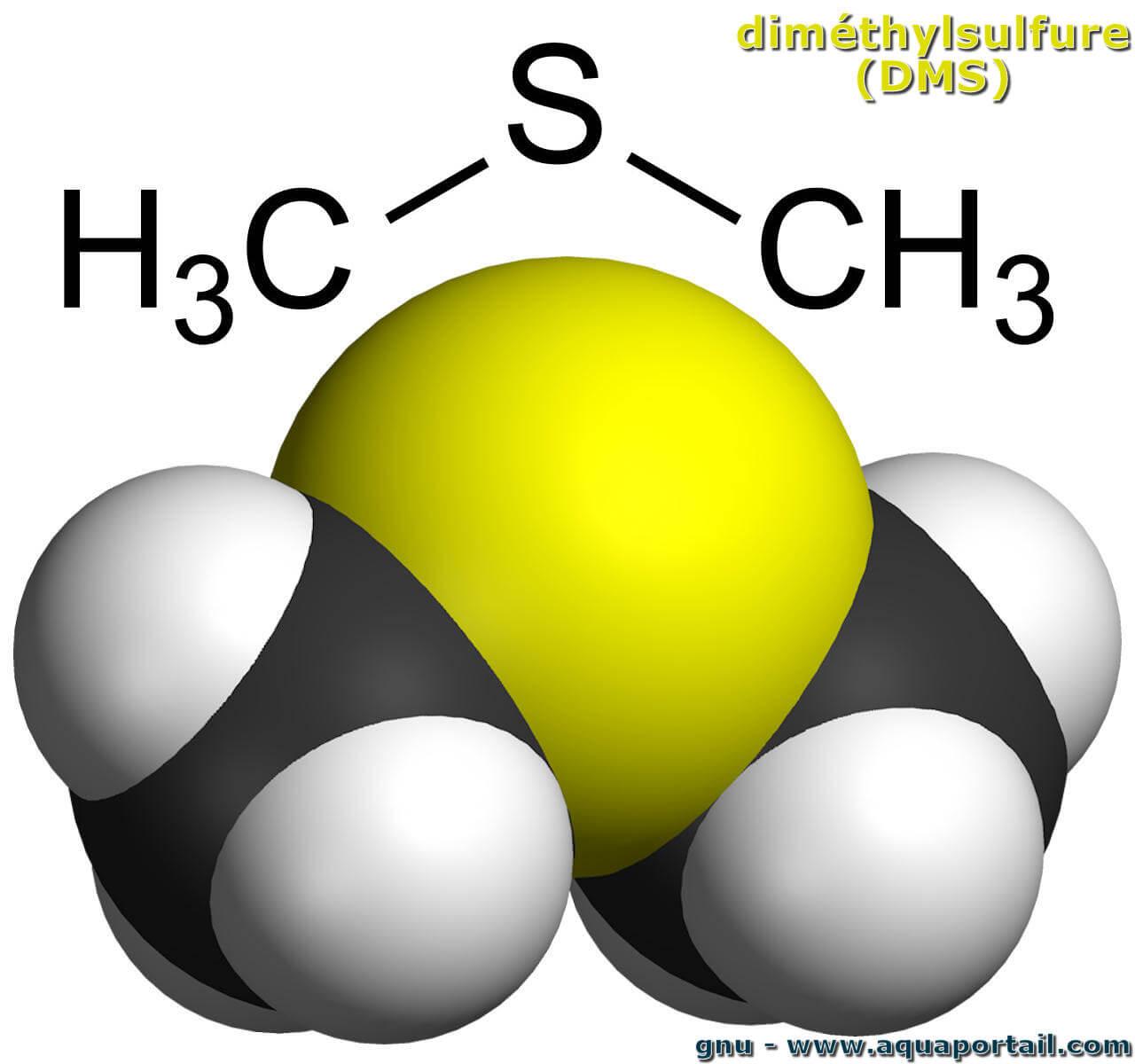
Le diméthylsulfure (DMS, sulfure de diméthyle) est un composé chimique volatile, un thioéther, de formule moléculaire (CH₃)₂S.
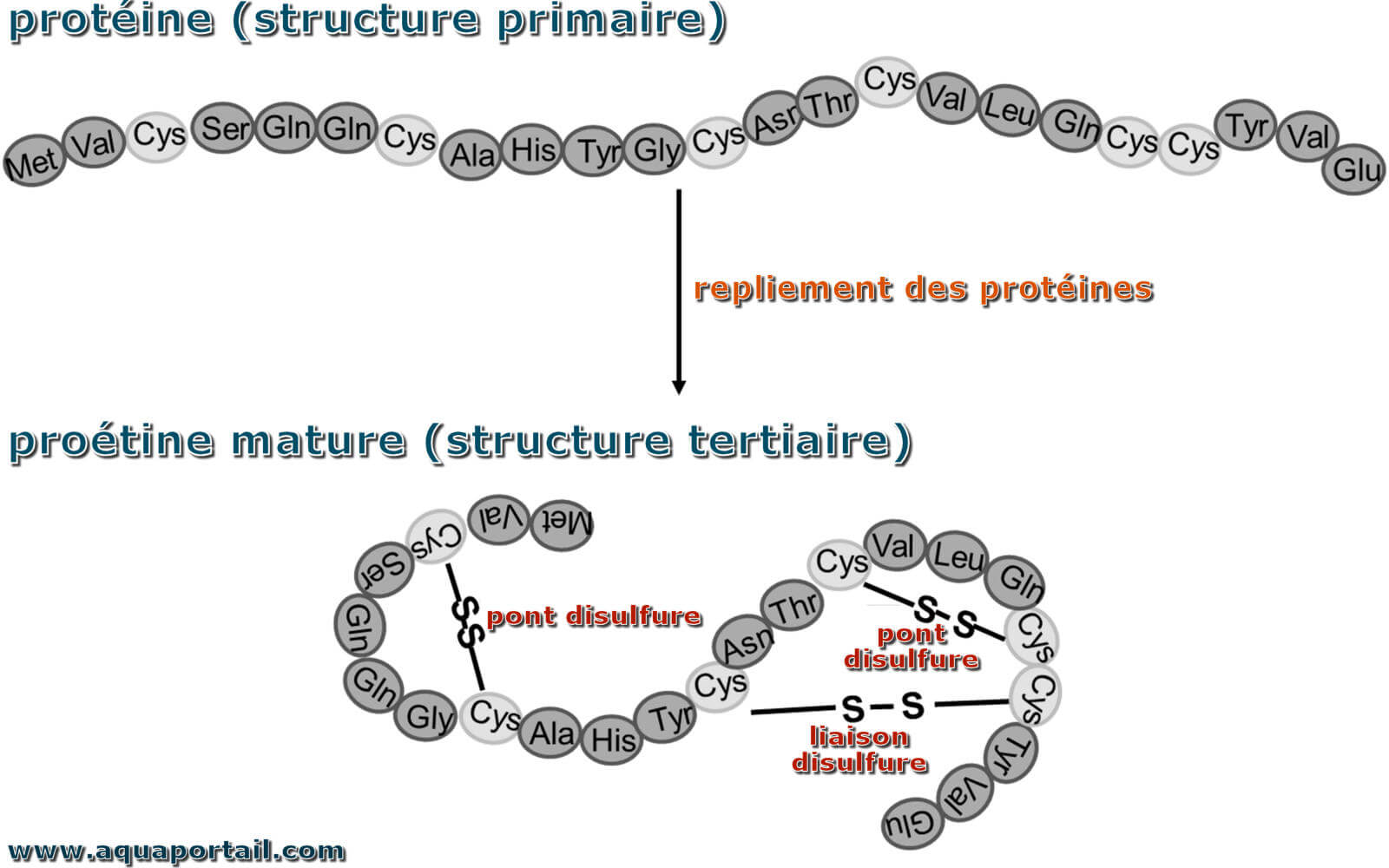
Un pont disulfure consiste en une liaison entre deux atomes de soufre d'une protéine contribuant à la stabilisation de sa structure tertiaire ou quaternaire.

Le sulfure est un anion inorganique du soufre (l'anion soufre le plus simple) de formule chimique S²⁻ ou un composé contenant un ou plusieurs ions S²⁻.

Le sulfure d'hydrogène est un gaz composé de d'hydrogène et de soufre, de symbole chimique H₂S.
