Méthanol
Définition
Le méthanol est un alcool, un composé chimique également connu sous le nom d'alcool méthylique, alcool à brûler, carbinol ou alcool de bois. Il est l'alcool le plus simple. À température ambiante, il apparaît comme un liquide léger, incolore, inflammable et toxique qui sert d'antigel, de solvant et de carburant. Sa formule chimique brute est CH4O.
Molécule de méthanol :
La molécule de méthanol, un composé organique, est de formule topologique CH3OH. La température d'auto-inflammation est de 658 K (385 °C).
Explications
Le méthanol est un alcool liquide inflammable toxique, incolore et volatil, fabriqué à l'origine par distillation à partir de bois et maintenant principalement par oxydation du méthane.
Le méthanol est principalement utilisé comme solvant industriel pour aider à créer des encres, des résines, des adhésifs et des colorants. Il est également utilisé comme solvant dans la fabrication d'ingrédients et de produits pharmaceutiques importants tels que le cholestérol, la streptomycine, les vitamines et les hormones.
Histoire
Le méthanol a été utilisé dans le processus d'embaumement, mais les anciens Égyptiens utilisaient un mélange de substances, y compris le méthanol, qu'ils ont obtenu par pyrolyse du bois. Cependant, en 1661, Robert Boyle, a isolé le méthanol pur, quand il l'a produit à travers la distillation de buis. Plus tard, il est devenu connu sous le nom de l'esprit pyroxyle. En 1834, les chimistes français Jean-Baptiste Dumas et Eugène Peligot déterminèrent sa composition élémentaire. Ils ont également introduit le mot méthylène dans la chimie organique. L'intention était de signifier "l'alcool fait de bois", mais il y a des erreurs dans la langue grecque : le mot "bois" est mal utilisé, et un ordre de mots erroné dû à l'influence de la langue française. Le terme "méthyle" a été créé vers 1840 par l'abréviation de méthylène, et a été plus tard utilisé pour décrire l'alcool méthylique; expression que la Conférence internationale sur la nomenclature chimique réduite à "méthanol" en 1892.
En 1923, les chimistes allemands Alwin Mittasch et Pier Mathias, qui travaillent pour BASF, développent un moyen de convertir un gaz de synthèse (un mélange de monoxyde de carbone, de dioxyde de carbone et d'hydrogène) en méthanol. Le brevet a été déposé le 12 janvier 1926 (numéro de référence 1569 775). Ce procédé utilise un catalyseur à l'oxyde de chrome et au manganèse et nécessite des pressions extrêmement élevées allant de 50 à 220 atm et des températures allant jusqu'à 450 °C, plus du tout à température ambiante. La production de méthanol moderne est plus efficace : des catalyseurs (généralement du cuivre) capables de fonctionner à des pressions plus faibles sont utilisés. Le méthanol moderne à basse pression (LPM) a été développé par ICI à la fin des années 1960 avec la technologie actuellement détenue par Johnson Matthey, qui est un des principaux donneurs de licence de la technologie du méthanol.
L'utilisation du méthanol comme carburant automobile a attiré l'attention au cours des crises pétrolières des années 1970 en raison de sa disponibilité, de son faible coût et des avantages environnementaux. Au milieu des années 1990, plus de 20 000 "véhicules à carburant flexible" (VCF) capables de fonctionner au méthanol ou à l'essence ont été vendus aux États-Unis. En outre, pendant la majeure partie des années 1980 et au début des années 1990, de petites quantités de méthanol sont mélangées dans les carburants à essence vendus en Europe. À la fin des années 1990, les constructeurs automobiles ont cessé de fabriquer des fours à base de méthanol pour se concentrer sur les véhicules fonctionnant à l'éthanol. Bien que le programme de méthanol VCF ait été un succès technique, l'augmentation du prix du méthanol au milieu et à la fin des années 1990 pendant une période de baisse des prix de l'essence a diminué l'intérêt pour le méthanol comme carburant.
Applications
Le méthanol, comme tout alcool, a plusieurs utilisations. C'est un solvant industriel et est utilisé comme matière première dans la fabrication du formaldéhyde. Le méthanol est également utilisé comme antigel dans les véhicules, le carburant de camping, les solvants pour les encres, les colorants, les résines, les adhésifs, les biocarburants et l'aspartame. Le méthanol peut également être ajouté à l'éthanol pour le rendre impropre à la consommation humaine (le méthanol est hautement toxique) et pour les véhicules modèles à moteur à combustion interne.
Toxicité
En concentrations élevées (ou inférieures par rapport à l'alcool éthylique), le méthanol peut provoquer des maux de tête, des étourdissements, des nausées, des vomissements et la mort (l'ingestion d'une dose comprise entre 20 ml et 150 ml est fatale). L'exposition aiguë peut causer la cécité ou la perte de vision, car elle peut endommager sérieusement le nerf optique (neuropathie optique). L'exposition chronique peut causer des dommages au foie ou une cirrhose.
L'empoisonnement au méthanol et son association avec une toxicité sévère sur le système nerveux central et oculaire constituent un problème de santé. Les caractéristiques cliniques de l'intoxication aiguë au méthanol comprennent l'acide formique, l'acidose métabolique, la toxicité visuelle, le coma et, dans les cas extrêmes, la mort.
Le méthanol est métabolisé en formaldéhyde dans le foie, et par des oxydations successives à travers un tétrahydrofuranne (THF), l'acide formique et le dioxyde de carbone se forment.
L'acide formique est le métabolite responsable des effets toxiques du méthanol, qui inhibe la cytochrome oxydase, interférant avec le transport des électrons dans la chaîne respiratoire. Inhibe la fonction mitochondriale dans la rétine et augmente le stress oxydatif. Son action cytotoxique s'exerce différemment sur les photorécepteurs, avec une récupération partielle des réponses dominées par les bâtonnets et aucune récupération sur les réponses médiées par les cônes ultraviolets.
La gravité de l'empoisonnement au méthanol est causée par les acides générés dans votre métabolisme par l'intermédiaire de l'enzyme alcool déshydrogénase (ADH). Ces métabolites s'accumulent dans le corps dans les 12–24 heures après l'intoxication. L'éthanol agit comme un antidote car il se lie de manière sélective et compétitive à l'ADH, par la même voie enzymatique.
Alors que le métabolisme du méthanol donne naissance à l'acide formique, responsable de sa toxicité, l'éthanol entre en compétition avec l'ADH et génère de l'acétaldéhyde, qui devient finalement l'acétyl coenzyme A (acétyl-CoA), pour la synthèse des acides gras.
Biométhanol
Dans l'industrie liée à la production de vin, le méthanol provient de la déméthylation enzymatique des pectines présentes dans la paroi cellulaire du raisin et, par conséquent, sa concentration dans les vins sera déterminée par la concentration de pectines dans le moût, qui dépend de la variété des raisins utilisés, de la concentration des enzymes et du degré d'activité de ces derniers.
Dans la pile à combustible, nous travaillons sur son application à base de méthanol qui peut être extrait de produits végétaux et intégrer un processus de génération durable naturel et écologique.
Synonymes, antonymes
5 synonymes (sens proche) de "méthanol" :
- alcool
- alcool à brûler
- alcool de bois
- alcool méthylique
- carbinol
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à MÉTHANOL sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
Le mot METHANOL est dans la page 3 des mots en M du lexique du dictionnaire.
Mots en M à proximité
méthane méthanesulfonate méthanisation méthanogène méthanogenèse méthanolméthanotrophe méthémoglobine méthionine méthode Balling méthode berlinoise
En rapport avec "méthanol"

Un acide-alcool désigne une substance organique possédant les fonctions acide et alcool, avec au moins une fonction acide carboxylique et une fonction alcool.

Est acido-alcoolo-résistante une coloration différentielle de mycobactéries consistant en un chauffage avec de la fuchsine et du phénol puis en un lavage avec...

L'alcool est tout composé organique dans lequel la fonction hydroxyle (-OH) est liée à un atome de carbone saturé.
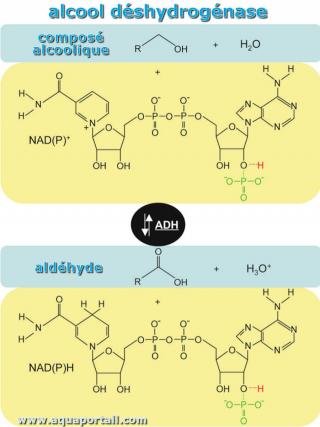
L'alcool déshydrogénase (ADH) est une enzyme protéique de type déshydrogénase que les organismes vivants ont développé pour faire face aux substrats...
