Acide aspartique
Définition
L'acide aspartique (Asp) est un acide aminé dicarboxylique constitutif des protéines dont la forme ionisée, l'aspartate, est l'un des vingt acides aminés avec lesquels les cellules forment des protéines. L'acide L–aspartique est un composant de l'aspartame. Dans l'ARN, il est codé par les codons GAU ou GAC.
Structure de l'acide aspartique :
L'acide aspartique, ou acide 2-aminobutanedioïque, possède un groupe carboxyle -COOH à l'extrémité de la chaîne latérale. Sa formule chimique est HOOC-CH2-CH(NH2)-COOH.
Explications
Au pH physiologique, l'acide aspartique a une charge négative (acide); Il appartient au groupe des acides aminés à chaînes latérales polaires chargées. Ce n'est pas un acide aminé essentiel car il peut être synthétisé par l'organisme humain. Sa biosynthèse a lieu par transamination de l'acide oxalacétique, un métabolite intermédiaire du cycle de Krebs.
L'acide aspartique a été découvert en 1827 par les chimistes français Auguste-Arthur Plisson et Étienne Ossian Henry, dérivés de l'asparagine, qui avait été isolée du jus d'asperge en 1806, en la faisant bouillir avec une base.
Réactions
Il intervient dans de nombreuses réactions métaboliques :
- Lors de la synthèse des ribonucléosides pyrimidiques, il se lie au carbamylphosphate grâce à une aspartate transcarbamylase pour former le carbamylaspartate, précurseur des ribonucléosides;
- Par transamination avec Pa-cétoglutarate, il donne de l'oxaloacétate : il est donc glucoformateur;
- Par désamination, il donne de l'acide acétique;
- Par décarboxylation, il donne l'α-alanine et la β-alanine;
- Dans le cycle de l'urée, il se lie à la citrulline pour former l'acide arginosuccinique.
- Chez certaines plantes en C4 appelées plantes à aspartate (Amaranthus, Atriplex, Eragrostis), c'est une forme de réserve de CO2, dans les chloroplastes des cellules du mésophylle et de transfert du CO2, aux mitochondries des cellules de la gaine périvasculaire. Il est synthétisé par amination réductrice de l'oxaloacétate.
L'acide aspartique est acide en raison de ses deux groupes carboxyles. Par conséquent, cet acide aminé est physiologiquement - en fonction du pH - habituellement sous la forme d'un sel interne sous la forme d'un aspartate.
Utilisations
Des quantités importantes d'acide L–aspartique sont utilisées pour fabriquer l'édulcorant aspartame. De plus, l'acide L–aspartique est utilisé comme matériau de départ pour la synthèse stéréosélective de divers autres composés organochimiques chiraux. Les esters polyaspartiques N-substitués sont utilisés comme composants réactifs dans les systèmes de peinture modernes.
De plus, l'acide L–aspartique est utilisé en tant que composant de solutions de perfusion pour la nutrition parentérale et en tant que formateur de sel
Métabolisme
L'aspartate n'est pas essentiel chez les mammifères, étant produit à partir d'oxaloacétate par une réaction de transamination. Il est également synthétisé à partir d'eftalimidomalonate de diéthyle sodique.
L'acide L–aspartique a été synthétisé pour la première fois à partir de l'asparagine trouvée dans les semis de légumineuses.
L'asperge végétale Asparagus officinalis contient également des niveaux assez élevés de cet acide aminé. On le trouve dans presque toutes les protéines liées, dans des proportions différentes.
Pour les aliments suivants riches en acides L–asparaginiques, les données sont basées sur chaque fois 100 g de l'aliment.
Biosynthèse
La biosynthèse de l'acide L–aspartique a lieu par exemple à partir de l'oxaloacétate de céto-acide homologue par transamination. Industriellement, l'acide L–aspartique est obtenu énantio-sélectivement par un procédé biotechnologique par addition d'ammoniac à la double liaison C=C de l'acide fumarique. Un microorganisme avec l'enzyme L–aspartase est utilisé.
Fonctions
On croit que le L–aspartate, la base conjuguée de l'acide aspartique, joue le rôle de transmetteur dans plus de 50 % des synapses du système nerveux central chez les vertébrés ainsi que de l'acide glutamique, y compris dans les fibres grimpantes du cervelet et les fibres moussues de la corne d'Ammons. Cela fonctionne via la stimulation des récepteurs NMDA. Cependant, l'effet n'est pas aussi fort qu'avec le glutamate.
En outre, l'acide L- aspartique dans le cycle de l'urée par l'enzyme argininosuccinate synthétase est combiné à la citrulline avec clivage de l'ATP en AMP et du PP i en argininosuccinate. Celle-ci est ensuite divisée par l'argininosuccinate lyase en L–arginine et en fumarate. La L–arginine libère alors de l'urée, tandis que le fumarate est reconverti dans le cycle du citrate en oxaloacétate, qui peut être retransféré en L–aspartate (transfert de groupes amino de l'α-aminoacide en urée par transamination d'oxaloacétate).
Synonymes, antonymes
Voir tous les synonymes pour "acide aspartique".2 synonymes (sens proche) de "acide aspartique" :
- acide 2-aminobutanedioïque
- aspartate
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à ACIDE ASPARTIQUE sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
L'expression ACIDE ASPARTIQUE est dans la page 1 des mots en A du lexique du dictionnaire.
Mots en A à proximité
acide aminé acide aminé essentiel acide arachidique acide arachidonique acide ascorbique acide aspartiqueacide benzoïque acide bêta-hydroxybutyrique acide biliaire acide borique acide butanedioïque
En rapport avec "acide aspartique"
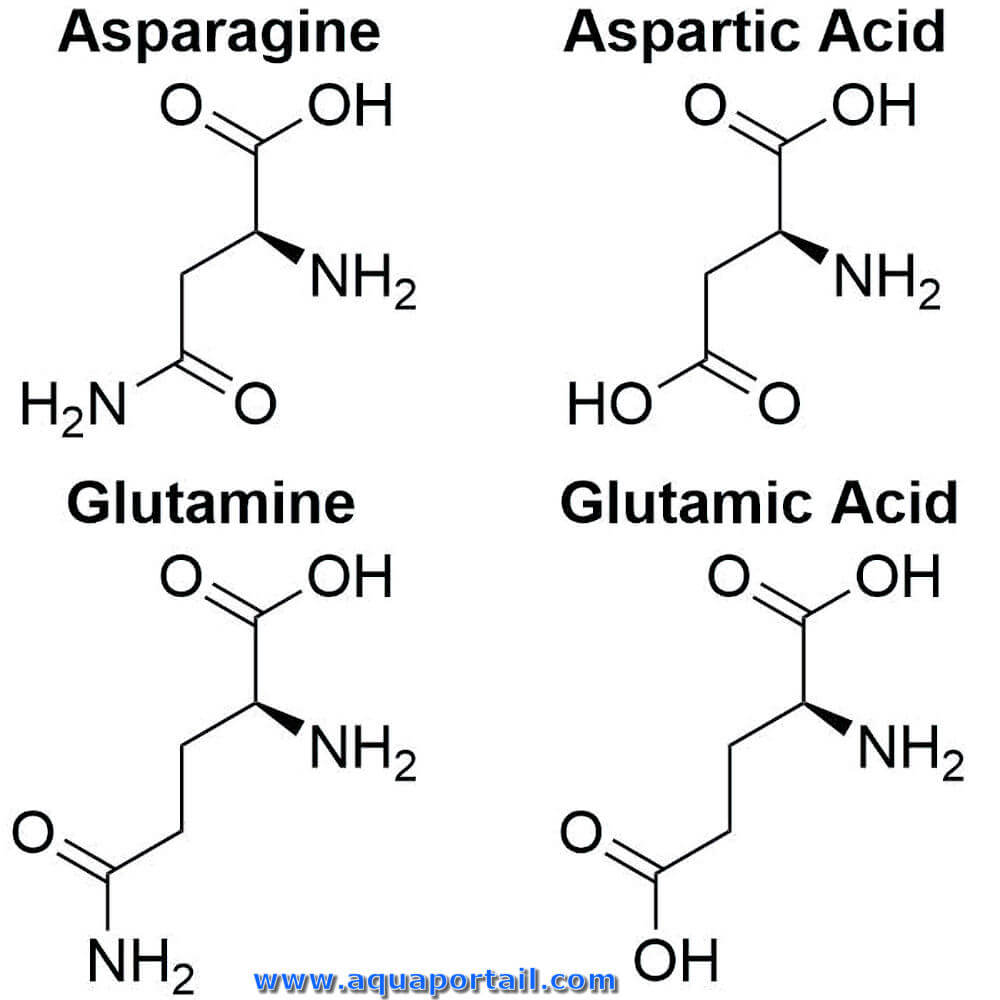
L'asparagine est un acide aminé (non essentiel chez l'Homme) qui entre dans la constitution des protéines des êtres vivants.

L'aspartame E951 est un édulcorant synthétique non calorique utilisé comme additif alimentaire, environ150–200fois plus sucré que le sucre.

L'aspartate est la forme ionisée d'un acide aminé protéinogène, l'acide aspartique qui entre pour 40 % dans la composition de l'aspartame.

La famille Asparagaceae appartient à l'ordre des asperges Asparagales au sein des monocotylédones.
