Transamination
Définition
La transamination est une réaction chimique dans laquelle le groupe α-aminé d'un acide aminé est transféré à un acide α-céto (généralement au α-cétoglutarate), générant en même temps un nouvel acide aminé et l'acide α-céto correspondant à l'amino. Des transaminases interviennent.
La transamination est un transfert d'un groupement amine d'un acide aminé à un autre. Elle fait aussi référence à un déplacement du groupe α-aminé d'un acide aminé en un acide α-céto. Cette réaction est catalysée par les aminotransférases et le coenzyme phosphate de pyridoxal. Le pyridoxal-5′-phosphate (PLP) est la forme active de la pyridoxine (vitamine B6).
Processus de transamination :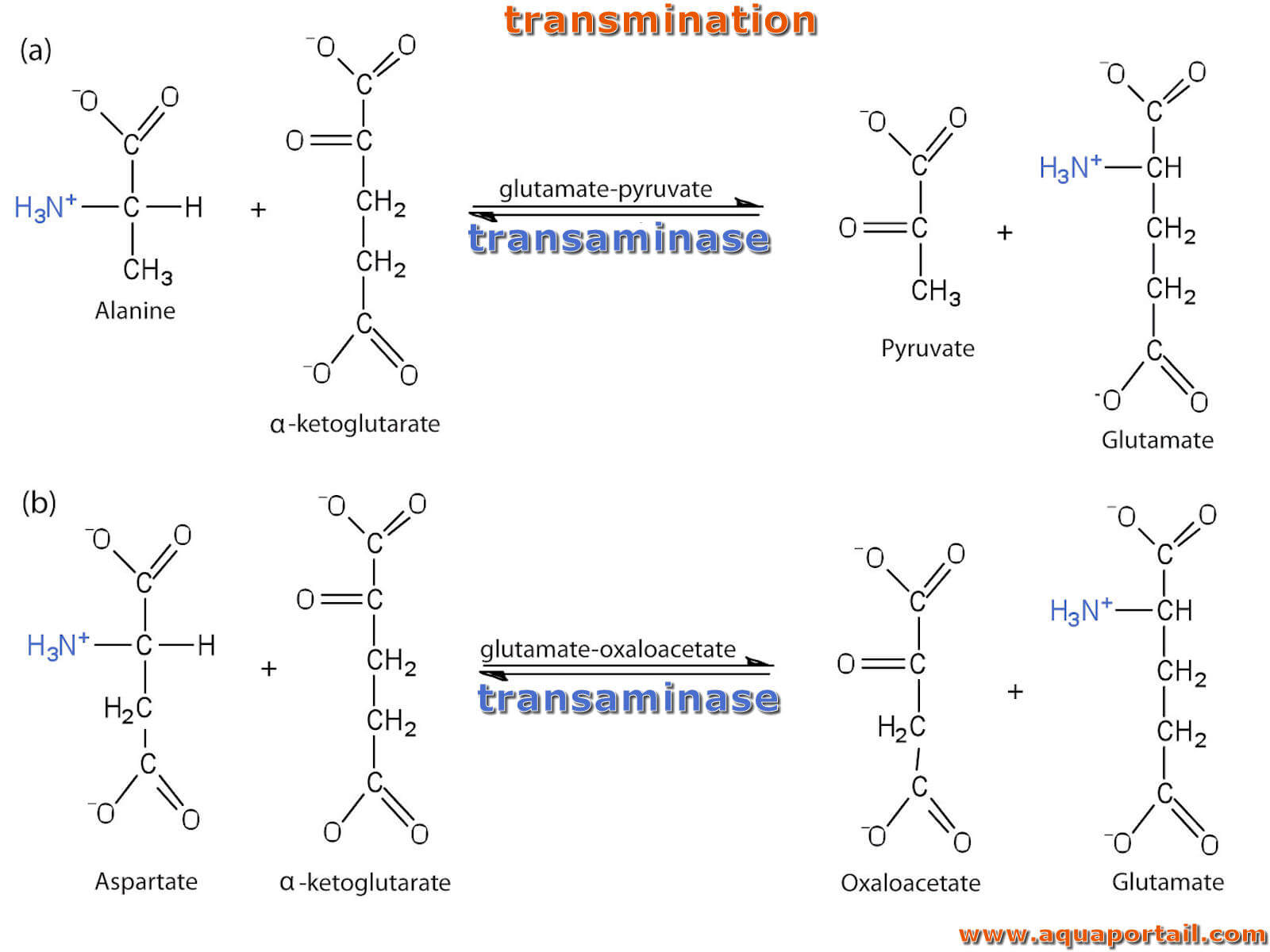
Dans les deux réactions de transamination de l'alanine et l'aspartate, ci-dessus, l'accepteur final du groupe amino est l'α-cétoglutarate et le produit final est le glutamate.
Explications
La transamination est un échange de groupes fonctionnels entre n'importe quel acide aminé (à l'exception de la lysine, de la proline et de la thréonine) et un acide -céto. Le groupe amino est généralement transféré à l'atome de carbone céto du pyruvate, de l'oxaloacétate ou du -cétoglutarate, convertissant l'acide α-céto en alanine, aspartate ou glutamate, respectivement. Les réactions de transamination sont catalysées par des transaminases spécifiques (également appelées aminotransférases), qui nécessitent le phosphate de pyridoxal comme coenzyme.
La réaction catalysée par la transaminase se déroule en deux étapes. Dans le premier, le groupe α-aminé d'un acide aminé est transféré à l'enzyme, produisant l'α-cétoacide correspondant et la forme amine de la coenzyme PLP, appelée PMP (pridoxamine-5′-phosphate). Dans la deuxième étape, le groupe amino est transféré à l'acétoacide accepteur, générant le nouvel acide aminé et restaurant la coenzyme PLP à sa forme initiale.
La transamination représente la première étape du catabolisme des acides aminés, étant la voie métabolique qui permet la désamination de la plupart des acides aminés. De plus, les réactions de transamination permettent de convertir les acides aminés essentiels en acides aminés non essentiels (c'est-à-dire ceux que le corps est capable de synthétiser à partir de zéro).
D'un point de vue biochimique, les réactions sont catalysées par différentes enzymes, appelées aminotransférases ou transaminases, chacune étant spécifique d'un acide aminé donné. Puisqu'il s'agit d'une réaction dans un état d'équilibre, les produits de la réaction dépendent de la disponibilité des différents α-cétoacides présents à l'intérieur de la cellule.
Le processus inverse de transamination est la désamination.
L'importance et le mécanisme de la transamination avec transaminases dans le métabolisme ont été reconnus par le biochimiste russe Alexander E. Braunstein à partir des années 1930.
Transamination des acides aminés
La transamination des acides aminés est la réaction entre un acide aminé et un alpha-cétoacide, dans lequel le groupe amino est transféré vers un α-cétoacide.
Après la formation de glutamate, le glutamate transfère son groupe amino directement à une variété d'acides alpha-céto par diverses réactions de transamination réversibles : don librement réversible d'un groupe alpha amino d'un acide aminé au groupe α-cét d'un acide α-céto acide, accompagné de la formation d'un nouvel acide aminé et d'un nouvel acide α-céto.
Ces réactions sont effectuées par des enzymes appelées aminotransférases. Toutes ces enzymes nécessitent du phosphate de pyridoxal (vitamine B6) comme groupe prothétique, une raison importante pour laquelle cette vitamine est essentielle à la vie.
Un exemple important de transamination survient entre le glutamate et l'oxaloacétate, qui produit de l'alpha-cétoglutarate et de l'aspartate, qui peuvent transférer leur groupe amino à d'autres alpha-cétoacides pour former différents acides aminés par des réactions de transamination. De cette manière, l'organisme peut produire ou décomposer lui-même des acides aminés non essentiels. Cette réaction est l'une des deux méthodes qui permettent l'introduction du groupe amino dans le cycle de l'urée.
Transamination des sels d'ammonium
La transamination des sels d'ammonium est la substitution nucléophile d'une amine ou d'un anion amide dans un sel d'ammonium. Par exemple, la fixation d'un anion amide à une amine primaire est utilisée pour produire des amines secondaires.
En laboratoire, il est possible de préparer des amines secondaires symétriques en utilisant du nickel de Raney (2 RNH2 → R2NH + NH3). Enfin, les sels d'ammonium quaternaire peuvent être désalkylés à l'aide d'éthanolamine.
Les aminonaphtalènes subissent également une réaction de transamination lors de leur catabolisme.
Types d'aminotransférase
La réaction de transamination peut être catalysée par différentes enzymes : elles peuvent être spécifiques à des acides aminés uniques, ou elles peuvent catalyser la réaction pour des groupes d'acides aminés composés d'unités chimiquement similaires, comme cela existe pour le groupe des acides aminés à chaîne ramifiée, qui comprend la leucine, isoleucine et valine. Les types de transaminases les plus courants sont l'alanine transaminase (ALT) et l'aspartate aminotransaminase (AST).
Synonymes, antonymes
Voir tous les synonymes pour "transamination".0 synonyme (sens proche) pour "transamination".
1 antonyme (sens contraire) :
Les mots ou les expressions apparentés à TRANSAMINATION sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
Le mot TRANSAMINATION est dans la page 3 des mots en T du lexique du dictionnaire.
Mots en T à proximité
traitement tertiairetrame trame verte tranquilliseur transaminase transaminationtranscapsidation Transcaucasie transcriptase transcriptase inverse transcription
En rapport avec "transamination"
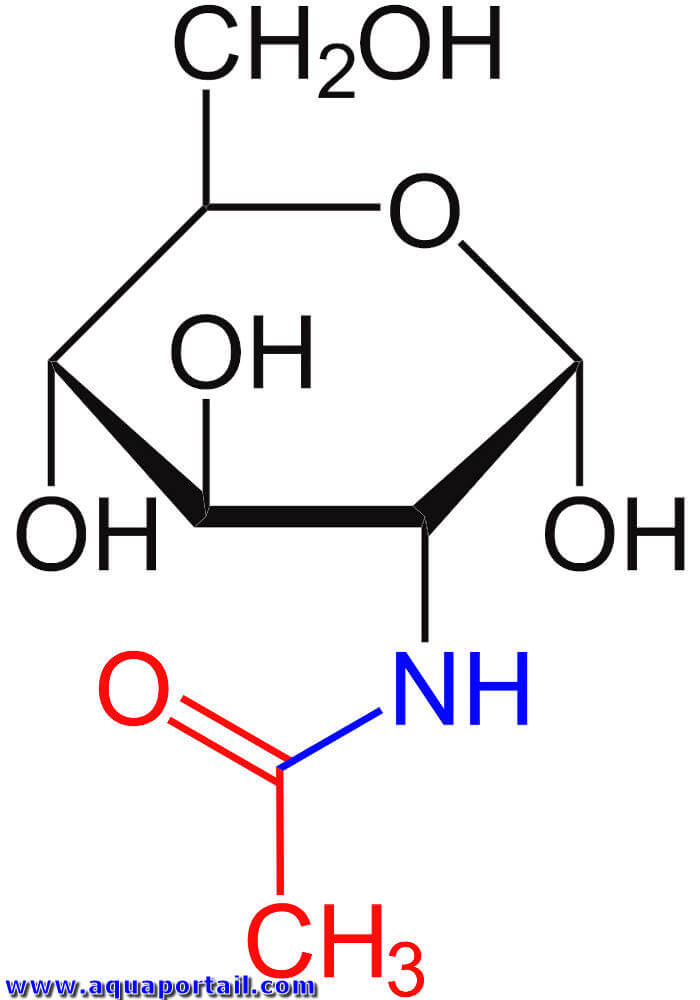
L'acétylglucosamine est un composé de sucre, d'un groupe amine et d'un groupe acétyle, proche de la cellulose.
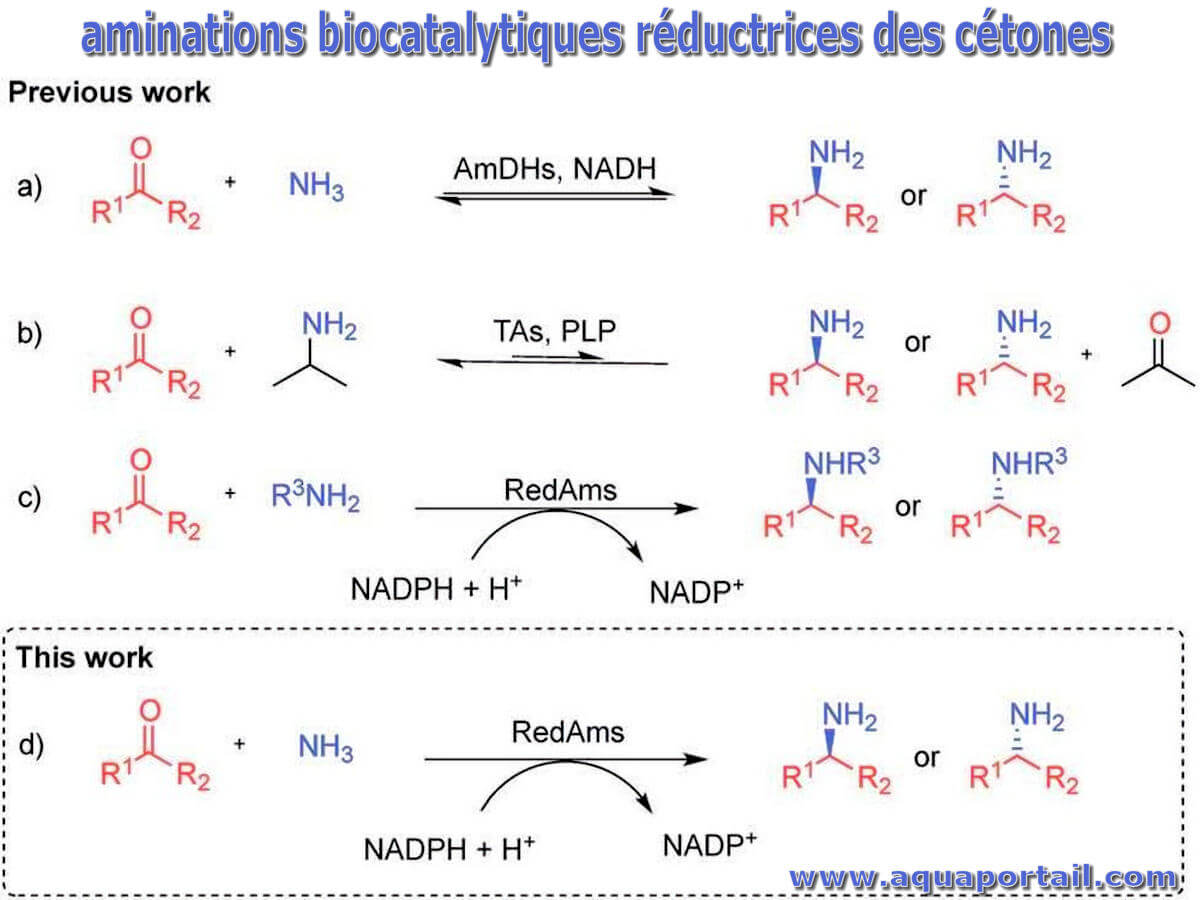
Une amination est une addition d'un groupement amine dans une molécule organique lors d'une réaction chimique, par une substitution nucléophile.

Une amine est généralement un groupe fonctionnel (groupe amino) dont l'atome d'azote possède un doublet non liant.

Une antivitamine est une substance chimiquement similaire à une vitamine, qui peut remplacer une vitamine ou un composé essentiel, mais sans en jouer le rôle.
