Acétylglucosamine
Définition
L'acétylglucosamine est un composé de sucre, d'un groupe amine et d'un groupe acétyle, proche de la cellulose. Sa polymérisation forme la chitine.
La N-acétylglucosamine est un composant acide de la muréine. On parle aussi de l'acide N-acétylmuramique. La formule chimique est C8H15NO6.
Structure de la N-acétylglucosamine :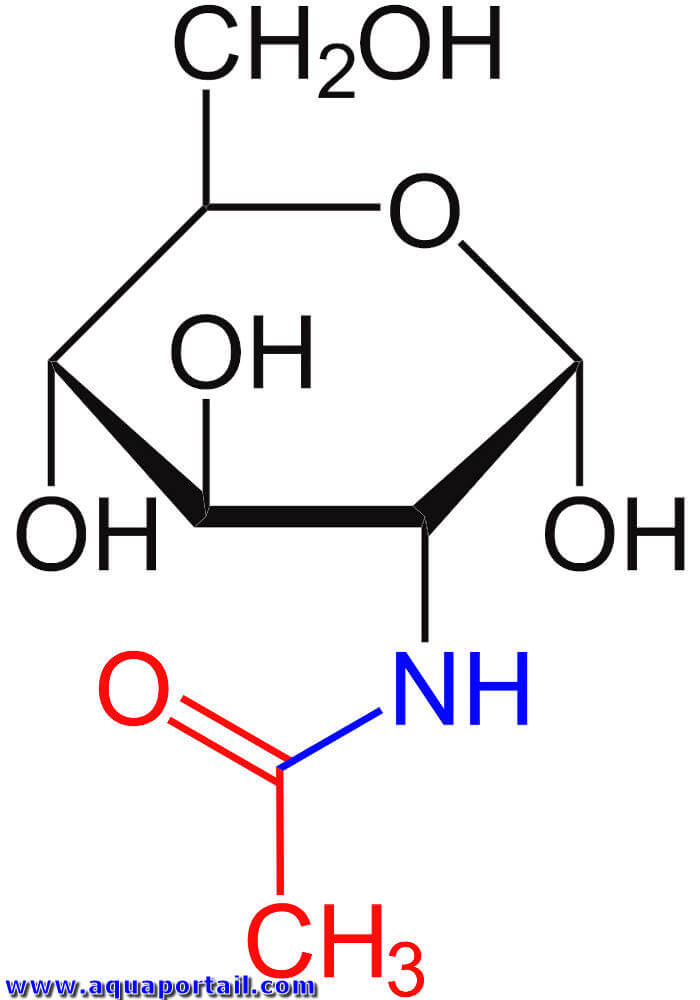
structure chimique de la N-acétyl-D-glucosamine : glucose (noir), amine (bleu), acétyle (rouge).
Explications
La N-acétylglucosamine, ou plus précisément la N-acétyl-D-glucosamine, est un dérivé acétylé de la glucosamine qui, à son tour, est un dérivé du glucose, un monosaccharide six carbones (aldohexose). Elle se distingue pour être l'un des constituants du peptidoglycane.
Les fonctions biologiques sont :
- composant fondamental du peptidoglycane car il forme un didisaccharide répété avec l'acide N-acétylmuramique (MurNAc);
- composant fondamental de l'acide hyaluronique car il forme un disaccharide répété avec l'acide glucuronique;
- composant fondamental de la chitine, un constituant structurel des champignons, de l'exosquelette des insectes et de nombreux autres arthropodes;
- neurotransmetteur.
La N-acétylglucosamine (GlcNAc), qui est un dérivé acétylé de la glucosamine (GlcN), est un composant de la chitine et du glycosaminoglycane (acide hyaluronique et chondroïtine) et a été largement utilisée dans les compléments alimentaires pour promouvoir et maintenir la santé des cartilages et des articulations osseuses. La méthode chimique, à savoir l'hydrolyse acide de la chitine brute des carapaces de crevettes ou de crabes, est la principale voie de production de GlcNAc. Cependant, cette méthode entraînera une pollution de l'environnement par les eaux usées et le produit pourra provoquer une réaction anaphylactique. Pour résoudre les problèmes mentionnés, des souches modifiées comprenant Escherichia coli, Bacillus subtilis, Corynebacterium glutamicum et Saccharomyces cerevisiae ont été construites pour la production de GlcNAc. De plus, de nombreux systèmes et méthodes d'ingénierie métabolique synthétique ont été appliqués pour améliorer la production de GlcNAc des souches modifiées.
La N-acétylglucosamine (NAG) est un substrat pour la synthèse des glycosaminoglycanes, des glycoprotéines qui protègent la muqueuse intestinale des dommages toxiques. La synthèse du NAG par N-acétylation de la glucosamine est altérée chez les patients atteints de MII (maladie inflammatoire de l'intestin). Dans les explants de tissu intestinal de patients, l'incorporation de NAG ajouté était diminuée chez les patients atteints de CU inactive, augmentant jusqu'à des niveaux témoins chez ceux atteints de colite active, indiquant probablement une réponse du tissu intestinal à l'inflammation. Dans une étude pilote, le NAG (3 à 6 g/jour pendant > 2 ans) administré par voie orale à des enfants atteints de MII réfractaire a produit une amélioration symptomatique chez la plupart des patients et une amélioration de l'histopathologie. Chez les enfants atteints de colite ou de rectite distale, la même dose de NAG a été administrée par lavement avec des effets similaires.
Synonymes, antonymes
Voir tous les synonymes pour "acétylglucosamine".0 synonyme (sens proche) pour "acétylglucosamine".
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à ACÉTYLGLUCOSAMINE sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
Le mot ACETYLGLUCOSAMINE est dans la page 1 des mots en A du lexique du dictionnaire.
Mots en A à proximité
acétylation acétylation des histones acétylcholine acétylcholinestérase acétylène acétylglucosamineacétyltransférase achaîne achat aquarium achatine achatiniculture
En rapport avec "acétylglucosamine"
La glucosamine est un dérivé aminé (C₆H₁₃NO₅) du glucose qui apparaît notamment comme constituant de substances structurelles comme la chitine...

Une acétylation est un transfert d'un groupe acétyle CH₃-CHO sur une molécule réceptrice.

L'acétylation des histones signifie la suppression de la charge positive de la molécule d'histone, ce qui affaiblit l'interaction entre les groupes phosphate...

Un acide acétylacétique qualifie un corps cétonique, un acide issu de la condensation de 3 molécules d'acétylcoenzyme A.
