L'homéostasie vasculaire
L'homéostasie vasculaire est un processus de régulation homéostatique du système vasculaire. Afin de maintenir l'homéostasie dans le système cardiovasculaire et de fournir suffisamment de sang aux tissus, le flux sanguin doit être redirigé continuellement vers les tissus au fur et à mesure qu'ils deviennent plus actifs.
Chiffres de l'homéostasie vasculaire :
L'homéostasie vasculaire implique une répartition du sang systémique au repos et pendant l'exercice. Bien que la plupart des données semblent logiques, les valeurs pour la distribution du sang au tégument peuvent sembler surprenantes. Pendant l'exercice, le corps distribue plus de sang à la surface du corps où il peut dissiper l'excès de chaleur généré par une activité accrue dans l'environnement.
Généralités
Dans un sens très réel, le système cardiovasculaire participe à l'allocation des ressources car il n'y a pas assez de circulation sanguine pour distribuer le sang de manière égale dans tous les tissus simultanément. Par exemple, lorsqu'un individu fait de l'exercice, une plus grande quantité de sang sera dirigée vers les muscles squelettiques, le coeur et les poumons. Après un repas, plus de sang est dirigé vers le système digestif. Seul le cerveau reçoit un apport de sang plus ou moins constant, que vous soyez actif, au repos, en train de penser ou engagé dans une autre activité.
Trois mécanismes homéostatiques assurent un flux sanguin, une tension artérielle, une distribution et, finalement, une perfusion adéquats : mécanismes neuronaux, endocriniens et autorégulateurs.
Régulation neuronale
Le système nerveux joue un rôle essentiel dans la régulation de l'homéostasie vasculaire. Les principaux sites régulateurs comprennent les centres cardiovasculaires cérébraux contrôlant les fonctions cardiaques et vasculaires. De plus, des réponses neuronales plus généralisées du système limbique et du système nerveux autonome sont des facteurs.
La régulation neurologique de la pression et du débit sanguin dépend des centres cardiovasculaires situés dans la médulla oblongue. Ce groupe de neurones répond aux variations de la pression artérielle ainsi qu'aux concentrations d'oxygène, de dioxyde de carbone et d'ions hydrogènes dans le sang. Le centre cardiovasculaire contient trois composants appariés distincts :
- Les centres cardio-accélérateurs stimulent la fonction cardiaque en régulant la fréquence cardiaque et le volume systolique via une stimulation sympathique du nerf de l'accélérateur cardiaque.
- Les centres cardio-inhibiteurs ralentissent la fonction cardiaque en diminuant la fréquence cardiaque et le volume systolique via la stimulation parasympathique du nerf vague.
- Les centres vasomoteurs contrôlent le tonus du vaisseau ou la contraction du muscle lisse dans le média tunique. Les variations de diamètre affectent la résistance périphérique, la pression et le débit, ce qui affecte le débit cardiaque. La majorité de ces neurones agissent via la libération du neurotransmetteur noradrénaline par des neurones sympathiques.
Bien que chaque centre fonctionne indépendamment, ils ne sont pas anatomiquement distincts.
Il existe également une petite population de neurones qui contrôlent la vasodilatation dans les vaisseaux cérébraux et les muscles squelettiques en relaxant les fibres musculaires lisses des tuniques vasculaires. Nombre d'entre eux sont des neurones cholinergiques, c'est-à-dire qu'ils libèrent de l'acétylcholine, qui à son tour stimule la libération par l'oxyde nitrique NO des cellules endothéliales des vaisseaux, ce qui provoque une vasodilatation. D'autres libèrent de la noradrénaline qui se lie aux récepteurs β2. Quelques neurones libèrent du NO directement en tant que neurotransmetteur.
Rappelez-vous qu'une légère stimulation des muscles squelettiques maintient le tonus musculaire. Un phénomène similaire intervient avec le tonus vasculaire dans les vaisseaux. Comme indiqué précédemment, les artérioles sont normalement partiellement rétrécies : avec une stimulation maximale, leur rayon peut être réduit à la moitié de l'état de repos. La dilatation complète de la plupart des artérioles nécessite la suppression de cette stimulation sympathique. Quand c'est le cas, une artériole peut se dilater jusqu'à 150 %. Une augmentation aussi importante peut affecter considérablement la résistance, la pression et le débit.
Les mécanismes neuronaux, endocriniens et autorégulateurs affectent le débit sanguin, la pression sanguine et éventuellement la perfusion de sang vers les tissus corporels. Les mécanismes neuronaux comprennent les centres cardiovasculaires de la moelle épinière, les barorécepteurs de l'aorte, des artères carotides et de l'oreillette droite, ainsi que des chimiorécepteurs associés qui surveillent les taux sanguins d'oxygène, de dioxyde de carbone et d'ions hydrogène. Les contrôles endocriniens comprennent l'épinéphrine et la noradrénaline, ainsi que l'ADH, le mécanisme rénine-angiotensine-aldostérone, l'ANH et l'EPO. L'autorégulation est le contrôle local de la vasodilatation et de la constriction par des signaux chimiques et la réponse myogénique. L'exercice améliore considérablement la fonction cardiovasculaire et réduit le risque de maladies cardiovasculaires, notamment l'hypertension, une des principales causes de crise cardiaque et d'accident vasculaire cérébral.Une hémorragie importante peut entraîner une forme de choc circulatoire appelée choc hypovolémique. Une sepsie, une obstruction et une inflammation généralisée peuvent également causer un choc circulatoire.
Réflexes barorécepteurs
Les barorécepteurs sont des récepteurs spécialisés dans les étirements situés dans de fines zones de vaisseaux sanguins et de cavités cardiaques qui répondent au degré d'étirement causé par la présence de sang. Ils envoient des impulsions au centre cardiovasculaire pour réguler la pression artérielle. Les barorécepteurs vasculaires se trouvent principalement dans les sinus (petites cavités) de l'aorte et des artères carotides : les sinus aortiques se trouvent dans les parois de l'aorte ascendante juste au-dessus de la valve aortique, tandis que les sinus carotides se trouvent à la base des artères carotides internes. Il existe également des barorécepteurs basse pression situés dans les parois de la veine cave et de l'oreillette droite.
Lorsque la pression artérielle augmente, les barorécepteurs sont étirés plus étroitement et initient des potentiels d'action plus rapidement. Lorsque la pression artérielle est basse, le degré d'étirement est plus faible et la cadence de tir plus lente. Lorsque le centre cardiovasculaire de la moelle oblongue reçoit cette entrée, il déclenche un réflexe qui maintient l'homéostasie :
- Lorsque la tension artérielle est trop élevée, les barorécepteurs se déclenchent plus rapidement et déclenchent une stimulation parasympathique du coeur. En conséquence, le débit cardiaque diminue. La stimulation sympathique des artérioles périphériques diminuera également, entraînant une vasodilatation. Ensemble, ces activités entraînent une chute de la pression artérielle.
- Lorsque la pression artérielle baisse trop, le taux de déclenchement des barorécepteurs diminue. Cela déclenchera une augmentation de la stimulation sympathique du coeur, entraînant une augmentation du débit cardiaque. Il déclenchera également une stimulation sympathique des vaisseaux périphériques, entraînant une vasoconstriction. La combinaison de ces activités entraîne une augmentation de la pression artérielle.
Les barorécepteurs de la veine cave et de l'oreillette droite contrôlent la pression artérielle à mesure que le sang retourne au coeur par la circulation systémique. Normalement, le flux sanguin dans l'aorte est identique au flux sanguin dans l'oreillette droite. Si le sang retourne plus rapidement dans l'oreillette droite qu'il ne l'est éjecté du ventricule gauche, les récepteurs auriculaires stimuleront les centres cardiovasculaires à augmenter le tir sympathique et le débit cardiaque jusqu'à l'obtention de l'homéostasie. L'inverse est également vrai. Ce mécanisme est appelé réflexe auriculaire.
Réflexes chimiorécepteurs
En plus des barorécepteurs, des chimiorécepteurs surveillent les niveaux d'oxygène, de dioxyde de carbone et d'ions hydrogène (pH), contribuant ainsi à l'homéostasie vasculaire. Les chimiorécepteurs qui surveillent le sang sont situés à proximité des barorécepteurs dans les sinus aortiques et carotidiens. Ils signalent le centre cardiovasculaire ainsi que les centres respiratoires de la moelle oblongue.
Étant donné que les tissus consomment de l'oxygène et produisent du dioxyde de carbone et des acides sous forme de déchets, lorsque le corps est plus actif, les niveaux d'oxygène chutent et le niveau de dioxyde de carbone augmente lorsque les cellules sont soumises à la respiration cellulaire pour répondre aux besoins énergétiques des activités. Cela entraîne la production d'un plus grand nombre d'ions hydrogène, entraînant une chute du pH sanguin. Lorsque le corps se repose, les niveaux d'oxygène sont plus élevés, les niveaux de dioxyde de carbone sont plus bas, plus d'hydrogène est lié et le pH augmente.
Les chimiorécepteurs réagissent à l'augmentation du niveau de dioxyde de carbone et d'ions hydrogène (baisse du pH) en stimulant les centres cardio-accélateurs et vasomoteurs, en augmentant le débit cardiaque et en contractant les vaisseaux périphériques. Les centres cardio-inhibiteurs sont supprimés. Avec la baisse des niveaux de dioxyde de carbone et d'ions hydrogène (augmentation du pH), les centres cardio-inhibiteurs sont stimulés, les centres cardio-accélérateurs et vasomoteurs sont supprimés, ce qui diminue le débit cardiaque et provoque une vasodilatation périphérique. Afin de maintenir un approvisionnement adéquat en oxygène dans les cellules et d'éliminer les déchets, tels que le dioxyde de carbone, il est essentiel que le système respiratoire réponde aux nouvelles demandes métaboliques. À son tour, le système cardiovasculaire transportera ces gaz vers les poumons pour les échanger, toujours selon les besoins métaboliques. Cette corrélation entre le contrôle cardiovasculaire et respiratoire ne saurait être trop soulignée.
D'autres mécanismes neuronaux peuvent également avoir un impact significatif sur la fonction cardiovasculaire. Celles-ci incluent le système limbique qui relie les réponses physiologiques à des stimuli psychologiques, ainsi que la stimulation généralisée sympathique et parasympathique.
Régulation endocrinienne
Le contrôle endocrinien du système cardiovasculaire implique les catécholamines, l'épinéphrine et la noradrénaline, ainsi que plusieurs hormones qui interagissent avec les reins lors de la régulation du volume sanguin.
Les catécholamines épinéphrine et noradrénaline sont libérées par la médullosurrénale. Elles améliorent et étendent la réponse sympathique ou "combat ou fuite" du corps. Ils augmentent la fréquence cardiaque et la force de contraction, tout en contractant temporairement les vaisseaux sanguins vers des organes qui ne sont pas indispensables aux réponses de fuite ou de combat et en redirigeant le flux sanguin vers le foie, les muscles et le coeur.
L'hormone antidiurétique (ADH), également appelée vasopressine, est sécrétée par les cellules de l'hypothalamus et transportée par les voies hypothalamo-hypophysaire vers l'hypophyse postérieure où elle est stockée jusqu'à sa libération par stimulation nerveuse. Le principal déclencheur incitant l'hypothalamus à libérer l'ADH est l'augmentation de l'osmolarité du liquide tissulaire, généralement en réponse à une perte importante du volume sanguin. ADH signale à ses cellules cibles dans les reins de réabsorber plus d'eau, évitant ainsi la perte de liquide dans l'urine. Cela augmentera les niveaux globaux de liquide et aidera à rétablir le volume sanguin et la pression sanguine. De plus, ADH limite les vaisseaux périphériques.
Le mécanisme rénine-angiotensine-aldostérone a un effet majeur sur le système cardiovasculaire. La rénine est une enzyme, bien que certaines sources l'identifient comme une hormone en raison de son importance dans la voie rénine-angiotensine-aldostérone. Les cellules spécialisées des reins présentes dans l'appareil juxta-glomérulaire répondent à une diminution du flux sanguin en sécrétant de la rénine dans le sang. La rénine convertit l'angiotensinogène, une protéine plasmatique produite par le foie, en sa forme active, l'angiotensine I. L'angiotensine I circule dans le sang et est ensuite convertie en angiotensine II dans les poumons. Cette réaction est catalysée par l'enzyme enzyme de conversion de l'angiotensine (ACE).
L'angiotensine II est un puissant vasoconstricteur qui augmente considérablement la tension artérielle. Il stimule également la libération d'ADH et d'aldostérone, une hormone produite par le cortex surrénalien. L'aldostérone augmente la réabsorption du sodium dans le sang par les reins. Puisque l'eau suit le sodium, cela augmente la réabsorption d'eau. Cela à son tour augmente le volume sanguin, augmentant la pression artérielle. L'angiotensine II stimule également le centre de la soif dans l'hypothalamus, de sorte qu'un individu consommera probablement plus de liquides, ce qui augmentera encore le volume sanguin et la pression sanguine.
L'érythropoïétine (EPO) est libérée par les reins lorsque le débit sanguin et / ou les niveaux d'oxygène diminuent. L'EPO stimule la production d'érythrocytes dans la moelle osseuse. Les érythrocytes sont le principal élément formé du sang et peuvent contribuer pour 40 % ou plus au volume sanguin, facteur important de viscosité, de résistance, de pression et de débit. En outre, l'EPO est un vasoconstricteur. La surproduction d'EPO ou l'absorption excessive d'EPO synthétique, souvent pour améliorer les performances sportives, augmentera la viscosité, la résistance et la pression, et réduira le débit en plus de sa contribution en tant que vasoconstricteur.
Sécrétée par des cellules situées dans les oreillettes du coeur, l'hormone natriurétique auriculaire (ANH) (également appelée peptide natriurétique auriculaire) est sécrétée lorsque le volume sanguin est suffisamment élevé pour provoquer un étirement extrême des cellules cardiaques. Les cellules du ventricule produisent une hormone ayant des effets similaires, appelée hormone natriurétique de type B. Les hormones natriurétiques sont des antagonistes de l'angiotensine II. Ils favorisent la perte de sodium et d'eau par les reins et inhibent la production et la libération de rénine, d'aldostérone et d'ADH. Toutes ces actions favorisent la perte de liquide dans le corps, entraînant une chute du volume et de la pression sanguine.
Autorégulation de la perfusion
Comme son nom l'indique, les mécanismes d'autorégulation ne nécessitent ni stimulation nerveuse spécialisée ni contrôle endocrinien. Il s'agit plutôt de mécanismes locaux d'autorégulation qui permettent à chaque région de tissu d'ajuster son débit sanguin - et donc sa perfusion. Ces mécanismes locaux incluent des signaux chimiques et des contrôles myogéniques.
Les signaux chimiques agissent au niveau des sphincters précapillaires pour déclencher une constriction ou une relaxation. Comme vous le savez, l'ouverture d'un sphincter précapillaire permet au sang de s'écouler dans ce capillaire particulier, alors que la contraction d'un sphincter précapillaire interrompt temporairement le flux sanguin vers cette région. Les facteurs impliqués dans la régulation des sphincters précapillaires sont les suivants :
- L'ouverture du sphincter est déclenchée en réponse à une diminution des concentrations en oxygène; augmentation des concentrations de dioxyde de carbone; des niveaux croissants d'acide lactique ou d'autres sous-produits du métabolisme cellulaire; concentrations croissantes d'ions potassium ou d'ions hydrogène (baisse du pH); des produits chimiques inflammatoires tels que les histamines; et augmentation de la température corporelle. Ces conditions stimulent à leur tour la libération de NO, un puissant vasodilatateur, des cellules endothéliales.
- La contraction du sphincter précapillaire est déclenchée par les niveaux opposés des régulateurs, qui déclenchent la libération d'endothélines, de puissants peptides vasoconstricteurs sécrétés par les cellules endothéliales. Les sécrétions plaquettaires et certaines prostaglandines peuvent également entraîner une constriction.
Encore une fois, ces facteurs modifient la perfusion tissulaire via leurs effets sur le mécanisme du sphincter précapillaire, qui régule le flux sanguin vers les capillaires. Étant donné que la quantité de sang est limitée, tous les capillaires ne peuvent pas se remplir en même temps. Le débit sanguin est donc attribué en fonction des besoins et de l'état métabolique des tissus, comme l'indiquent ces paramètres. Gardez toutefois à l'esprit que la dilatation et la constriction des artérioles alimentant les lits capillaires constituent le principal mécanisme de contrôle.
Réponse myogénique
La réponse myogénique est une réaction à l'étirement du muscle lisse dans les parois des artérioles lorsque le flux sanguin se modifie dans le vaisseau. Cela peut être considéré comme une fonction largement protectrice contre les fluctuations dramatiques de la pression artérielle et du débit sanguin afin de maintenir l'homéostasie. Si la perfusion d'un organe est trop faible (ischémie), le tissu subira de faibles niveaux d'oxygène (hypoxie). En revanche, une perfusion excessive pourrait endommager les vaisseaux plus petits et plus fragiles de l'organe. La réponse myogénique est un processus localisé qui sert à stabiliser le flux sanguin dans le réseau capillaire qui suit cette artériole.
Lorsque le flux sanguin est faible, le muscle lisse du vaisseau ne sera que très peu étiré. En réponse, il se détend, permettant au vaisseau de se dilater et augmentant ainsi le mouvement du sang dans les tissus. Lorsque le flux sanguin est trop élevé, le muscle lisse se contracte en réponse à l'étirement accru, provoquant une vasoconstriction qui réduit le flux sanguin.
Effet de l'exercice sur l'homéostasie vasculaire
Le coeur est un muscle et, comme tout muscle, il réagit de façon spectaculaire à l'exercice. Pour un jeune adulte en bonne santé, le débit cardiaque (fréquence cardiaque × volume systolique) augmente chez le non-athlète d'environ 5,0 litres (5,25 litres) par minute à un maximum d'environ 20 litres (21 litres) par minute. Cela s'accompagnera d'une augmentation de la pression artérielle d'environ 120/80 à 185/75. Cependant, des athlètes aérobiques bien entraînés peuvent augmenter considérablement ces valeurs. Pour ces personnes, le débit cardiaque augmente d'environ 5,3 litres (5,57 litres) par minute au repos à plus de 30 litres (31,5 litres) par minute au cours de l'exercice. Parallèlement à cette augmentation du débit cardiaque, la pression artérielle augmente de 120/80 au repos à 200/90 aux valeurs maximales.
En plus d'améliorer la fonction cardiaque, l'exercice augmente la taille et la masse du coeur. Le poids moyen du coeur du non-athlète est d'environ 300 g, alors qu'il augmentera à 500 g chez un athlète. Cette augmentation de la taille rend généralement le coeur plus fort et plus efficace pour pomper le sang, augmentant à la fois le volume systolique et le débit cardiaque.
La perfusion tissulaire augmente également au fur et à mesure que le corps passe d'un état de repos à un exercice léger et éventuellement à un exercice intensif (voir Figure 4). Ces modifications entraînent une vasodilatation sélective des muscles squelettiques, du coeur, des poumons, du foie et du tégument. Simultanément, une vasoconstriction intervient dans les vaisseaux menant aux reins et à la plupart des organes digestifs et reproducteurs. Le flux de sang vers le cerveau reste en grande partie inchangé, qu'il soit au repos ou en exercice, car les vaisseaux cérébraux dans le cerveau ne répondent généralement pas aux stimuli régulateurs, dans la plupart des cas, faute de récepteurs appropriés.
La vasodilatation intervenant dans certains vaisseaux, la résistance diminue et de plus en plus de sang se précipite dans les organes fournis. Ce sang finit par retourner dans le système veineux. Le retour veineux est encore amélioré par le muscle squelettique et les pompes respiratoires. À mesure que le sang retourne plus rapidement dans le coeur, la précharge augmente et le principe de Frank-Starling nous dit que la contraction du muscle cardiaque dans les oreillettes et les ventricules sera plus forte. Finalement, même les athlètes les mieux entraînés se fatigueront et devront prendre une période de repos après l'exercice. Le débit cardiaque et la distribution du sang reviennent ensuite à la normale.
L'exercice régulier favorise la santé cardiovasculaire de différentes façons. Parce que le coeur d'un athlète est plus gros que celui d'un non-athlète, le volume systolique augmente. Le coeur athlétique peut ainsi délivrer la même quantité de sang que le coeur non athlétique, mais avec une fréquence cardiaque inférieure. Cette efficacité accrue permet à l'athlète de faire de l'exercice pendant de plus longues périodes avant que ses muscles ne se fatiguent et de stresser moins le coeur. L'exercice réduit également le taux de cholestérol global en éliminant de la circulation une forme complexe de cholestérol, de triglycérides et de protéines connues sous le nom de lipoprotéines de basse densité (LDL), qui sont largement associées à un risque accru de maladie cardiovasculaire. Bien qu'il n'existe aucun moyen d'éliminer les dépôts de plaque des parois des artères autre qu'une intervention chirurgicale spécialisée, l'exercice favorise la santé des vaisseaux en diminuant le taux de formation de plaque et en réduisant la pression artérielle; le coeur n'a donc pas à générer autant de force pour vaincre la résistance.
En règle générale, 30 minutes d'exercice non continu au cours de la journée ont des effets bénéfiques et il a été prouvé que le taux de crises cardiaques était réduit de près de 50 %. Bien qu'il soit toujours conseillé de suivre un régime alimentaire sain, d'arrêter de fumer et de perdre du poids, des études ont clairement montré que les personnes en forme et en surpoids peuvent en réalité être en meilleure santé que les personnes minces sédentaires. Ainsi, les avantages d'un exercice modéré sont indéniables.
Hypertension et hypotension
Tout trouble affectant le volume sanguin, le tonus vasculaire ou tout autre aspect du fonctionnement vasculaire est également susceptible d'affecter l'homéostasie vasculaire. Cela inclut l'hypertension, l'hémorragie et le choc.
La pression artérielle chronique élevée est connue cliniquement comme hypertension. Elle est définie comme une pression artérielle chronique et persistante de 140/90 mm Hg ou plus. Les pressions comprises entre 120/80 et 140/90 mm Hg sont définies comme préhypertension. Environ 68 millions d'Américains souffrent actuellement d'hypertension. Malheureusement, l'hypertension est typiquement un trouble silencieux; par conséquent, les patients hypertendus peuvent ne pas reconnaître la gravité de leur maladie et ne pas suivre leur plan de traitement. Le résultat est souvent une crise cardiaque ou un accident vasculaire cérébral. L'hypertension peut également entraîner un anévrisme (gonflement d'un vaisseau sanguin par affaiblissement de la paroi), une maladie artérielle périphérique (obstruction de vaisseaux dans les régions périphériques du corps), une maladie rénale chronique ou une insuffisance cardiaque.
Hémorragie
La perte de sang mineure est gérée par l'hémostase et la réparation. L'hémorragie est une perte de sang qui ne peut pas être contrôlée par des mécanismes hémostatiques. Initialement, le corps répond aux hémorragies en initiant des mécanismes visant à augmenter la pression artérielle et à maintenir le débit sanguin. En fin de compte, cependant, le volume sanguin devra être rétabli, soit par des processus physiologiques, soit par une intervention médicale.
En réponse à la perte de sang, les stimuli des barorécepteurs amènent les centres cardiovasculaires à stimuler les réponses sympathiques pour augmenter le débit cardiaque et la vasoconstriction. Cela entraîne généralement une augmentation du rythme cardiaque d'environ 180 à 200 contractions par minute, ce qui ramène le débit cardiaque à un niveau normal. La vasoconstriction des artérioles augmente la résistance vasculaire, alors que la constriction des veines augmente le retour veineux au coeur. Ces deux étapes aideront à augmenter la pression artérielle. La stimulation sympathique déclenche également la libération d'épinéphrine et de noradrénaline, ce qui améliore à la fois le débit cardiaque et la vasoconstriction. Si les pertes sanguines représentaient moins de 20 % du volume sanguin total, ces réponses ramèneraient généralement la pression artérielle à la normale et redirigeraient le sang restant vers les tissus.
Une atteinte endocrinienne supplémentaire est toutefois nécessaire pour rétablir le volume sanguin perdu. Le mécanisme angiotensine-rénine-aldostérone stimule le centre de la soif dans l'hypothalamus, ce qui augmente la consommation de liquide pour aider à rétablir le sang perdu. Plus important encore, il augmente la réabsorption rénale de sodium et d'eau, réduisant ainsi la perte d'eau dans le débit urinaire. Les reins augmentent également la production d'EPO, stimulant ainsi la formation d'érythrocytes qui non seulement délivrent de l'oxygène aux tissus mais augmentent également le volume sanguin global.
Choc circulatoire
La perte de trop de sang peut entraîner un choc circulatoire, une maladie potentiellement mortelle dans laquelle le système circulatoire est incapable de maintenir le flux sanguin pour fournir suffisamment d'oxygène et d'autres nutriments aux tissus pour maintenir le métabolisme cellulaire. Il ne faut pas le confondre avec un choc émotionnel ou psychologique. En règle générale, le patient en état de choc circulatoire présentera une augmentation de la fréquence cardiaque mais une pression artérielle réduite, mais il existe des cas dans lesquels la pression artérielle restera normale. La production d'urine va chuter de manière spectaculaire et le patient peut sembler confus ou perdre conscience. Un débit urinaire inférieur à 1 mL / kg de poids corporel / heure est préoccupant. Malheureusement, le choc est un exemple de boucle à rétroaction positive qui, si elle n'est pas corrigée, peut entraîner la mort du patient.
Il existe plusieurs formes de choc reconnues :
- Le choc hypovolémique chez l'adulte est généralement provoqué par une hémorragie, bien qu'il puisse être provoqué chez l'enfant par des pertes de liquide dues à des vomissements graves ou à une diarrhée. Les autres causes de choc hypovolémique comprennent les brûlures étendues, l'exposition à certaines toxines et les pertes urinaires excessives liées au diabète insipide ou à l'acidocétose. En règle générale, les patients présentent une fréquence cardiaque rapide, presque tachycardique; un pouls faible souvent décrit comme un "fil"; une peau froide et moite, en particulier aux extrémités, en raison d'un débit sanguin périphérique restreint; respiration rapide et superficielle; hypothermie; la soif; et bouche sèche. Les traitements consistent généralement à administrer des liquides par voie intraveineuse pour rétablir le fonctionnement normal du patient, ainsi que divers médicaments tels que la dopamine, l'épinéphrine et la noradrénaline pour augmenter la pression artérielle.
- Le choc cardiogénique résulte de l'incapacité du coeur à maintenir le débit cardiaque. Le plus souvent, il s'agit d'un infarctus du myocarde (crise cardiaque), mais il peut aussi s'agir d'arythmie, de désordres valvulaires, de cardiomyopathies, d'insuffisance cardiaque ou simplement d'un débit sanguin insuffisant dans les vaisseaux cardiaques. Le traitement consiste à réparer les dommages causés au coeur ou à ses vaisseaux afin de résoudre la cause sous-jacente, plutôt que de traiter directement le choc cardiogénique.
- Un choc vasculaire survient lorsque les artérioles perdent leur tonus musculaire normal et se dilatent considérablement.Elle peut provenir de diverses causes et les traitements impliquent presque toujours un remplacement du liquide et des médicaments, appelés agents inotropes ou agents presseurs, qui redonnent le tonus aux muscles des vaisseaux. En outre, il est nécessaire d'éliminer ou au moins d'atténuer la cause sous-jacente de la maladie. Cela peut inclure des antibiotiques et des antihistaminiques, ou certains stéroïdes, qui peuvent aider à réparer les lésions nerveuses. Une cause commune est la septicémie (ou septicémie), également appelée "intoxication par le sang", qui est une infection bactérienne répandue qui entraîne une réaction inflammatoire au niveau de l'organisme, appelée choc septique. Choc neurogèneest une forme de choc vasculaire qui survient lors de lésions crâniennes ou rachidiennes et qui endommagent les centres cardiovasculaires de la moelle épinière ou les fibres nerveuses provenant de cette région. Le choc anaphylactique est une réaction allergique grave qui provoque la libération généralisée d'histamines, provoquant une vasodilatation dans tout le corps.
- Le choc obstructif, comme son nom l'indique, survient lorsqu'une partie importante du système vasculaire est obstruée. Il n'est pas toujours reconnu comme une affection distincte et peut être associé à un choc cardiogénique, y compris une embolie pulmonaire et une tamponnade cardiaque. Les traitements dépendent de la cause sous-jacente et, en plus de l'administration intraveineuse de liquides, comprennent souvent l'administration d'anticoagulants, l'élimination du liquide de la cavité péricardique ou de l'air de la cavité thoracique et une intervention chirurgicale requise. La cause la plus fréquente est une embolie pulmonaire, un caillot qui se loge dans les vaisseaux pulmonaires et interrompt le flux sanguin. Les autres causes comprennent la sténose de la valve aortique; tamponnade cardiaque, dans laquelle l'excès de liquide dans la cavité péricardique nuit à la capacité du coeur à se détendre complètement et à se remplir de sang (entraînant une diminution de la précharge);et un pneumothorax dans lequel une quantité excessive d'air est présente dans la cavité thoracique, à l'extérieur des poumons, ce qui nuit au retour veineux, à la fonction pulmonaire et à l'apport d'oxygène aux tissus.
En rapport avec "homéostasie vasculaire"

L'appareil cardiovasculaire (système circulatoire) se compose du coeur, qui est un organe de pompage musculaire, et d'un système fermé pour la circulation...
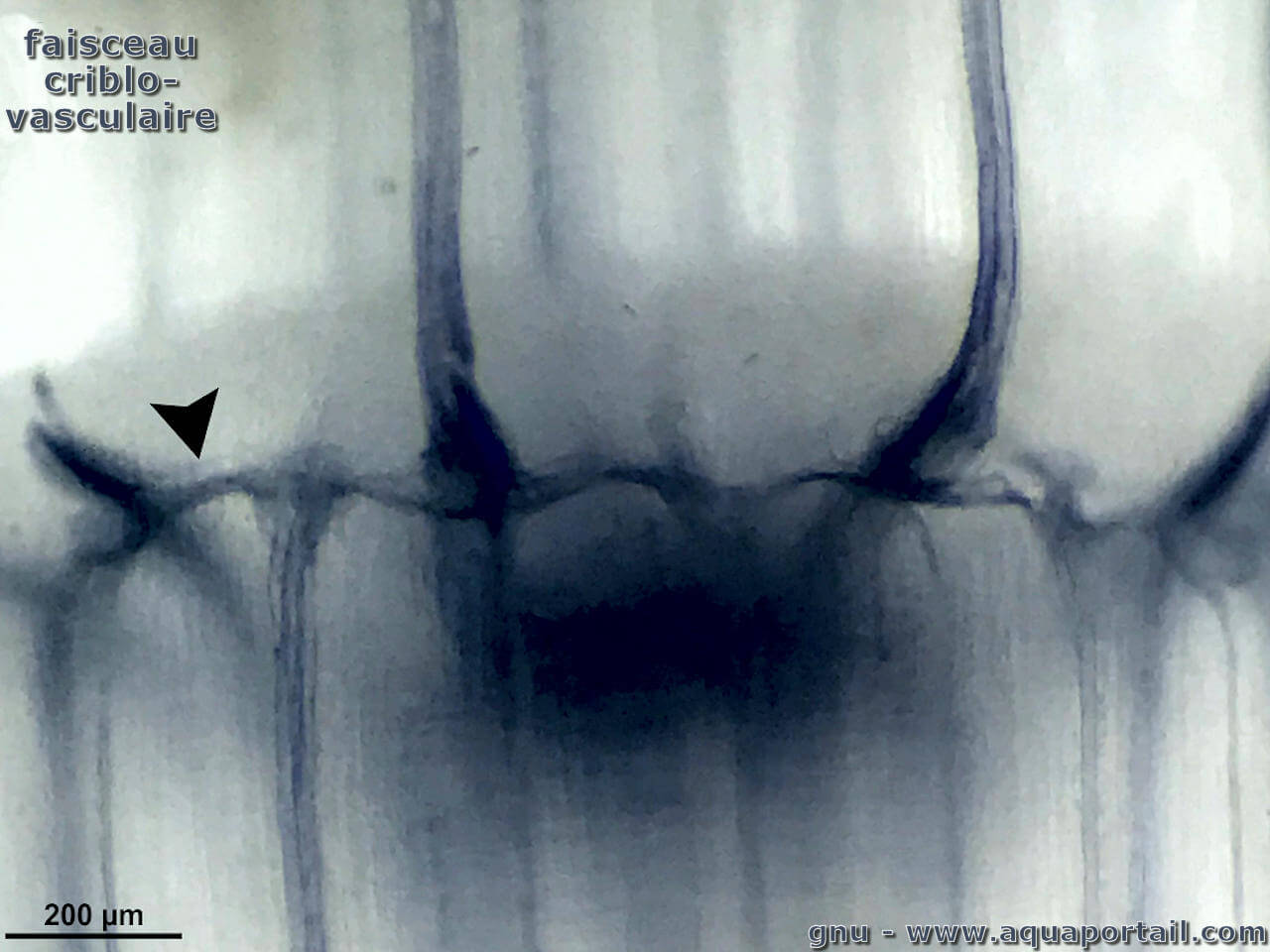
En botanique, un faisceau vasculaire est chaque faisceau, chacun des cordons individuels qui forment le système vasculaire primaire des plantes.
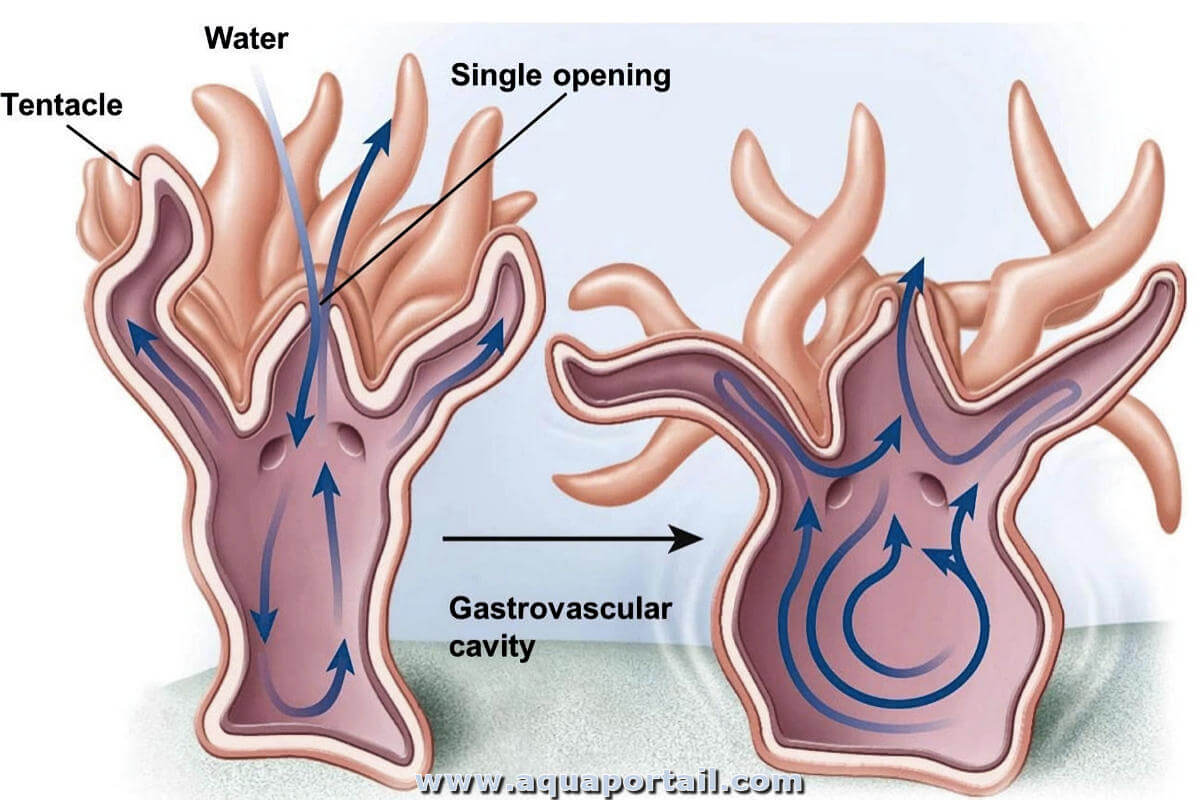
Ce qui est gastro-vasculaire (gastrovasculaire) est en rapport avec le système gastrique et la vascularisation, fonctionnant à la fois dans la digestion...

L'homéostasie est un processus d'autorégulation par lequel un organisme tend à maintenir sa stabilité tout en s'adaptant aux conditions optimales pour...
