Histidine
Définition
L'histidine (His) est l'un des 22 acides aminés constitutifs des protéines de la matière vivante. Sa décarboxylation donne de l'histamine et sa dégradation de l'acide, l'acide glutamique. Les codons correspondants sont CAU et CAC. Son groupe fonctionnel est un imidazole chargé positivement.
Structure de l'histidine :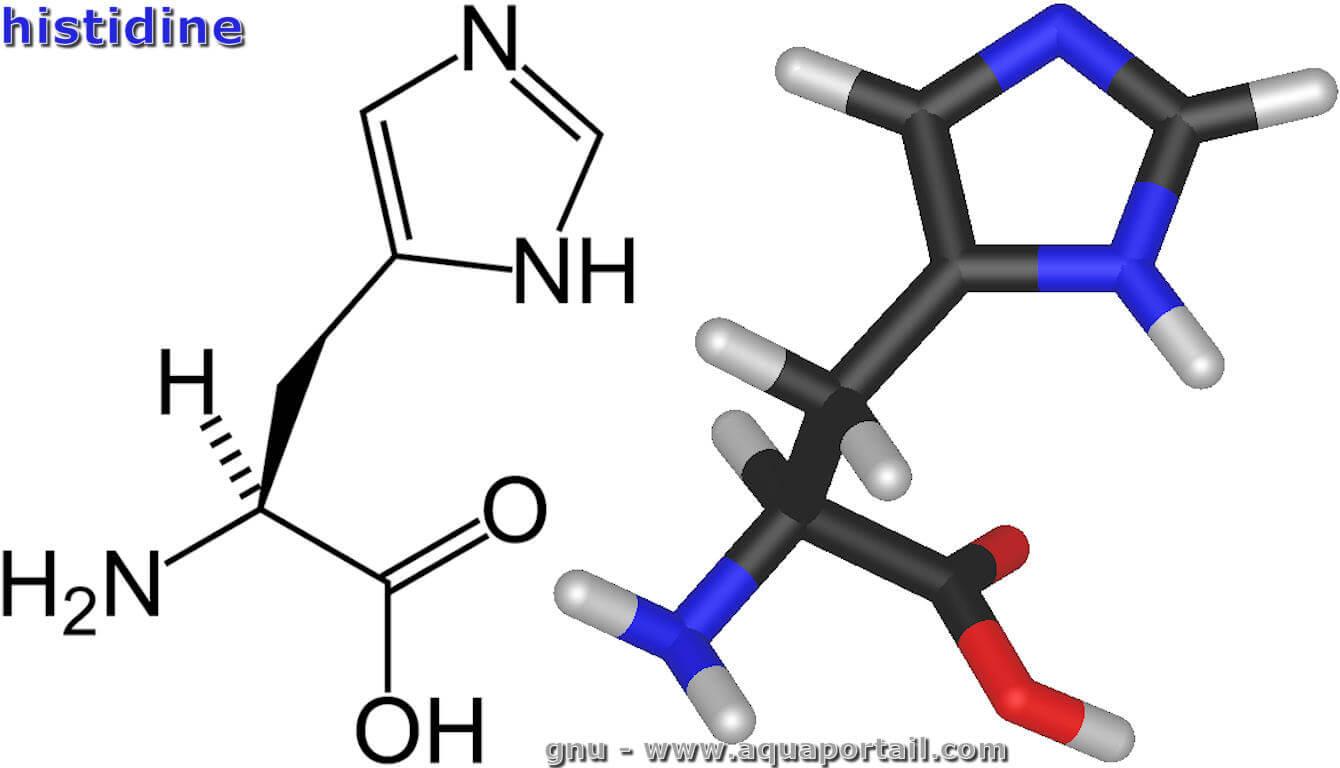
L'histidine est un composé chimique acide 2-amino-3- (1H-imidazol-5-yl) propanoïque, de formule moléculaire C6H9N3O2, de masse molaire 155,16 g/mol et avec un point de fusion à 560 K (287 °C). L'histidine a d'abord été purifié par Albrecht Kossel en 1896, en Allemagne.
Explications
L'histidine est un acide aminé essentiel chez les animaux, tandis que les bactéries, les champignons et les plantes peuvent la synthétiser en interne. Elle est l'un des 22 acides aminés essentiels.
La racémisation de l'histidine en L–acides aminés peut être utilisée pour la datation des acides aminés avec une détermination de l'âge pour le matériel osseux fossile.
Les produits laitiers, la viande, le poulet et le poisson contiennent de l'histidine. L'histidine est un précurseur de l'histamine dans lequel elle est transformée par décarboxylation. L'histamine est une substance libérée par les cellules du système immunitaire au cours d'une réaction allergique. Il participe également au développement et au maintien de tissus sains, en particulier de la myéline qui recouvre les neurones.
La pilocarpine est un alcaloïde dérivé de l'histidine présent dans le genre Pilocarpus chez les Rutacées. C'est un parasympathicomimétique.
Propriétés chimiques
L'histidine a un pKa de 6,5. Cela signifie que de petites variations du pH physiologique modifieront leur charge totale. En dessous d'un pH de 6, le noyau imidazole est principalement protoné, avec une charge positive. Le cycle imidazole est également un hydrocarbure aromatique.
Pendant la catalyse, l'azote de base de l'histidine est capable de capturer un proton de sérine, de thyronine et de cystéine, raison pour laquelle il fait partie du centre catalytique de certaines enzymes.
Sa chaîne latérale est chargée positivement (acide aminé basique) à des valeurs de pH physiologiques. Parmi les vingt acides alpha-aminés, seule l'histidine (avec un pkH = 6) s'ionise dans l'échelle de pH physiologique. À un pH de 6, son groupe latéral imidazole n'est chargé qu'à 50 %, ce qui rend l'histidine neutre à une extrémité basique du spectre du pH physiologique. Ce fait a pour conséquence que les chaînes latérales de l'histidine participent aux réactions catalytiques des enzymes.
En ce qui concerne son rôle dans la molécule d'hémoglobine, le cinquième ligand hémique Fe (II) est HisF8, l'histidine proximale (proche). Dans l'oxyhémoglobine, Fe (II) est placé à 0,22 Å en dehors du plan de l'hème du côté histidine proximal et, de plus, est coordonné par l'oxygène. L'histidine distale (distante) est liée par une liaison hydrogène à l'oxygène. Dans l'hémoglobine, la sixième position du ligand Fe (II) s'est déplacée vers un point situé à 0,55 Å en dehors du plan de l'hème.
Il est dégradé par l'alpha-cétoglutarate, bien que la conversion de l'histidine en glutamate soit plus compliquée que celle du reste des acides aminés dégradés par cette réaction. Il se désamine de manière non oxydante, puis il est hydraté et son cycle imizol est clivé pour former le N-formiminoglutamate. Ensuite, le groupe formimino (formimine) transfère le tétrahydropholate pour former de l'acide glutamique et du N5-formimino-tétrahydrofolate.
Le cycle imidazole de l'histidine est sujet à un tautomérisme, plus spécifiquement un tautomérisme imine-énamine.
Biosynthèse de l'histidine
Cinq des six atomes de l'histidine sont dérivés du 5-phosphoribosyl-alpha-pyrophosphate (PRPP), un intermédiaire également impliqué dans la biosynthèse du tryptophane, des nucléotides puriques et de la pyrimidine. Le sixième carbone de l'histidine provient de l'ATP. Les atomes d'ATP qui ne sont pas incorporés dans l'histidine sont éliminés sous forme de ribonucléotide 5-aminoimidazole-4-carboxamide, qui est également un intermédiaire dans la synthèse des purines.
La biosynthèse inhabituelle de l'histidine à partir d'une purine a été citée comme preuve à l'appui de l'hypothèse selon laquelle la vie à sa source était basée sur l'ARN. Les résidus d'histidine sont souvent des composants des centres actifs des enzymes, où ils agissent en tant que nucléophiles ou catalyseurs généraux acide-base, ou les deux. En conséquence, la découverte que l'ARN a des propriétés catalytiques suggère que le fragment imidazole des purines joue un rôle similaire dans ces enzymes à ARN (ribozymes). Cela suggère que la voie de la synthèse de l'histidine est une transition fossile vers un mode de vie plus efficace basé sur les protéines.
Caractéristiques et avantages
En retirant le groupe acide carboxylique de l'histidine, l'enzyme histidine décarboxylase le convertit en histamine, une substance physiologique importante librement présente dans l'intestin et dans les granules basophiles des cellules du système phagocytaire mononucléaire.
L'histamine est un vasodilatateur puissant, impliqué dans les réactions allergiques telles que l'urticaire et l'inflammation. L'histamine stimule également la sécrétion de pepsine et d'acide chlorhydrique par l'estomac.
L'histidine est élevée dans le plasma et le cerveau pendant les carences en protéines et également dans certaines conditions pathologiques, ce qui entraîne la possibilité d'effets directs sur les fonctions du système nerveux central.
Utilisations thérapeutiques de l'histidine
Cet acide aminé est vital pour notre corps car sa décarboxylation permet sa transformation en histamine, raison pour laquelle il est utilisé dans le traitement de la polyarthrite rhumatoïde (inflammation et manque de mobilité), des maladies allergiques, des ulcères et de l'anémie. En association avec l'hormone de croissance et d'autres acides aminés, il contribue à la réparation des tissus, en particulier dans le système cardiovasculaire. Dans le système nerveux central, il est synthétisé et libéré par les neurones et utilisé comme neuromodulateur.
En dehors du système nerveux est un médiateur de milieux physiologiques. Une carence en histidine peut causer des problèmes d'audition. Il est également connu que l'histidine aide à la détoxification des métaux lourds, au traitement de l'impuissance et de la frigidité, améliore la réponse immunitaire, aide à éviter les vomissements pendant la grossesse. Il est également important de maintenir les gaines de myéline entourant les axones neuronaux. Il est également nécessaire pour la production de globules rouges et blancs, protège le corps des dommages causés par les radiations et réduit la pression artérielle.
Synonymes, antonymes
Voir tous les synonymes pour "histidine".1 synonyme (sens proche) de "histidine" :
- pilocarpine
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à HISTIDINE sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
Le mot HISTIDINE est dans la page 2 des mots en H du lexique du dictionnaire.
Mots en H à proximité
hippopotame hippopotame pygmée hispide histamine histaminocyte histidinehistiocyte histochimie histochimique histogenèse histologie
En rapport avec "histidine"

Un acide aminé essentiel est un acide aminé indispensable qui ne peut pas être synthétisé et fabriqué par l'organisme.

L'acide glutamique est un acide aminé non essentiel présent dans les protéines végétales et animales.

Une histamine est une monoamine biogène résultant de la décarboxylation de l'histidine par une histidine décarboxylase.
Une actinidine est une pyridine dérivée, présente dans l'huile essentielle de valériane avec les racines de l'espèce officinale Valeriana officinalis...
