Catalase
Définition
Une catalase est une enzyme qui catalyse la décomposition du peroxyde d'hydrogène (H2O2) en eau et dioxygène. Du groupe des oxydoréductases, elle transforme le peroxyde d'hydrogène en eau et dioxygène selon la réaction de dismutation : 2 H2O2 = 2 H2O + O2.
Une catalase tétramère d'érythrocyte (humain) :
La catalase humaine est constituée de quatre sous-unités identiques de 60 kDa chacune. Chacun de ceux-ci contient un groupe hème et un site de liaison NADPH.
Explications
Une catalase est une chromoprotéine porphyrinique à hème ferrique présente dans les peroxysomes animaux et végétaux et dans les globules rouges. C'est un sous-produit de la dégradation des purines et de l'oxydation des acides gras et peut endommager le génome et les protéines.
La catalase a été la première enzyme antioxydante découverte. Les catalases sont présentes chez presque tous les êtres vivants aérobies, chez l'homme en particulier dans les peroxysomes du foie et des reins, et les érythrocytes. L'enzyme est sous la forme d'un homotétramère dans les peroxysomes.
Le peroxyde d'hydrogène est un résidu du métabolisme cellulaire de nombreux organismes vivants et a, entre autres, une fonction protectrice contre les micro-organismes pathogènes, principalement les anaérobies, mais compte tenu de sa toxicité, il doit rapidement se transformer en composés moins dangereux. Cette fonction est réalisée par cette enzyme qui catalyse sa décomposition dans l'eau et l'oxygène. En outre, la catalase est utilisée dans l'industrie textile pour l'élimination du peroxyde d'hydrogène et, dans une moindre mesure, elle est utilisée pour le nettoyage des lentilles de contact qui ont été stérilisées dans une solution de peroxyde d'hydrogène.
La catalase est une enzyme antioxydante commune avec le taux de renouvellement le plus élevé. Elle est présente dans les tissus vivants et est une enzyme clinique clé impliquée dans la dégradation du peroxyde d'hydrogène en eau et en oxygène moléculaire. Selon la structure et la séquence, les catalases peuvent être divisées en trois classes, à savoir la catalase monofonctionnelle ou catalase typique, la catalase-peroxydase et la pseudocatalase ou Mn-catalase.
La catalase a des sources endogènes et exogènes. Par exemple, on le trouve dans les érythrocytes et ses sources exogènes proviennent de plantes telles que le coton, le tournesol et la citrouille.
Biomarqueur
La catalase est un biomarqueur important du stress oxydatif et de la pathogenèse de nombreuses maladies et infections. Elle aide à prévenir l'apparition de maladies neurologiques et inflammatoires, la carcinogenèse et le syndrome métabolique. Il a également été rapporté qu'elle était utilisée comme thérapie pour le cancer, la rétinopathie diabétique et les patients cardiaques.
Action
Le mécanisme d'action de la catalase comporte deux étapes. Au cours de la réaction enzymatique conduisant à la dissociation de H2O2, la catalase est d'abord oxydée en un intermédiaire de fer hypervalent, connu sous le nom de composé I, qui est ensuite ramené à l'état de repos par une seconde molécule de H2O2.
Le mécanisme complet de la catalase n'est pas connu, quoique la réaction chimique se déroule en deux étapes :
- Dans la première étape, le peroxyde d'hydrogène est réduit et l'enzyme est oxydée pour produire l'eau du produit.
- Dans la seconde étape, le peroxyde d'hydrogène et l'enzyme sont tous deux réduits et oxydés en oxygène et ainsi libérés en tant que produit à côté d'une autre molécule d'eau.
Aux faibles concentrations de peroxyde d'hydrogène, la catalase oxydée peut oxyder le méthanol et l'éthanol en acide via l'aldéhyde.
Cette enzyme peut agir comme une peroxydase pour de nombreuses substances organiques, en particulier pour l'éthanol qui agit comme un donneur d'hydrogène. Les enzymes de nombreux micro-organismes, tels que Penicillium simplicissimum, qui présentent une activité de catalase et de peroxydase, sont fréquemment appelées catalases-peroxydases.
Isozymes
La catalase est située dans tous les principaux sites de production de H2O2 dans l'environnement cellulaire (tels que les peroxysomes, les mitochondries, le cytosol et le chloroplaste) des plantes supérieures. De multiples formes moléculaires d'isoenzymes de catalase indiquent son rôle polyvalent dans le système végétal. La modulation de H2O2 par les isozymes de la catalase dans des cellules ou des organites spécifiques à des moments et des phases de développement spécifiques interfère directement ou indirectement avec la transduction du signal chez les plantes.
Les isoenzymes catalase CAT-1, CAT-2, CAT-3 ont été respectivement codées par les gènes de structure Cat1, Cat2 et Cat3. L'expression du gène cat montre la spécificité du temps, de l'espèce et du stress.
Le déficit en catalase chez les plantes développe des anomalies telles que la chlorose et la stérilité de la tête et la sensibilité aux conditions photorespiratoires normales. La phylogénie moléculaire des protéines catalase végétales révèle également la structure et les liens fonctionnels entre un large éventail d'espèces végétales. Ce chapitre compile les dernières informations sur la structure, la localisation, la biochimie, les gènes et la fonction des catalases chez les plantes.
Utilisation industrielle
Les catalases (EC 1.11.1.6) sont des enzymes antioxydantes microbiennes utiles dans l'industrie qui catalysent la conversion du peroxyde d'hydrogène en eau et en oxygène moléculaire.
Actuellement, il existe au moins huit souches capables de produire des catalases : Penicillum variable, A. niger, S. cerevisiae, Staphylococcus, Micrococcus lysodeiktious, Thermoascus aurantiacus, Bacillus subtilis et rhizobium radiobacter. Les catalases sont utilisées dans plusieurs applications industrielles telles que la transformation des aliments ou du textile pour éliminer le peroxyde d'hydrogène utilisé pour la stérilisation ou le blanchiment.
Test microbiologique
En microbiologie, le test de catalase est utilisé pour la différenciation bactérienne. La différenciation des staphylocoques à catalase positive des streptocoques à catalase négative revêt une importance clinique particulière. Ici, une goutte de réactif catalase (3 % de solution de peroxyde d'hydrogène) est placé sur une lame et une boucle de matériel bactérien brièvement tenu. Réaction positive : bouillonnement direct, formation de cloques; Réaction négative : pas de bouillonnement ou retardé. Alternativement, le peroxyde d'hydrogène dilué peut être déposé directement sur une colonie bactérienne sur une plaque d'agar.
La plupart des bactéries aérobies et anaérobies facultatives, ainsi que les champignons, ont l'enzyme catalase, qui est capable de cliver le H2O2 toxique pour les cellules.
Expérimentalement, le peroxyde d'hydrogène est utilisé en biologie pour induire la mort cellulaire programmée des cellules eucaryotes isolées.
Absence congénitale
L'absence congénitale de catalase est la cause d'une acatalasémie (ou acatalasie), la maladie de Takahara qui se manifeste par l'absence d'activité catalase dans les globules rouges et par de graves infections gangréneuses de la bouche, pouvant entraîner une perte de dents et des destructions sévères des mâchoires et des régions molles qui les recouvrent.
Comme maladie congénitale, 2 sur 100 000 habitants souffrent de ce trouble au Japon. Effectivement, des mutations dans le gène CAT peuvent conduire à une déficience héréditaire en catalase, qui est plus fréquente au Japon.
Synonymes, antonymes
Voir tous les synonymes pour "catalase".2 synonymes (sens proche) de "catalase" :
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à CATALASE sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
Le mot CATALASE est dans la page 2 des mots en C du lexique du dictionnaire.
Mots en C à proximité
catabolisme des protéines catabolite cataclysme cataclysmique catadrome catalasecatalepsie catalyse catalyse hétérogène catalyse homogène catalyseur
En rapport avec "catalase"

La biocatalyse est le processus chimique par lequel des enzymes ou d'autres catalyseurs biologiques effectuent des réactions entre des composants organiques.
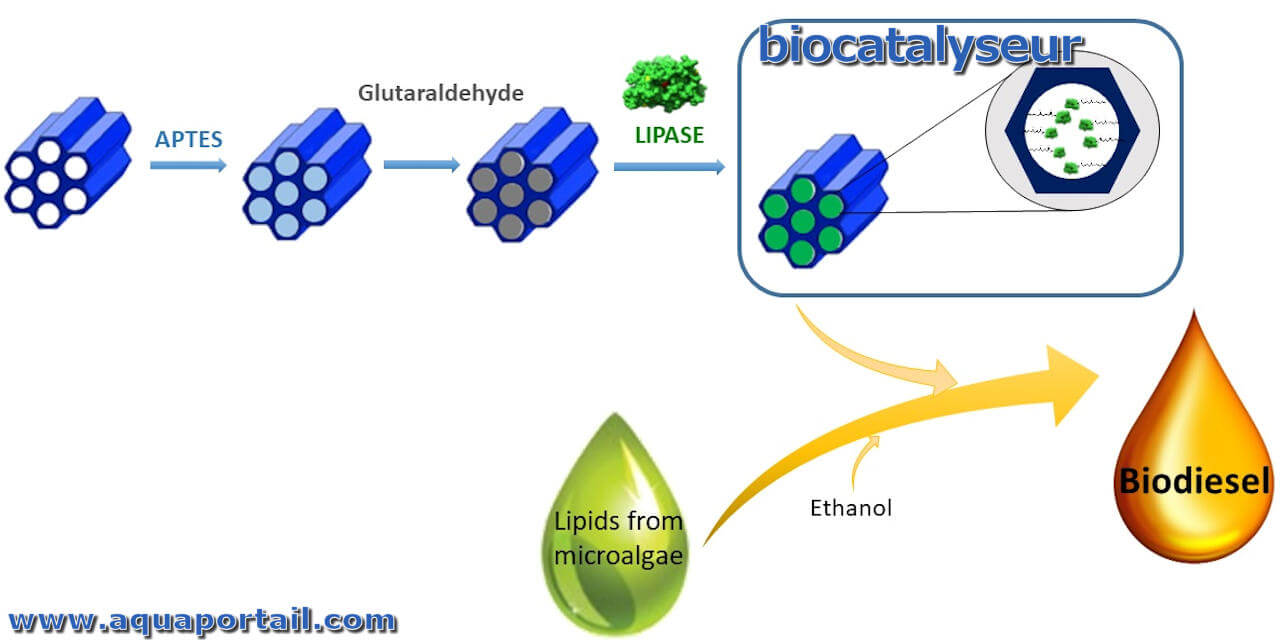
Un biocatalyseur est une macromolécule naturelle qui accélère une réaction biochimique. Les catalyseurs naturels (biologiques) sont, par exemples, les enzymes...
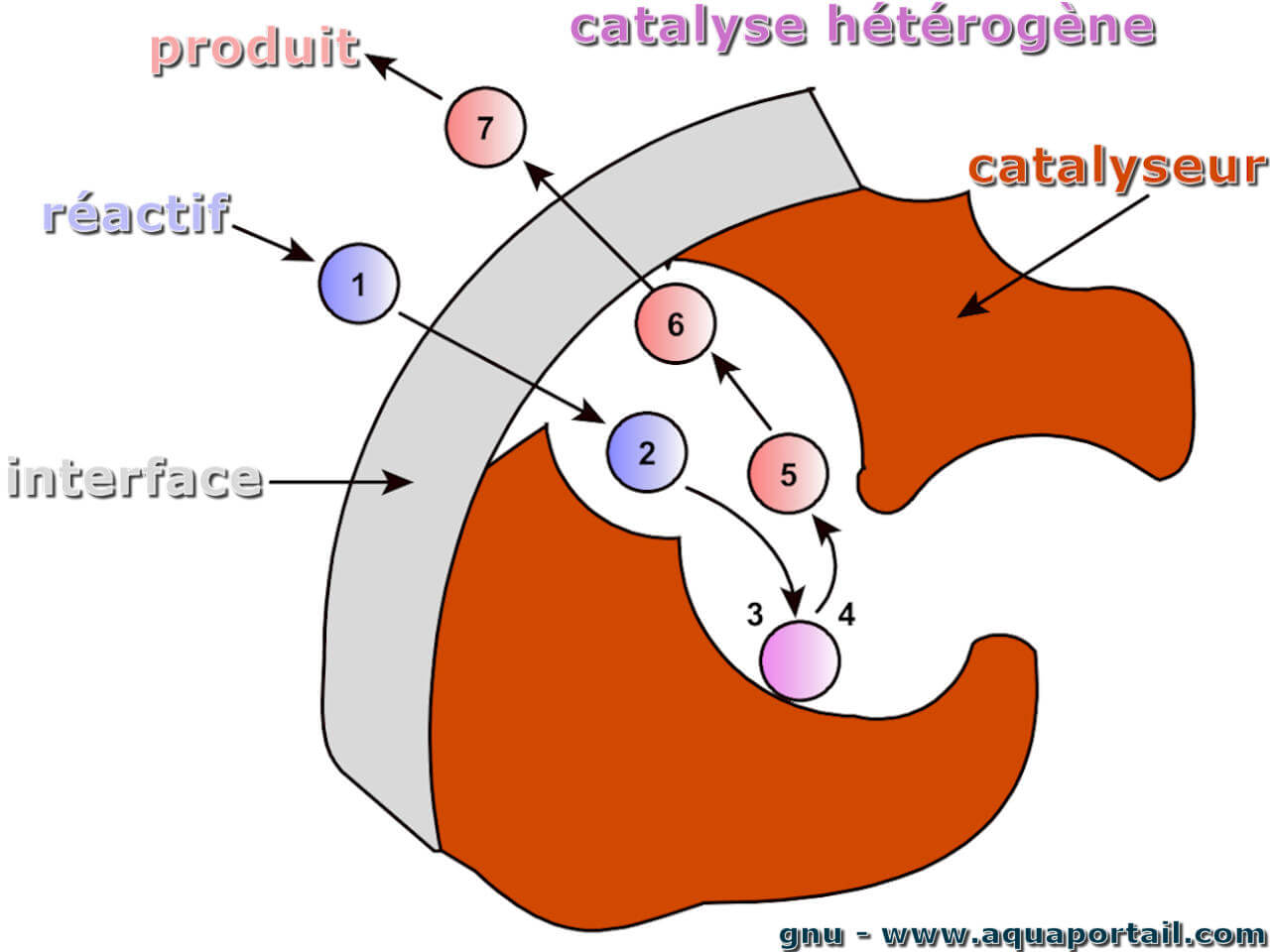
Une catalyse est un processus chimique qui consiste en l'accélération cinétique d'une réaction chimique grâce à une substance appelée catalyseur, qui ne subit...

La catalyse hétérogène est une catalyse dans laquelle le catalyseur et les réactifs d'une réaction chimique sont présents en différentes phases (gazeuse...
