Protéine globulaire
Définition
Une protéine globulaire, ou une sphéroprotéine, est une forme sphérique de protéine avec une structure plus complexe, qui diffère fondamentalement d'une protéine fibreuse. Une globulaire est plus ou moins soluble dans les solutions aqueuses où les globulaires forment des suspensions colloïdales, les fibreuses étant pratiquement insolubles.
L'hémoglobine est une protéine globulaire :
La structure tridimensionnelle de l'hémoglobine montre une protéine globulaire, un oligomère de type tétramère.
Explications
Les protéines globulaires, avec une structure tertiaire ou quaternaire plus ou moins sphérique, sont l'un des deux principaux types de protéines, avec les protéines fibreuses.
Structure globale et solubilité
L'expression protéine globulaire est assez ancienne (datant probablement du 19ème siècle) et est devenue quelque peu archaïque compte tenu des centaines de milliers de protéines et de l'existence d'un vocabulaire descriptif de motifs structurels plus élégants et descriptifs. La nature globulaire de ces protéines ne peut être déterminée sans le recours aux techniques modernes, utilisant uniquement des ultracentrifugeuses ou des techniques de diffusion dynamique de la lumière.
La structure tertiaire de la protéine induit sa sphéricité. Les groupes apolaires (queues hydrophobes) sont regroupés à l'intérieur de la molécule, tandis que les polaires (têtes hydrophiles) sont disposés à l'extérieur, permettant l'attrait des dipôles-dipôles avec le solvant, ce qui explique la solubilité de la molécule.
Leurs chaînes latérales non polaires font saillie à l'intérieur de la molécule, tandis que les chaînes polaires font saillie vers l'extérieur, conduisant ainsi à la solubilité dans l'eau. Ce terme obsolète remonte au 19ème siècle et a été remplacé par la classification des protéines en domaines protéiques.
Plus en détails, la séquence d'acides aminés des protéines de ce type induit l'enroulement de la protéine, générant une structure très compacte. La forme générée après le repliement est directement responsable de l'activité de la protéine elle-même selon le dogme "structure-fonction". La forme globulaire est déterminée par la structure tertiaire de ces polypeptides, qui dispose des résidus d'acides aminés hydrophiles sur la surface externe de la protéine, enfermant les résidus apolaires dans le noyau dit hydrophobe.
Les protéines globulaires peuvent avoir une structure tertiaire très complexe, caractérisée par de nombreux domaines disposés dans l'espace. La séquence primaire d'une chaîne polypeptidique peut assumer un très grand nombre de conformations, mais toutes les protéines globulaires limitent le nombre de leurs conformations à un ou quelques (paradoxe de Levinthal). Selon le dogme d'Anfinsen, en fait, les protéines sont capables d'atteindre de manière autonome le bon état conformationnel (qui coïncide avec un minimum d'énergie libre) en vertu exclusive de sa séquence d'acides aminés, tout au plus avec l'intervention de la chaperonine. Les mécanismes sous-jacents au repliement correct des protéines ne sont pas encore clairs, mais de faibles interactions entre les acides aminés sont impliquées, telles que les liaisons hydrogène et les interactions de van der Waals.
Pendant le repliement, toutefois, l'énergie libérée est très modeste, car le repliement implique une diminution nette de l'entropie de la protéine. Ce fait se traduit par une certaine instabilité de la structure tertiaire, facilement modifiable par les altérations de l'environnement (températures élevées, variations de salinité ou de pH) et explique le renouvellement relativement rapide de ce type de protéine.
Différents rôles dans le corps
Contrairement aux protéines fibreuses qui ne remplissent que des fonctions structurelles, les protéines globulaires peuvent également agir comme :
- enzymes : catalyseurs de réactions organiques se déroulant dans le corps dans des conditions normales et avec une grande spécificité. Par exemple, les estérases jouent ce rôle.
- Messagers : transmettant des messages pour réguler les processus biologiques. Un exemple serait l'hormone insuline.
- transporteurs d'autres molécules à travers la membrane cellulaire, comme les hémoglobines qui transportent l'oxygène.
- Stockage des acides aminés : les acides aminés sont hydrophiles ce qui leur permet d'être solubles dans l'eau.
- Les protéines régulent généralement davantage les fonctions régulatrices que les protéines fibreuses.
- Les protéines chélatantes (de chélation) ou stockantes (de stockage); par exemple, la ferritine, qui joue le rôle de réserve de fer;
- Les protéines structurelles, par exemple l'actine et la tubuline, qui sont globulaires et solubles en tant que monomères, mais polymérisent pour former des fibres rigides et longues, soumises à un renouvellement rapide.
Exemples
Parmi les protéines globulaires les plus connues, l'hémoglobine est un membre de la famille des globulines. Les autres protéines globulaires sont les immunoglobulines (IgA, IgD, IgE, IgG et IgM) et les alphaglobulines, bêtaglobulines et gammaglobulines.
Presque toutes les enzymes jouant un rôle important dans le métabolisme sont globulaires, ainsi que les protéines impliquées dans la transduction du signal dans la cellule (membrane cellulaire).
Le groupe des protéines globulaires comprend :
- les globines;
- les histones et les protamines;
- les albumines;
- les globulines;
- les prolamines;
- les glutelines;
- les phytoglobulines (édestine, phaséoline, viciline, légumine, glycinine, arachine, amadine...).
Synonymes, antonymes
Voir tous les synonymes pour "protéine globulaire".1 synonyme (sens proche) de "protéine globulaire" :
- sphéroprotéine
1 antonyme (sens contraire) :
- protéine fibreuse
Les mots ou les expressions apparentés à PROTÉINE GLOBULAIRE sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
L'expression PROTEINE GLOBULAIRE est dans la page 9 des mots en P du lexique du dictionnaire.
Mots en P à proximité
protéine conjuguée protéine d'échafaudage protéine de transport protéine en hélice protéine G protéine globulaireprotéine kinase protéine membranaire protéine recombinante protéine transmembranaire protéine végétale
En rapport avec "protéine globulaire"

Une alphaglobuline est une globuline en circulation dans le plasma sanguin. Elle est caractérisée par sa mobilité électrique dans des solutions alcalines...

Une bêtaglobuline est une globuline en circulation dans le plasma sanguin qui se caractérise par une certaine mobilité électrique dans des solutions alcalines...
Une euglobuline appartient à une classe de globulines, des protéines simples, caractérisée en ce qu'elle est insoluble dans l'eau, y compris dans l'eau...
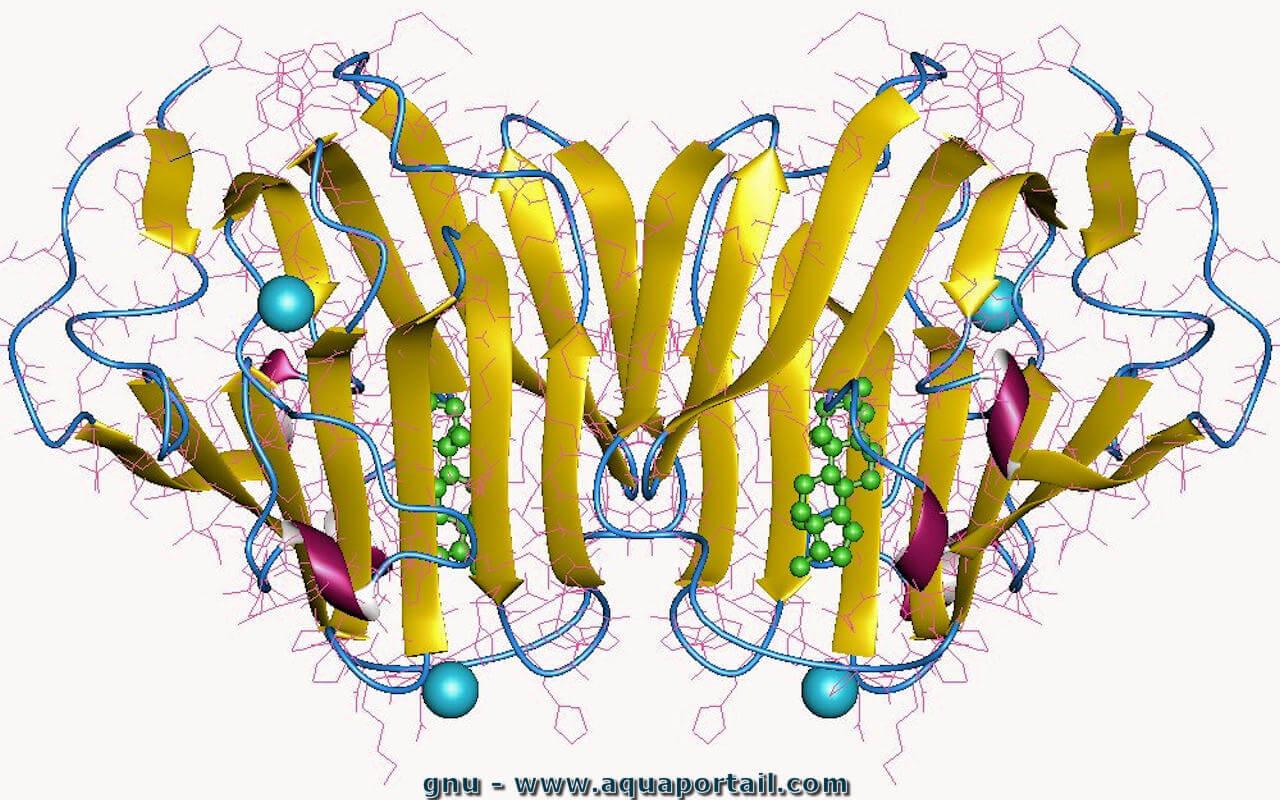
Une globuline est une protéine plasmatique qui comprend les anticorps. Les globulines sont des protéines hydrosolubles sériques, solubles dans des solutions...
