Statine
Définition
La statine est un acide aminé gamma qui apparaît deux fois dans la séquence de la pepstatine, un inhibiteur actif contre la pepsine et d'autres protéases acides. Elle est responsable de l'activité inhibitrice de la pepstatine car elle imite l'état de transition tétraédrique de la catalyse de la protéase. La sécrétion d'une hormone stimuline est inhibée par les statines et stimulée par les libérines hypothalamiques.
En milieu médical, les statines sont un groupe de médicaments qui peuvent aider à réduire le taux de cholestérol à lipoprotéines de basse densité (LDL) dans le sang.
Une molécule de statine :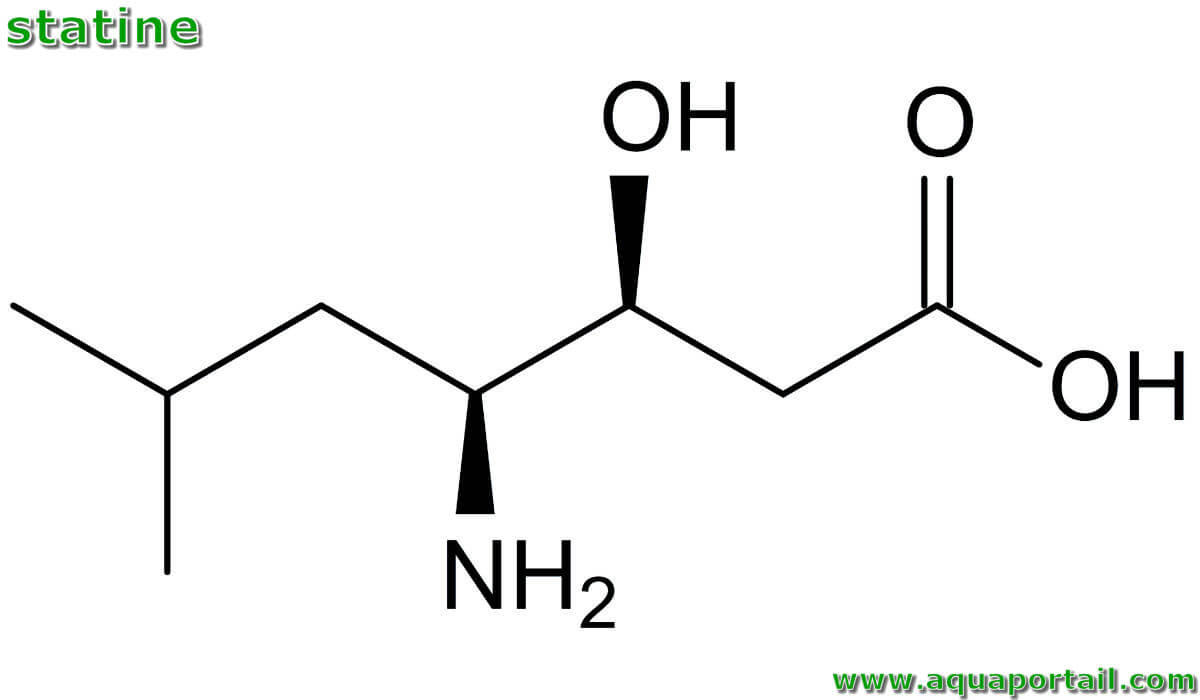
Le nom IUPAC de la statine est l'acide (3S, 4S)-4-amino-3-hydroxy-6-méthylheptanoïque. L'acide (3S, 4S)-4-amino-3-hydroxy-6-méthyl-heptanoïque est un composé organique contenant 8 atomes de carbone.
Explications
La formule chimique de la statine est C8H
Les acides aminés gamma lient le groupe amino au carbone 4, contrairement aux acides aminés alpha plus courants, qui se lient au carbone 2.
Voir aussi la somatostatine et l'endostatine.
Pepstatine
La pepstatine est un puissant inhibiteur des protéases aspartiques. Elle est un hexapeptide contenant l'acide aminé inhabituel statine, un isovaléryle ayant la séquence val-Val-Sta-Ala-Sta (TVA- Val-Val-Sta-Ala-Sta). À l'origine, elle est isolée de cultures de plusieurs espèces d'Actinomyces (actinomycètes),
La pepstatine ::
Produits de pepstatine et structure de la pepstatine dans le centre catalytique de la pepsine. La pepstatine a la séquence Isovaleryl-Val-Val-Sta-Ala-Sta (Iva-Val-Val-Sta-Ala-Sta).
En raison de sa capacité à inhiber la pepsine à des concentrations picomolaires. La pepstatine A est bien connue pour être un inhibiteur des protéinases aspartiques telles que la pepsine, les cathepsines D et E, ou cardosines. Outre son rôle d'inhibiteur de protéase, l'action pharmacologique de ce composé sur les cellules reste incertaine. La pepstatine A supprime la différenciation des ostéoclastes médiée par l'activation du récepteur NF-kB (en anglais "RANKL" à "Receptor Activated C F K B ligand").
La pepstatine A supprime la formation d'ostéoclastes multinucléaires dans un phénomène dose-dépendant. Cet effet inhibiteur n'affecte que les ostéoclastes, et aucun effet sur les cellules apparentées aux ostéoclastes n'a été décrit. La pepstatine A supprime également la pré-différenciation - ostéoclastes dans les ostéoclastes mononucléaires de manière dose-dépendante.
Cette inhibition semble être indépendante de l'activité protéolytique de la cathepsine D, ou d'autres protéases, puisque la formation d'ostéoclastes n'est pas inhibée lorsqu'elle est exposée à des concentrations capables d'inhiber l'activité de la cathepsine D. La signalisation cellulaire semble indiquer que la phosphorylation d'ERK est inhibée dans les cellules traitées avec la pepstatine A, alors que la phosphorylation d'IkB et d'Akt ne montre pas de signes d'altération.le traitement par la pepstatine A semble entraîner une diminution de l'expression du facteur nucléaire des cellules T activé c1 ("NFATc1" pour "Nuclear Factor Activated T cells"). Ces résultats semblent indiquer que la différenciation pepstatine A supprime ostéoclastes en bloquant la voie de signalisation de ERK et l'inhibition de l'expression de NFATc1.
Molécule de pepstatine :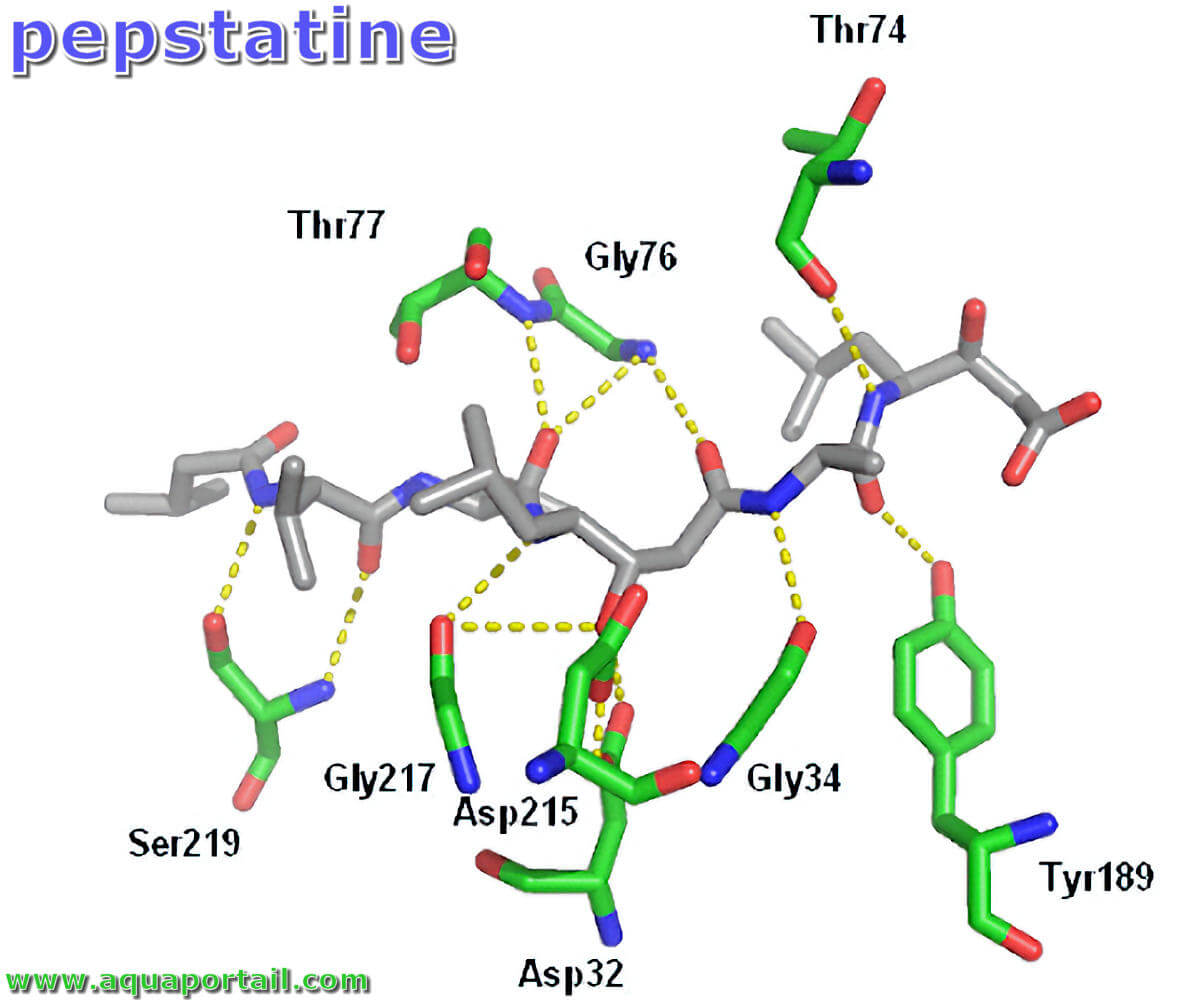
Structure de la pepstatine au centre catalytique de la pepsine. La pepstatine est un composé organique qui contient 34 atomes de carbone et a un poids moléculaire de 685 892 Da.
La pepstatine est pratiquement insoluble dans l'eau, le chloroforme, l'éther ou le benzène, cependant, elle peut être dissoute dans le méthanol, l'éthanol et le DMSO avec de l'acide acétique à une concentration comprise entre 1 et 5 mg/mL.
La pepstatine est un inhibiteur peptidique isolé à partir de cultures d'Actinomyces et est largement utilisé comme inhibiteur puissant de la cathepsine E. La pepstatine est un puissant inhibiteur des protéases aspartiques.
La pepstatine est un hexapeptide contenant l'acide aminé inhabituel statine. La pepstatine est isolée à l'origine des cultures de plusieurs espèces d'Actinomyces, en raison de sa capacité à inhiber la pepsine à des concentrations picomolaires.
Parce que cet inhibiteur est un inhibiteur général des peptidases aspartiques de la famille A1, il n'est cependant pas spécifique de la cathepsine E. En outre, α2 -la macroglobuline s'est avérée être un inhibiteur protéique non spécifique de la cathepsine E. La dégradation de la ribonucléase A réduite et carboxyméthylée par la cathepsine E à pH 5,5 a été complètement bloquée par l'α2-macroglobuline, mais celle de la chaîne B de l'insuline oxydée n'a pas été inhibée par cette protéine.
Toutes les protéinases aspartiques sont inhibées par la pepstatine, par la liaison du groupe hydroxyle de la statine aux deux aspartates catalytiques. La constante d'inhibition (Ki) de la pepstatine pour la chymosine déterminée à pH 6,0 et 3,2 est de 2,2 × 10-7 mol/l et 3,2 × 10-8 mol/l, respectivement. La pepsine et la cathepsine montrent également une dépendance au pH de l'effet inhibiteur, et la pseudochymosine est plus sensible à la pepstatine qu'à la chymosine.
La pepstatine étant relativement inefficace vis-à-vis de la chymosine de veau, des inhibiteurs analogues ont été développés.
La cathepsine D sensible à la pepstatine A est une endopeptidase de l'acide aspartique qui est localisée dans le compartiment endolysosomal des cellules et induit le clivage protéolytique d'une grande variété de substrats endosomaux à pH acide, tels que les hormones polypeptidiques, les protéines et les toxines végétales ou bactériennes.
La tripeptidyl peptidase lysosomale insensible à la pepstatine est une protéine de 46 kDa qui élimine normalement les tripeptides de l'extrémité N-terminale des protéines.
La pepstatine est pratiquement insoluble dans l'eau, le chloroforme, l'éther ou le benzène, cependant, elle peut être dissoute dans du méthanol, de l'éthanol et du DMSO avec de l'acide acétique, à une concentration comprise entre 1 et 5 mg/mL.
Pour distinguer la sedolisine et la sedolisine-B des autres carboxylprotéinases insensibles à la pepstatine, l'inhibition par la tyrostatine doit être déterminée, car la tyrostatine est un inhibiteur spécifique à la fois de la sedolisine et de la sedolisine-B. La tyrostatine a été isolée par nous en 1989 à partir de Kitasatosporia
Synonymes, antonymes
Voir tous les synonymes pour "statine".1 synonyme (sens proche) de "statine" :
1 antonyme (sens contraire) :
- libérine
Les mots ou les expressions apparentés à STATINE sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
Le mot STATINE est dans la page 4 des mots en S du lexique du dictionnaire.
Mots en S à proximité
stalagmite staminé staminode staphylocoque stase statinestation de lagunage station hydrométrique stationnaire statistique statoblaste
En rapport avec "statine"
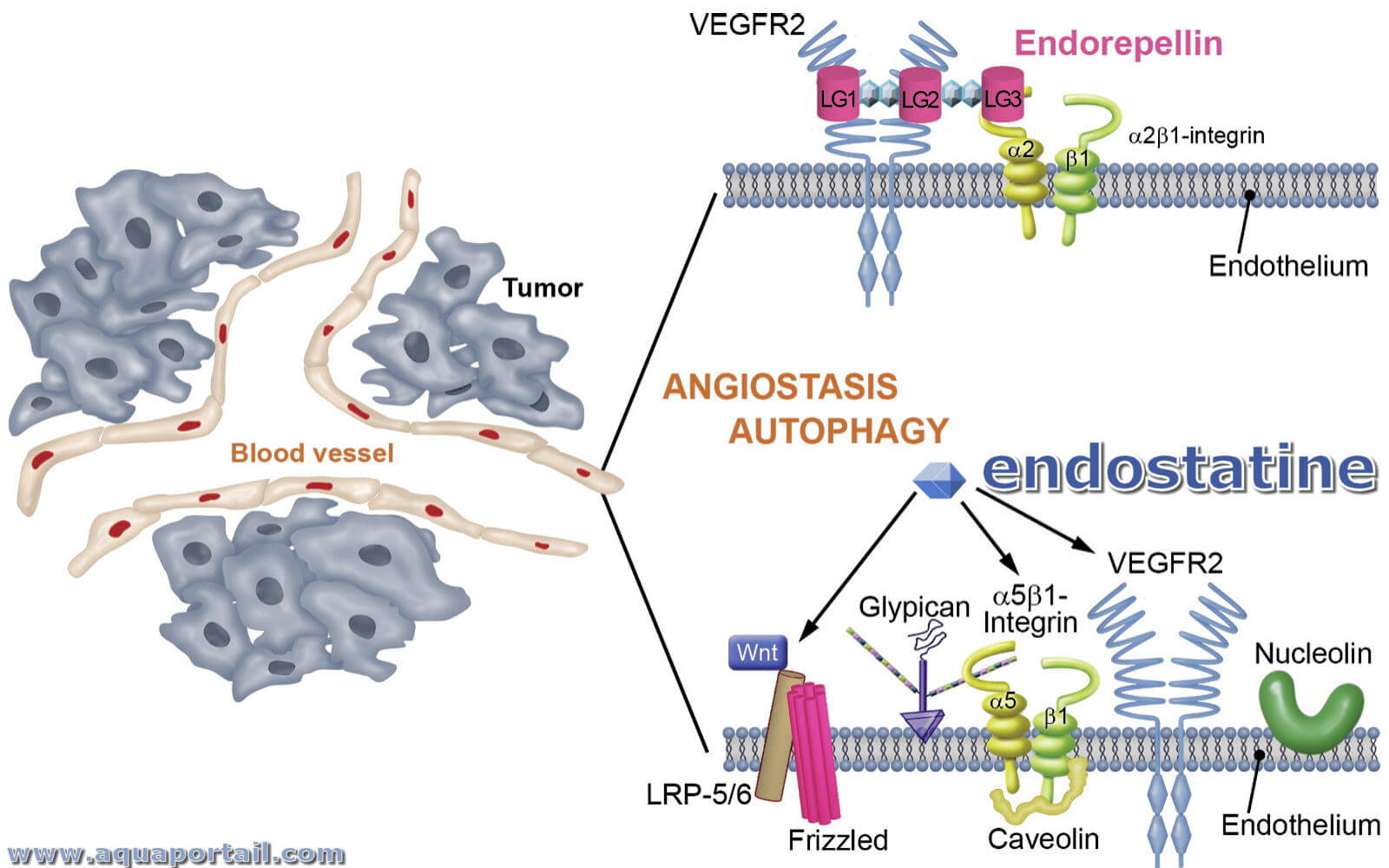
L'endostatine est un polypeptide de 184 acides aminés, correspondant au domaine globulaire trouvé à l'extrémité C-terminale du collagène de type 18.
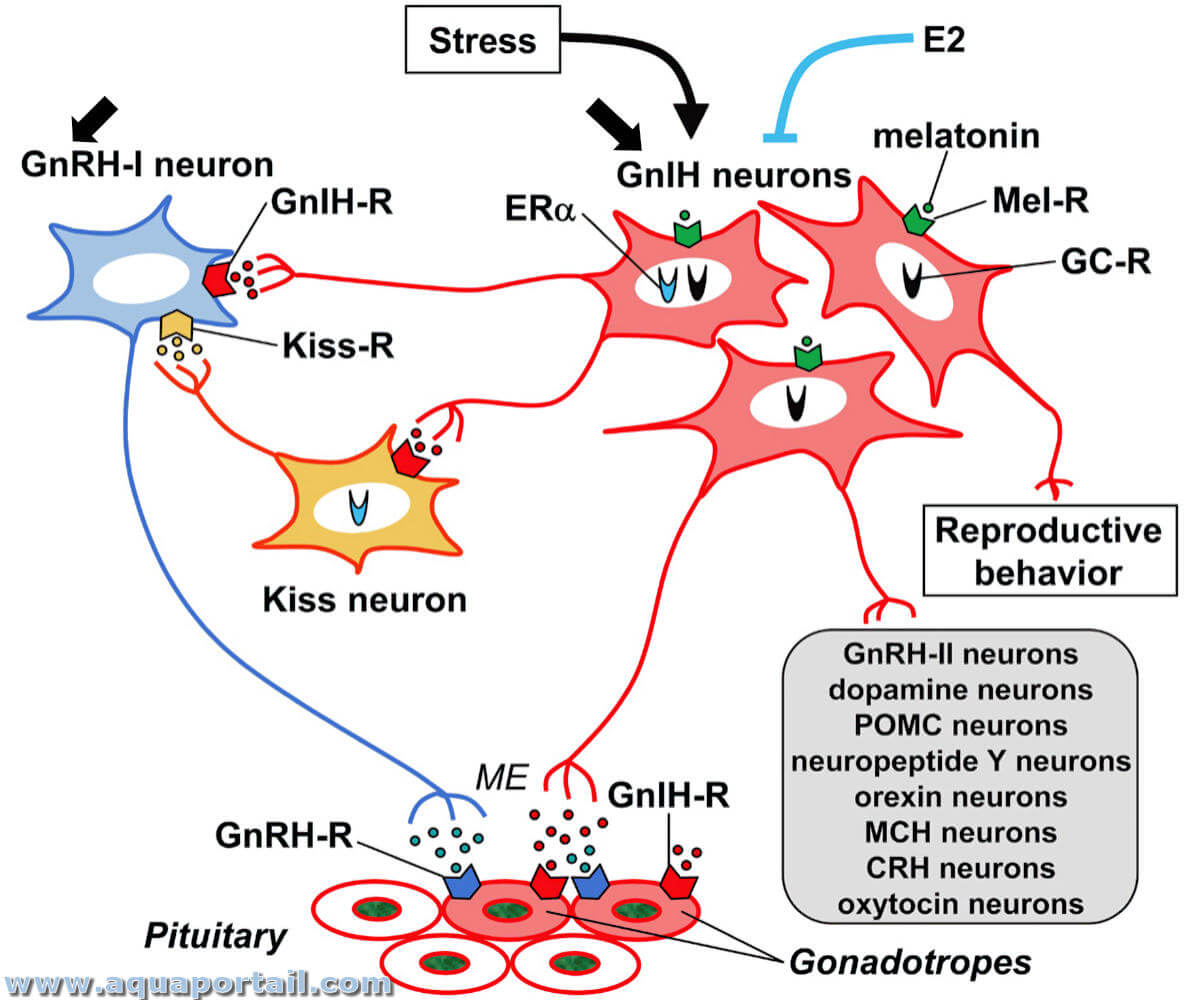
La gonadolibérine (GnRH, Gonadotropin releasing hormone) désigne une hormone polypeptidique sécrétée par l'hypothalamus stimulant la synthèse...
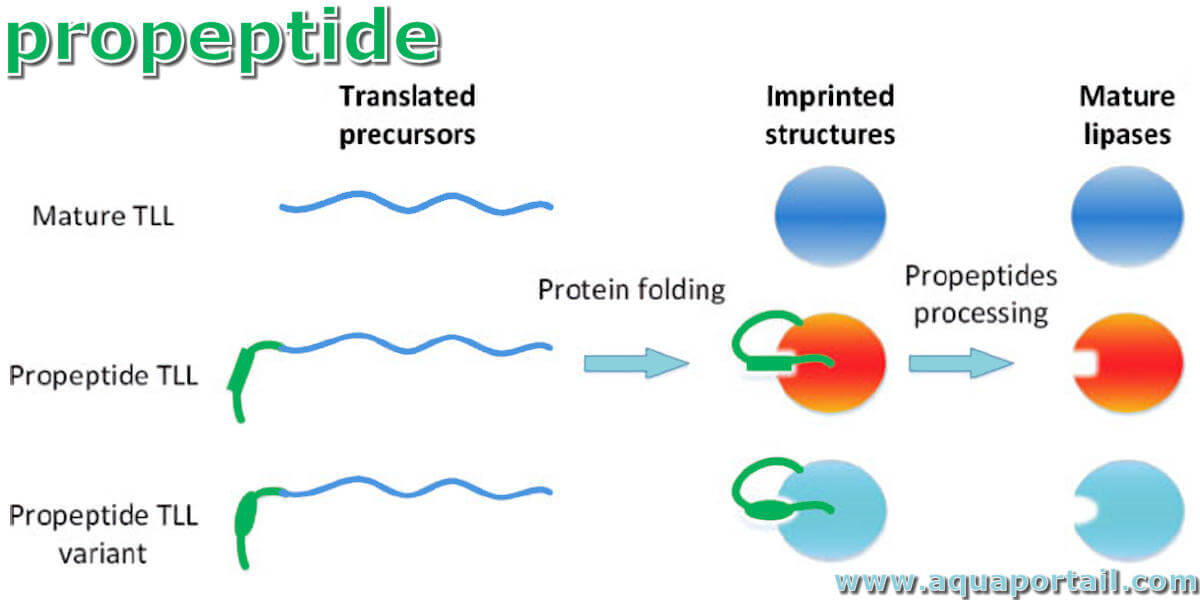
Un propeptide est un précurseur protéique, une proprotéine. Les propeptides sont de courtes séquences qui facilitent le repliement des protéines.

Connue sous le sigle GHRH, la somatolibérine (ou somatocrinine) est l'hormone polypeptidique hypothalamique provoquant la sécrétion de l'hormone somatotrope...
