Mutarotation
Définition
La mutarotation est un phénomène qui intervient lorsque les sucres sont dissous dans l'eau. Le glucose peut servir d'exemple. Si la forme de la chaîne ouverte se transforme en anneau, le groupe OH nouvellement formé peut être en forme alpha, en forme bêta, ou vers le haut.
La mutarotation du glucose :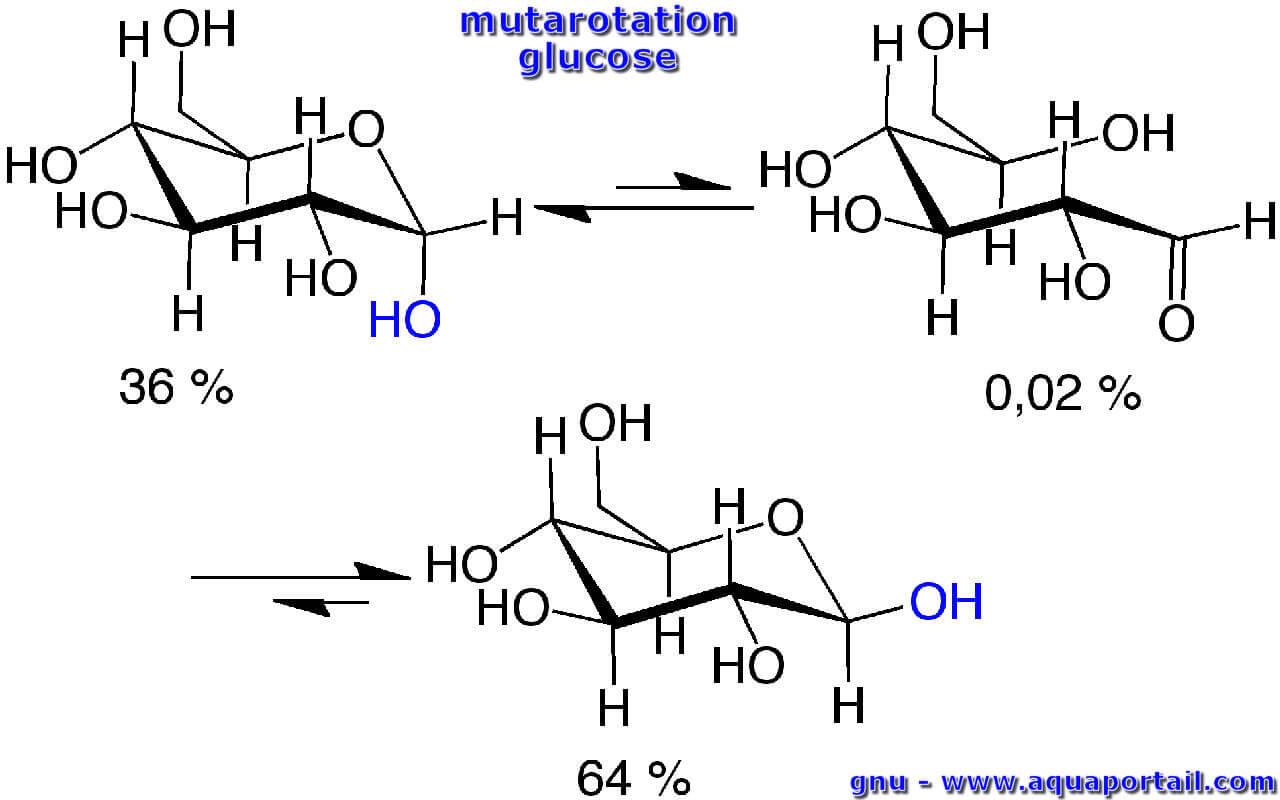
Schéma de la mutarotation entre les formes alpha et bêta du glucose. De nombreux hydrates de carbone sont optiquement actifs, c'est-à-dire qu'ils font tourner une lumière polarisée linéairement autour d'un angle de rotation spécifique à chaque structure.
Explications
La mutarotation fait référence au changement de la rotation optique qui accompagne l'épimérisation. Dans la chimie des sucres, ce terme désigne habituellement l'épimérisation de l'atome de carbone de l'hémiacétal.
Dans la structure cyclique du glucose, le carbone 1 devient chiral, et est appelé carbone anomérique (carbone hémiacétal). Deux anomères sont distingués selon la disposition du groupe hydroxyle : dans les monosaccharides de la série D (par rapport au glycéraldéhyde), le groupe hydroxyle reste en position axiale (vers le bas dans la représentation plane) dans l'anomère alpha et dans la position équatoriale (vers le dessus dans la représentation plate) dans l'anomère bêta.
Les formes alpha et bêta du glucose sont des diastéréoisomères, elles ont donc des propriétés physiques différentes. Parmi celles-ci, la rotation optique.
Lorsque le D-glucose est cristallisé dans l'éthanol, il subit un processus de cyclisation donnant lieu à l'alpha-D-glucopyranose avec un point de fusion de 146 °C et alpha-D +112,2 °. Si l'on cristallise le D-glucose à partir d'un mélange d'éthanol et d'eau, on fait un cycle pour obtenir du bêta-D-glucopyranose, avec un point de fusion compris entre 148 et 155 °C et alpha-D +18,7 °.
Malgré leur interconversion facile en solution, les formes alpha et bêta des glucides peuvent exister indépendamment, beaucoup pouvant être isolées sous forme de solides cristallins sous forme pure. Les deux formes à l'état solide ne s'interconvertissent pas, étant indéfiniment stables. Il est à noter que pour mesurer ces rotations optiques, on procède à la mesure immédiate après la dissolution de chacune d'elles dans l'eau.
Lorsqu'elle est laissée au repos, la rotation optique de la solution contenant l'isomère alpha diminue de 112,2 ° à +52,5 °; la rotation de la solution d'isomère bêta augmente de +18,7 ° à la même valeur de +52,5 °. Ce phénomène est la mutarotation, dans laquelle le cycle pyrane (structure monomère) peut être ouvert pour former un aldéhyde acyclique (représentant un intermédiaire du procédé) par une réaction chimique (forme ouverte); il se ferme en donnant la forme alpha ou bêta, obtenant à la fin un mélange en équilibre bien que nous ayons commencé seulement à partir de la forme alpha ou bêta.
La répartition entre les formes anomères alpha et bêta à l'équilibre est calculée à partir des rotations optiques des isomères purs et de la rotation optique finale de la solution, et elle est déterminée à 36 % et 64 % à une température de 25 °C. À l'équilibre, seules les formes pyranosées du D-glucose sont présentes en quantités significatives car la forme ouverte du glucose représente 0,02 %, une valeur si faible qu'elle est négligeable.
Les sucres cycliques présentent une mutarotation lorsqu'ils sont transformés en leurs formes anomères α et β.
Le processus a été découvert par Dubrunfaut en 1846 quand il s'est rendu compte que la rotation spécifique des solutions aqueuses de sucres a changé au fil du temps.
Synonymes, antonymes
Voir tous les synonymes pour "mutarotation".0 synonyme (sens proche) pour "mutarotation".
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à MUTAROTATION sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
Le mot MUTAROTATION est dans la page 5 des mots en M du lexique du dictionnaire.
Mots en M à proximité
Mustélidés mutagène mutagenèse mutagenèse dirigée mutant mutarotationmutase mutation mutation faux-sens mutation non-sens mutation par décalage de cadre
En rapport avec "mutarotation"

La rotation des cultures consiste à alterner des plantes de familles différentes et avec des besoins nutritionnels différents dans un même lieu pendant...

Une dismutase est une enzyme qui catalyse une réaction de dismutation. Une dismutation est une réaction redox dans laquelle le substrat agit à la fois comme...
Une mutase est une enzyme de la classe des isomérases qui catalyse le déplacement intramoléculaire d'un groupement fonctionnel.

Une rotation est un mouvement circulaire d'un objet autour d'un center (ou point) de rotation.
