Uréase
Définition
L'uréase est l'enzyme qui divise l'urée (catalysant l'hydrolyse de l'urée) en ammoniac et en dioxyde de carbone ou en carbamate d'ammonium et carbonate; étant donné que la réaction se déroule en solution aqueuse, des ions carbonate d'hydrogène se forment également dans certains cas.
Les deux réactions types sont :
- H2N-CO-NH2 + H2O → 2 NH3 + CO2.
- H2N-CO-NH2 + 2 H2O → 2 NH4+ + CO32-.
L'hydrolyse de l'urée a lieu en deux étapes. Dans la première étape, de l'ammoniac et du carbamate sont produits. Le carbamate s'hydrolyse spontanément et rapidement en ammoniac et en acide carbonique. L'activité uréase augmente le pH de son environnement lorsque l'ammoniac est produit, qui est basique.
La molécule d'uréase :
Les uréases (EC 3.5.1.5) appartiennent fonctionnellement à la superfamille des amidohydrolases (hydrolases) et des phosphotriestérases (estérases).
Explications
L'uréase appartient au groupe des amidases et se trouve souvent dans les graines de plantes, les bactéries, les crabes et les mollusques bivalves marins.
Uréase végétale en botanique
En botanique, l'uréase végétale est une enzyme catalysant la dégradation de l'urée (avec azote) chez les streptophytes Streptophyta et les Ulvophycées Ulvophyceae, tandis que ce rôle est joué par une uréeamidolyase chez les Chlorophycées Chlorophyceae et les Trebouxiophyceae. Elle est présente en abondance dans les sols avec une plus forte activité dans la rhizosphère. L'oligoélément nickel est un des constituants de l'uréase.
L'uréase végétale agit comme un insecticide indépendamment de la fonction de séparation de l'urée et produit une agrégation plaquettaire dans le sang des mammifères.
L'uréase des haricots blancs a été la première enzyme qui a pu être purifiée et cristallisée par James Batcheller Sumner (Prix Nobel de chimie) en 1926.
Description
En particulier, l'uréase dans les bactéries du sol joue un rôle important dans le cycle de l'azote, car sans elle, la fertilisation azotée ne serait pas possible en raison de l'urée, un composant du lisier, qui résiste à la décomposition en l'absence d'enzymes. De l'autre côté sont des bactéries uréase positives dans les selles la cause des indésirables ammoniac-émissions dans l'élevage (en Allemagne en 2005, environ 490 000 tonnes de 590 000 des émissions totales d'ammoniac).
L'activité catalytique de l'enzyme augmente considérablement la vitesse de réaction d'un facteur 1014. L'uréase des haricots (et probablement aussi des bactéries) est une métalloenzyme et contient du nickel.
n raison de la structure du centre contenant du nickel dans la chimie organométallique, l'uréase est considérée comme un système modèle possible pour l'activation catalytique du dioxyde de carbone. N-carbamates complexes (liaison de l'atome de carbone pauvre en électrons du dioxyde de carbone à l'atome d'azote riche en électrons des imines/amines) avec du nickel (0 ou 2-valent -divalent-) comme atome central existent et sont structurellement caractérisés; Des études spectroscopiques infrarouges ont montré une réduction d'énergie (activation) des doubles liaisons C=O thermodynamiquement très stables. Cependant, la preuve du transfert de ce dioxyde de carbone "activé" vers d'autres substrats est toujours en suspens.
Signification médicale
Les organismes (par exemple Helicobacter pylori, cause d'ulcères de l'estomac et du duodénum) qui ont de l'uréase sont souvent des agents pathogènes du système digestif, car ils peuvent survivre dans l'environnement acide de l'estomac en raison de l'ammoniac libéré. Il en est de même pour les espèces pathologiques du genre Proteus (ne pas confondre avec l'animal appelé le terrariophilie-2176-proteus-anguinus.html">protée !), qui colonisent ainsi le tractus urogénital. Cette réaction alcaline de l'ammoniac est également utilisée pour détecter ces organismes.
Importance pour l'agriculture
L'uréase dans les bactéries du sol est la condition préalable à l'action des excréments comme engrais azoté, car seul le clivage hydrolytique de l'urée rend l'azote disponible sous forme d'ions ammonium. Cependant, l'ammoniac intermédiaire est gazeux et seules de petites quantités de gaz peuvent être absorbées par l'humidité du sol. Une partie de l'ammoniac s'échappe donc toujours et se perd sous forme d'engrais. Cette proportion est d'autant plus grande que l'urée de matière première est concentrée et donc le plus d'ammoniac est perdu par le sol et le fumier de la maison.
Étant donné que l'ammoniac est également nocif pour l'environnement de plusieurs manières et que des accords internationaux ont été conclus pour limiter les émissions, des tentatives sont faites, entre autres, avec des inhibiteurs d'uréase (résoudre le problème et réduire les émissions des écuries).
Cinétique
La réaction de l'uréase avec l'urée peut être utilisée pour illustrer la dépendance de la vitesse de réaction au temps lorsque l'on choisit une solution d'urée avec une concentration élevée.
Puisque les ions se forment lorsque l'urée se décompose en solution aqueuse, l'augmentation des ions peut être suivie en mesurant la conductivité. La conductivité augmente linéairement sur une période de temps plus longue.
La réaction peut également être surveillée par photométrie. Du bleu de bromothymol est ajouté comme indicateur, qui vire au bleu de plus en plus intense au cours de la réaction. L'extinction, une mesure de concentration, augmente également linéairement sur une période de temps plus longue.
Lorsque l'urée se désintègre, la vitesse de réaction est constante sur une période de temps plus longue. Il y a une réaction d'ordre zéro pour cela.
Il est cependant crucial que la concentration en substrat, ici celle de l'urée, ne soit pas trop faible. Pour des concentrations de substrat plus petites, ces expériences peuvent être utilisées pour illustrer la dépendance de la vitesse de réaction sur la concentration, le temps étant maintenu constant, conformément à la théorie de Michaelis-Menten.
Histoire
Les effets de l'uréase ont été découverts par Fourcroy et Vauquelin en 1798 et associés par Louis Pasteur en 1861 à des micro-organismes décrits pour la première fois par Van Tieghem en 1864 sous le nom de Micrococcus ureae. En 1876, l'uréase bactérienne a été isolée par le muscle et la réaction catalytique a été définie. Seule la découverte de l'uréase de soja par T. Takeuchi en 1909 et sa production ultérieure en grandes quantités ont permis de mener des études approfondies.
Synonymes, antonymes
Voir tous les synonymes pour "uréase".0 synonyme (sens proche) pour "uréase".
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à URÉASE sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
Le mot UREASE est dans la page 1 des mots en U du lexique du dictionnaire.
Mots en U à proximité
uranidine uranoscope urbanisation urcéolé Ureaplasma urealyticum uréaseurédie urédiniospore urédospore urée urée formaldéhyde
En rapport avec "uréase"

Une désoxyribonucléase est une enzyme qui catalyse l'hydrolyse des chaînes moléculaires d'acide désoxyribonucléique (ADN) en chaînes moléculaires plus courtes...
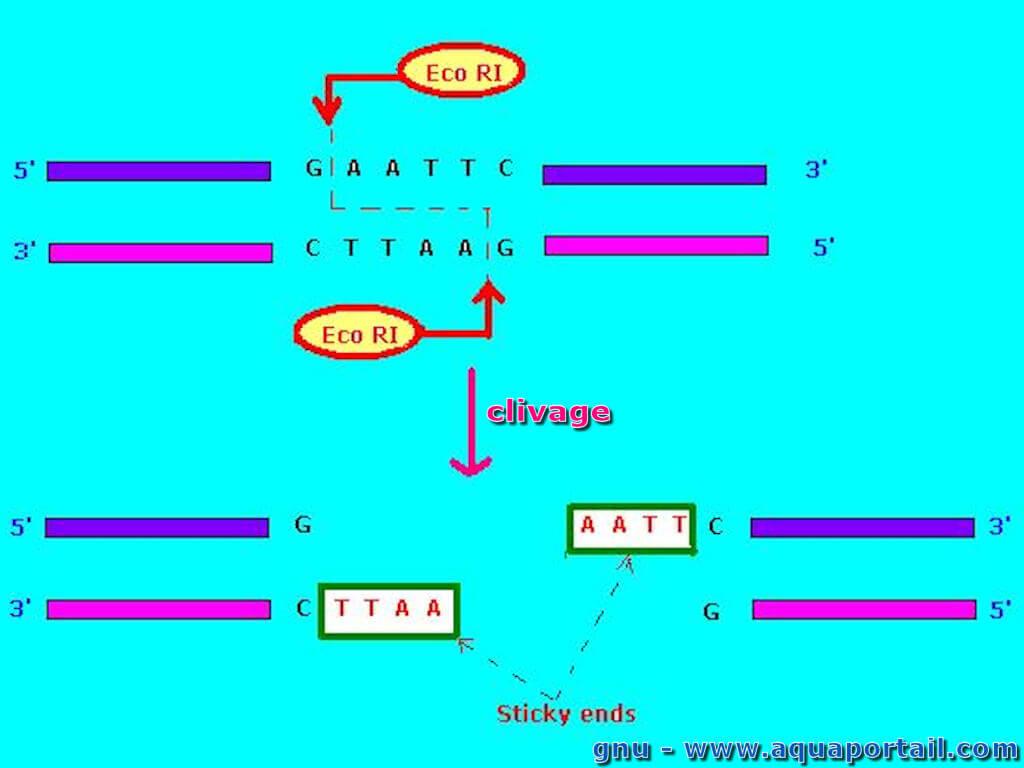
Une endonucléase est une nucléase qui se passe à l'intérieur, en dedans, par hydrolysation.
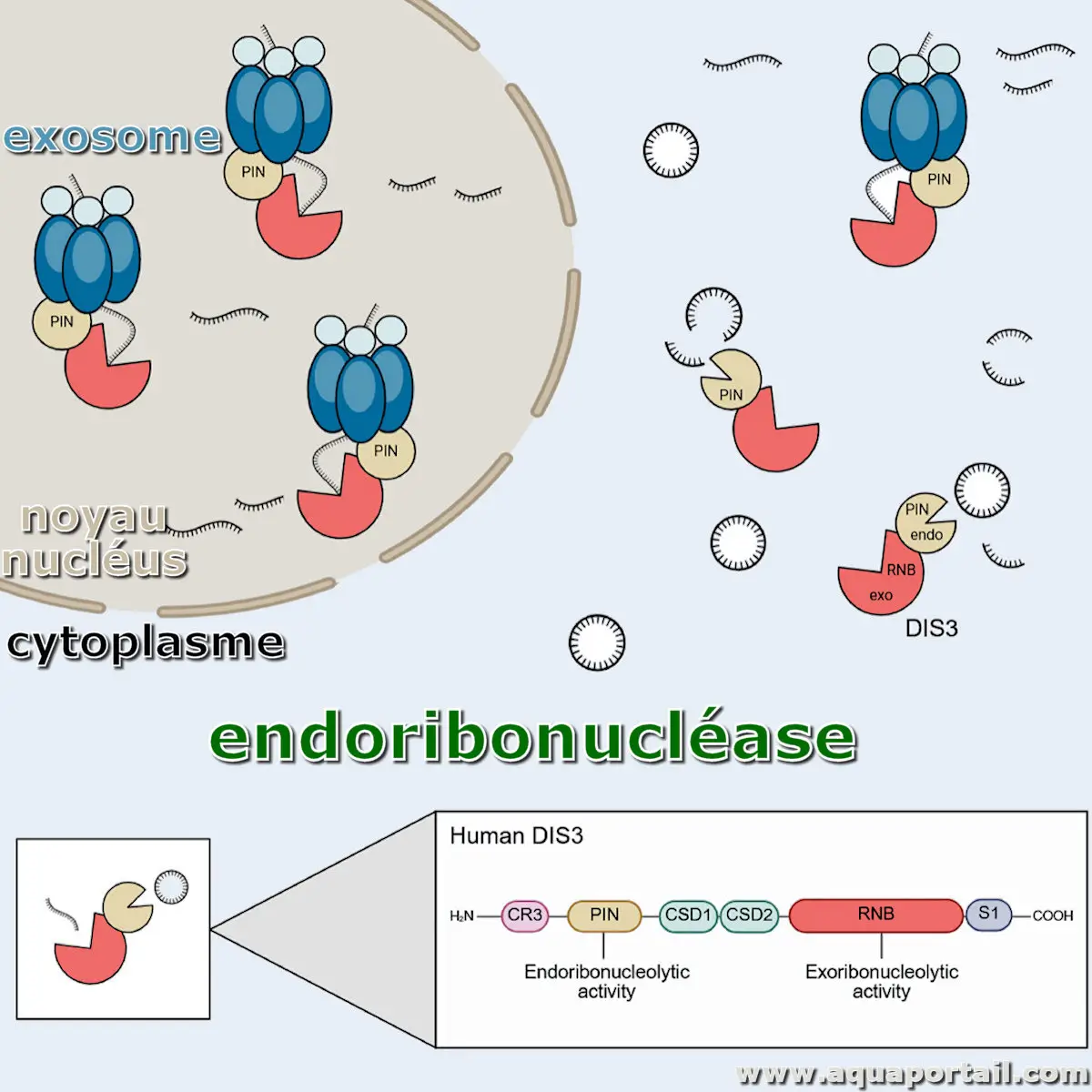
Une endoribonucléase est une enzyme appartenant au groupe plus large des ribonucléases, spécialisée dans le clivage de l'ARN.
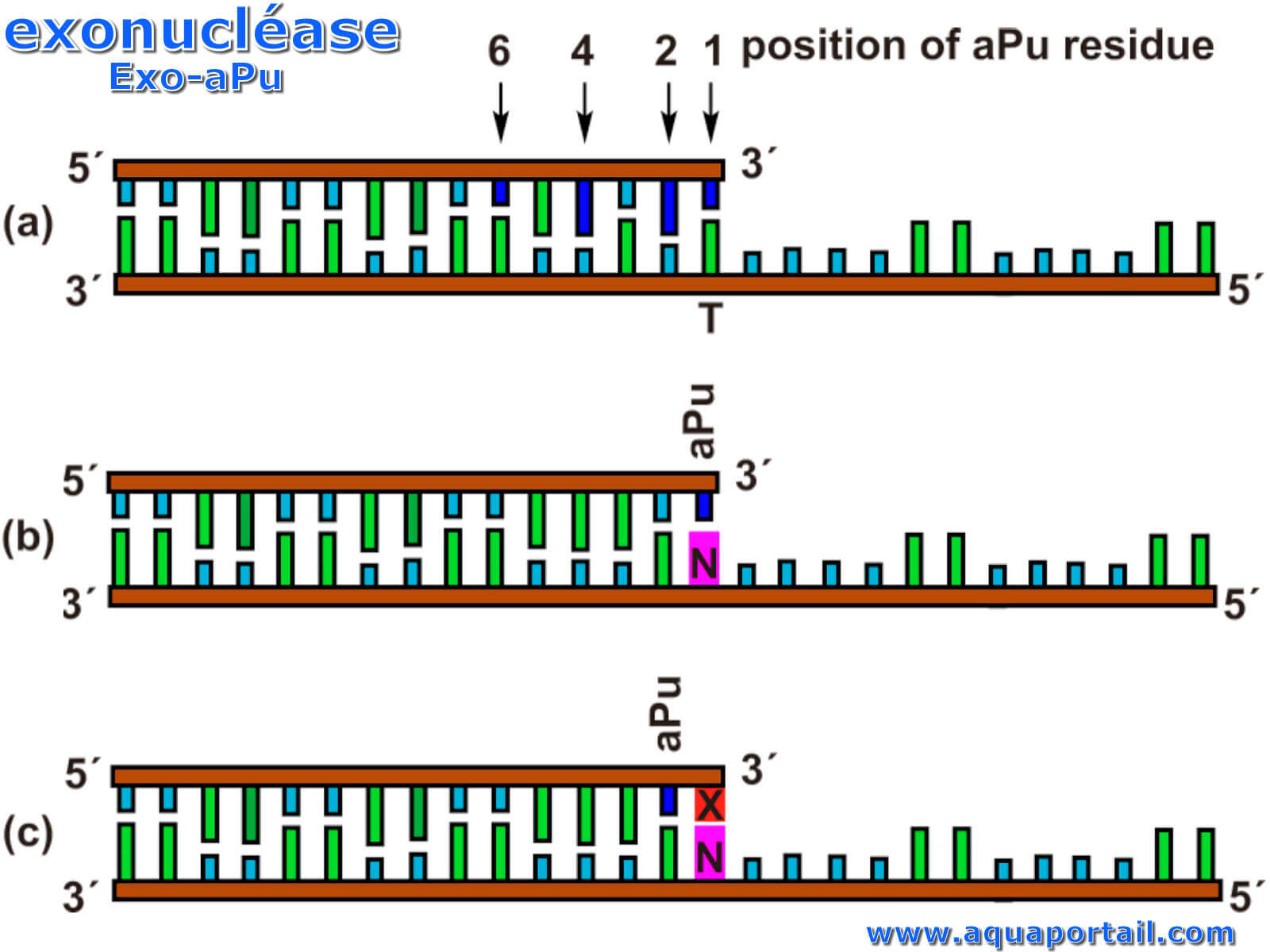
L'exonucléase distingue la partie qui est au-dehors de la nucléase. Les exonucléases sont des enzymes qui fonctionnent en coupant les nucléotides...
