Eau de cristallisation
Définition
Une eau de cristallisation est une eau en combinaison avec une substance cristallisée. Cette eau d'hydratation est mécaniquement interposée dans quelques substances. Elle produit un phénomène de décrépitation lorsqu'on expose ces substances à la chaleur. Cette eau du sol interposée ne constitue jamais qu'une très infime partie du poids des corps dans lesquels elle se trouve. Pour chasse l'eau de cristallisation, il suffit de réduire ces corps en poudre et de les exposer au soleil ou à une température de 100 °C.
Une eau de cristallisation :
L'eau de cristallisation est de l'eau qui est incluse en tant que ligand dans le réseau cristallin d'un produit chimique. Dans les formules chimiques, les molécules d'eau de cristallisation sont généralement indiquées après un point.
Explications
L'eau cristalline ou eau d'hydratation est le nom donné à l'eau liée au solide cristallin. Les substances cristallines contenant de l'eau sont également appelées hydrates. Lorsqu'ils sont cristallisés dans de l'eau ou des solvants qui en contiennent, de nombreux composés chimiques incorporent de l'eau dans leur réseau cristallin.
Les molécules d'eau peuvent être liées de façon coordonnée à des ions (eau de coordination, par exemple, sulfate de cuivre), présentes sous forme d'eau structurelle liée à des molécules par des liaisons hydrogène, ou - comme les minéraux du groupe zéolite - ne pas être impliquées dans le réseau cristallin. Les rapports de liaison de l'eau dans les cristaux de protéines sont les plus divers.
L'eau de cristallisation n'est généralement liée que faiblement et s'échappe par la chaleur, ce qui peut entraîner une décoloration du sulfate de cuivre, voire une dissolution dans l'eau de cristallisation de la personne dans le cas d'autres substances.
Un autre nom pour une substance avec de l'eau de cristallisation est un hydrate. La même substance sans eau de cristallisation est alors appelée anhydrate. Les sels anhydres sont appelés anhydrates (par exemple, sulfate de sodium anhydrate, sulfate de cuivre anhydrate, à ne pas confondre avec anhydride et anhydrite). Les anhydrates sont généralement des substances hautement hygroscopiques et sont donc utilisés pour sécher les solvants et les gaz.
Lorsque les hydrates sont formés, de l'énergie est ensuite libérée sous forme de chaleur d'hydratation - c'est l'énergie qui doit être fournie pendant la déshydratation (donc la "combustion").
Présence et occurrences
L'eau de cristallisation est très présente dans les hydrates de sel, les cristaux de protéines, mais aussi dans les cristaux de substances organiques polaires. De nombreux composés chimiques entraînent avec eux des molécules du solvant dans le cristal lorsqu'ils cristallisent à partir de solutions. À partir d'une solution aqueuse, il s'agit donc d'eau, mais dans l'ammoniac liquide, par exemple, la même chose existe souvent avec les molécules d'ammoniac.
La présence d'eau de cristallisation peut affecter de manière significative les propriétés, telles que la couleur et la dureté, du solide. En fait, l'hydrate est simplement un autre composé chimique : les molécules d'eau sont liées chimiquement. L'eau de cristallisation peut exister avec des sels et des acides. Certains acides ne peuvent être isolés que sous forme d'hydrate, comme l'acide hexafluorosilicique, qui peut être cristallisé avec deux molécules d'eau de cristallisation sous forme solide, mais sans décomposition de l'eau. De nombreux sels ont plusieurs hydrates.
Par exemple, le sulfate de cuivre bleu profond bien connu (en photo au-dessus) est un pentahydrate avec cinq molécules de H2O par unité de formule. Lorsqu'il est chauffé, il perd son eau.
Un autre exemple bien connu d'incorporation d'eau dans un réseau cristallin solide est le durcissement du gypse. L'hémihydrate de sulfate de calcium 2 CaSO4·H2O en poudre est mélangé à de l'eau liquide et versé dans un moule. Avec cela, l'eau liquide disparaît et il ne reste qu'un solide durci (le dihydrate).
La plupart des substances contenant de l'eau de cristallisation sont donc des solides "secs", mais il existe également des hydrates qui ont leur propre point de fusion. En général, il s'agit d'une température beaucoup plus basse que celle de l'anhydrate. Le chlorure de zinc sous forme strictement sèche fond à 317 °C, mais les hydrates (il y en a plus) fondent à ou en dessous de la température ambiante. On pourrait dire que ces substances se "dissolvent" dans leur propre eau de cristallisation, mais cela ignore le fait que dans le liquide, les molécules d'eau subissent encore une forte interaction avec le chlorure.
Une grande quantité d'eau est également incorporée dans les cristaux de protéines pendant le processus de cristallisation. Les molécules d'eau y participent au schéma de liaison hydrogène qui est une force majeure qui maintient le cristal ensemble. Dans les cristaux de protéines, on trouve souvent 1 molécule d'eau liée par acide aminé dans la protéine, et en plus une quantité plus ou moins grande d'eau désordonnée se trouve dans le cristal. La partie totale du cristal de protéine qui est remplie d'eau est souvent de dizaines de pour cent.
Effets sur des produits
Les médicaments et autres produits organiques sont souvent basiques et utilisés comme hydrohalogénures. Dans certains cas, les hydrohalogénures cristallisent sous forme d'hydrates en même temps. Exemples : tirofiban et ziprasidone. L'hémihydrate d'estradiol est un autre exemple d'un médicament de base utilisé sous la forme de son hydrohalogénure.
Contrairement aux sels minéraux, les protéines cristallisent avec des quantités d'eau exceptionnellement élevées dans le réseau cristallin. Des contenus contenant jusqu'à 50 % d'eau ne sont pas rares. La couche d'hydratation étendue est ce qui permet aux cristallographes de protéines de justifier que la conformation dans le cristal n'est pas très différente de la conformation libre que la protéine adopte en solution.
Techniquement, on utilise la capacité du gypse à absorber en chauffant (en brûlant) partiellement ou totalement l'eau de cristallisation perdue lors de l'agitation avec de l'eau et en durcissant ainsi.
L'anhydrite est également un minéral dans les dépôts de sel et consiste en sulfate de calcium exempt de sulfate de calcium (CaSO 4). Une autre application technique est l'ajout du gel de silice dessicant au chlorure de cobalt, bleu en l'absence d'eau cristalline et coloré en rose dans l'eau de cristallisation. La décoloration rose du gel de silice traité indique que le gel de silice ne peut plus absorber plus d'humidité et doit donc être régénéré par chauffage.
Les hydrates de sel peuvent servir de réserve de chaleur. L'hydrate est fondu et la chaleur peut être stockée. Si nécessaire, il réagit à nouveau vers un hydrate et dégage de la chaleur. Selon ce principe de travail :
- Packs de chaleur;
- Chauffage central avec panneaux solaires;
- Utilisation de la chaleur perdue dans la voiture.
Synonymes, antonymes
Voir tous les synonymes pour "eau de cristallisation".1 synonyme (sens proche) de "eau de cristallisation" :
- eau d'hydratation
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à EAU DE CRISTALLISATION sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
L'expression EAU DE CRISTALLISATION est dans la page 1 des mots en E du lexique du dictionnaire.
Mots en E à proximité
eau conditionnée eau contaminée eau courante eau d'infiltration eau d'irrigation eau de cristallisationeau de fonte eau de gravitation eau de javel eau de mer eau de mer artificielle
En rapport avec "eau de cristallisation"

La cristallisation, complétée par la recristallisation, décrit généralement la formation (naturelle ou artificielle) de cristaux, habituellement avec...

Une queue de cristallisation, de forme généralement symétrique avec une déformation de type homoaxiale, est une zone cristalline allongée située à l'extrémité...
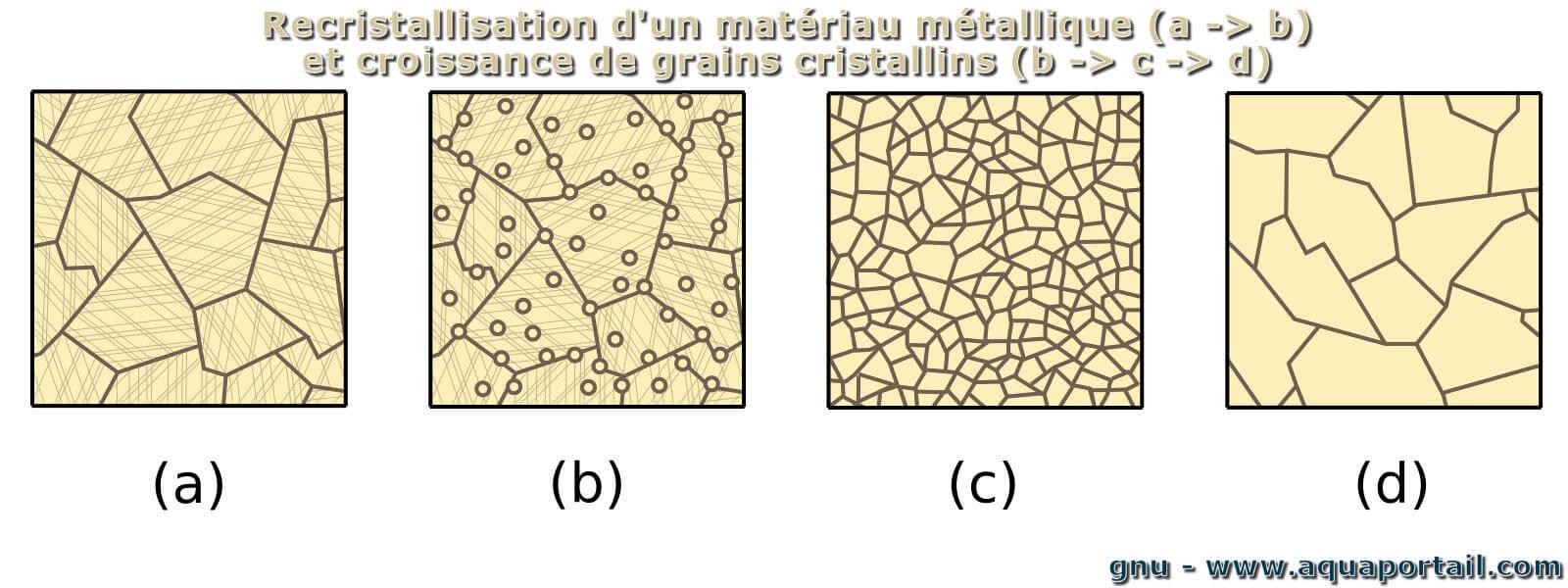
La recristallisation, faisant suite à une cristallisation primaire, est la répétition du processus de cristallisation dans une solution qui a déjà été faite...
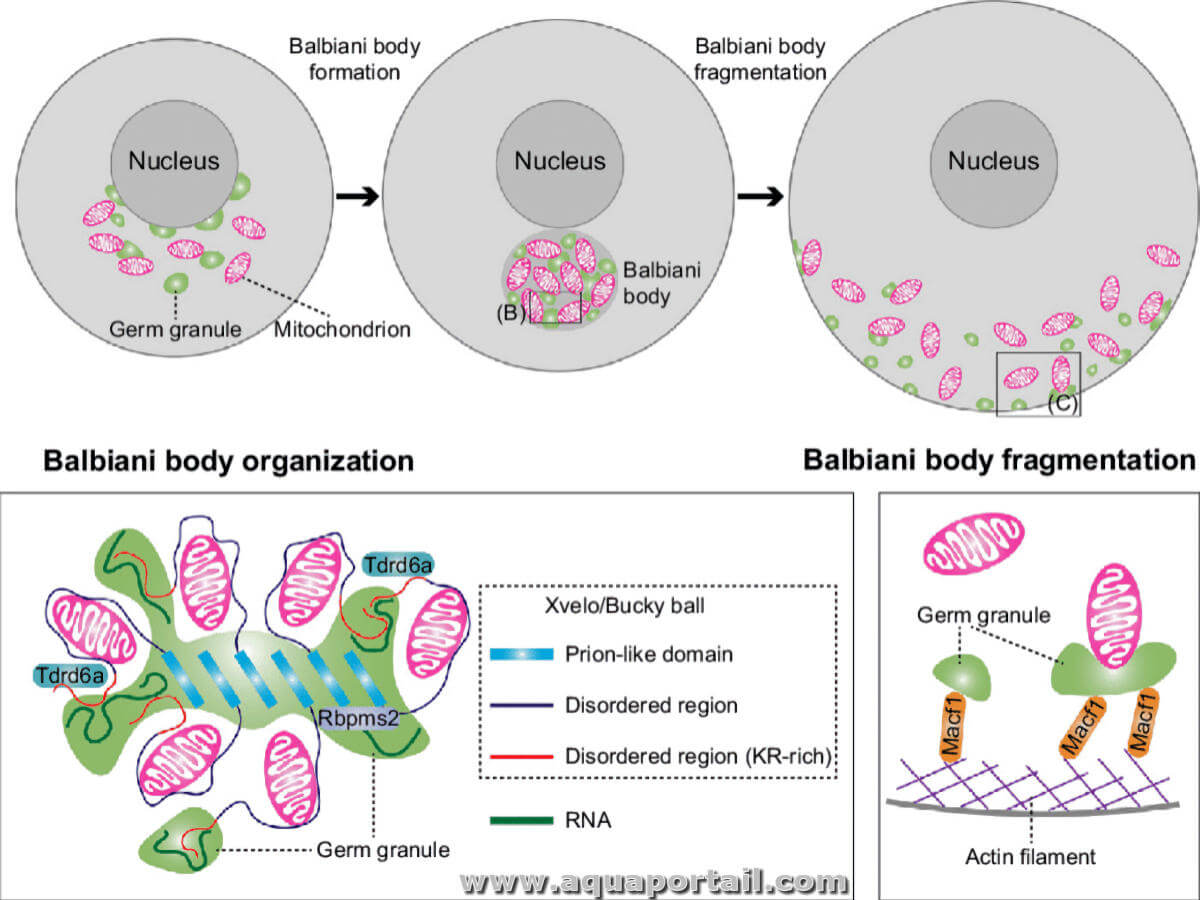
Un anneau de Balbiani (ou corps de Balbiani) est un agrégat ovocytaire conservé qui facilite l'organisation de l'ovocyte en une cellule polarisée avec...
