Oxygène
Définition
L'oxygène est un élément chimique (symbole O, numéro atomique 8) très réactif se liant facilement à d'autres éléments pour former, par exemple, le gaz dioxygène O2 ou l'eau H2O. Sous sa forme de dioxygène moléculaire, un gaz incolore, inodore et insipide, il représente 21 % des gaz atmosphériques.
Une molécule d'oxygène :
L'oxygène O, sous forme électronique, est le 8ème élément de la table période des éléments chimiques.
Explications
L'oxygène est l'accepteur final d'électrons de la chaîne respiratoire mitochondriale. Il est libéré en dioxygène par les organismes photosynthétiques à partir d'une molécule d'eau. C'est un constituant de toutes les molécules organiques.
Son nom vient des racines grecques oxys ("acide", littéralement "piquant", en référence au goût des acides) et gonos ("producteur"), c'est-à-dire "producteur d'acide", car au moment où ce nom a été donné, on a cru à tort que tous les acides avaient besoin d'oxygène pour leur composition. Cette substance comprend une partie importante de l'atmosphère et est nécessaire pour maintenir la vie terrestre.
Il fait partie du groupe des amphiphiles dans le tableau périodique et est un élément non métallique hautement réactif qui forme facilement des composés (en particulier des oxydes) avec la plupart des éléments, à l'exception des gaz nobles hélium et Néon. De même, il s'agit d'un agent oxydant fort et a la deuxième plus haute électronégativité de tous les éléments, en second lieu seulement au fluor. Mesuré par sa masse, l'oxygène est le troisième élément le plus abondant dans l'univers, après l'hydrogène et l'hélium; il est le plus abondant dans la croûte terrestre, formant près de la moitié de sa masse.
En raison de sa réactivité chimique, il ne peut pas rester dans l'atmosphère terrestre en tant qu'élément libre sans être constamment renouvelé par l'action photosynthétique des organismes qui utilisent l'énergie solaire pour produire de l'oxygène élémentaire à partir de l'eau. L'oxygène élémentaire O2 n'a commencé à s'accumuler dans l'atmosphère qu'après l'apparition de ces organismes, il y a environ 2 500 millions d'années. L'oxygène diatomique constitue 20,8 % du volume de l'atmosphère terrestre.
Puisqu'il constitue la majeure partie de la masse d'eau, c'est aussi la composante majoritaire de la masse des êtres vivants. Beaucoup des molécules les plus importantes qui font partie des êtres vivants, tels que les protéines, les acides nucléiques, les glucides et les lipides, contiennent de l'oxygène, ainsi que les principaux composés inorganiques qui forment des coquilles d'animaux, des dents et des os. L'oxygène élémentaire est produit par les cyanobactéries, les algues et les plantes, et toutes les formes de vie complexes l'utilisent pour la respiration cellulaire. Il est toxique d'obliger les organismes anaérobies, les premières formes de vie qui prédominaient sur Terre jusqu'à ce que l'O2 commence à s'accumuler dans l'atmosphère. Une autre forme (allotropique) de l'oxygène, l'ozone O3, aide à protéger la biosphère du rayonnement ultraviolet à haute altitude, dans la couche dite d'ozone, mais pollue près de la surface, où elle est un sous-produit du smog. À des altitudes encore plus élevées en orbite terrestre basse, l'oxygène atomique a une présence significative et provoque l'érosion des engins spatiaux.
| Numéro atomique | 8 |
| masse atomique | 15,999 g.mol-1 |
| électronégativité de Pauling | 3,5 |
| masse volumique | 1,429 g.cm-3 à 20 °C |
| température de fusion | -219 °C |
| Température d'ébullition | -183 °C |
| rayon atomique (Van der Waals) | 0,074 nm |
| rayon ionique | 0,14 (-2) nm |
| isotopes | 2 (O2 : oxygène; O3 : ozone) |
| Configuration électronique | [He] 2s2 2p4 |
| Énergie de première ionisation | 1311 kJ.mol-1 |
| Découverte | Le nom de cet élément vient du grec et engendre le mot acide. |
Carl Wilhelm Scheele a découvert l'oxygène indépendamment à Upsala en 1773, ou même plus tôt, et Joseph Priestley, dans le Wiltshire en 1774, mais l'honneur est souvent attribué à Priestley parce qu'il a publié son travail auparavant. Antoine Lavoisier, dont les recherches ont contribué à discréditer la théorie alors populaire du phlogistique de combustion et de corrosion, a inventé le nom "oxygène" en 1777. Il est produit industriellement par distillation fractionnée d'air liquéfié, l'utilisation de zéolithe avec cycles de la pression pour concentrer l'oxygène de l'air, l'électrolyse de l'eau et d'autres moyens. L'oxygène est utilisé dans la production d'acier, de plastiques et de textiles; les hélices de fusées; oxygénothérapie; et assistance pour respirer dans les avions, les sous-marins, les vols spatiaux et la plongée.
Le transport de l'oxygène du sang est dit oxyphorique.
Synonymes, antonymes
Voir tous les synonymes pour "oxygène".3 synonymes (sens proche) de "oxygène" :
- dioxygène
- oxygène gazeux
- oxygène liquide
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à OXYGÈNE sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
Le mot OXYGENE est dans la page 3 des mots en O du lexique du dictionnaire.
Mots en O à proximité
oxydo-réducteuroxydoréductase oxydoréduction oxygénase oxygénation oxygèneoxygène dissous oxygène liquide oxygène rouge oxygène singulet oxygène solide
En rapport avec "oxygène"

Les besoins en oxygène correspondent à la quantité d'oxygène nécessaire à la vie et au développement optimum d'un organisme d'un point de vue biologique.
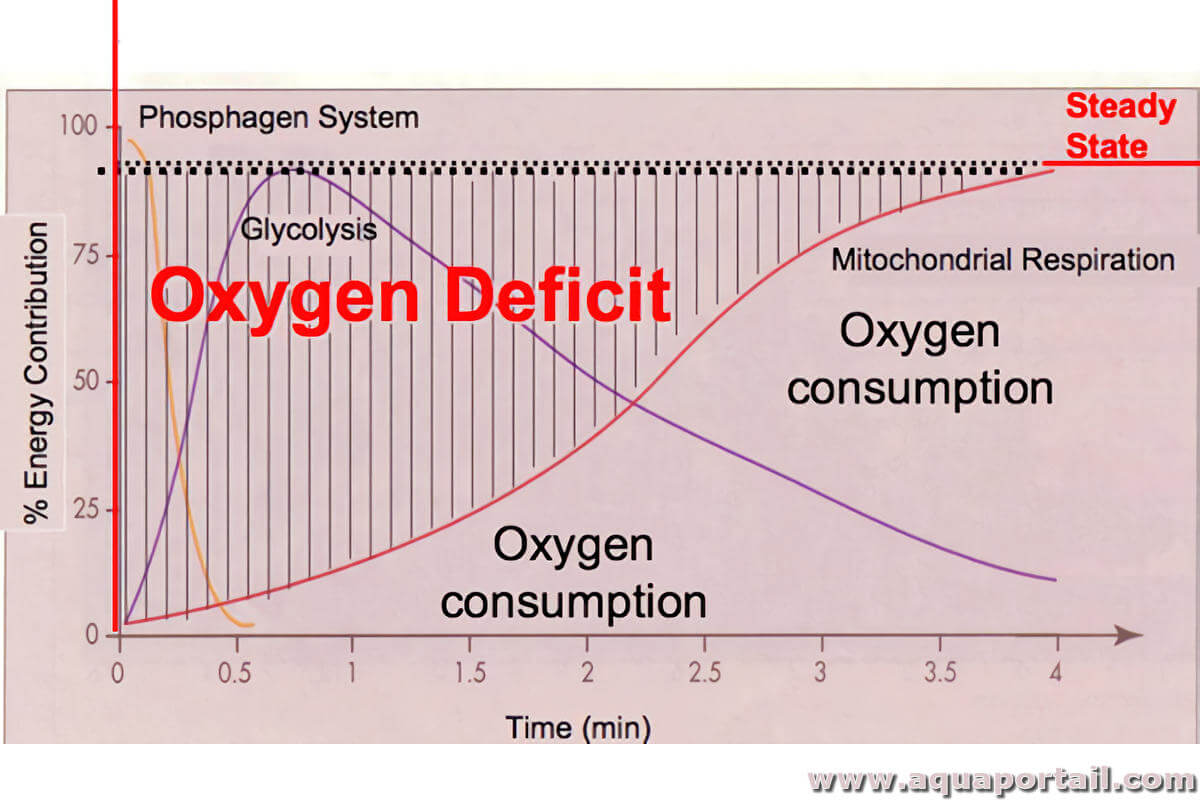
Un déficit en oxygène est la différence entre les concentrations d'oxygène observées et la concentration qui serait présente à 100 % de saturation.
Le dégagement d'oxygène est le processus consistant à générer de l'oxygène moléculaire au travers d'une réaction chimique.
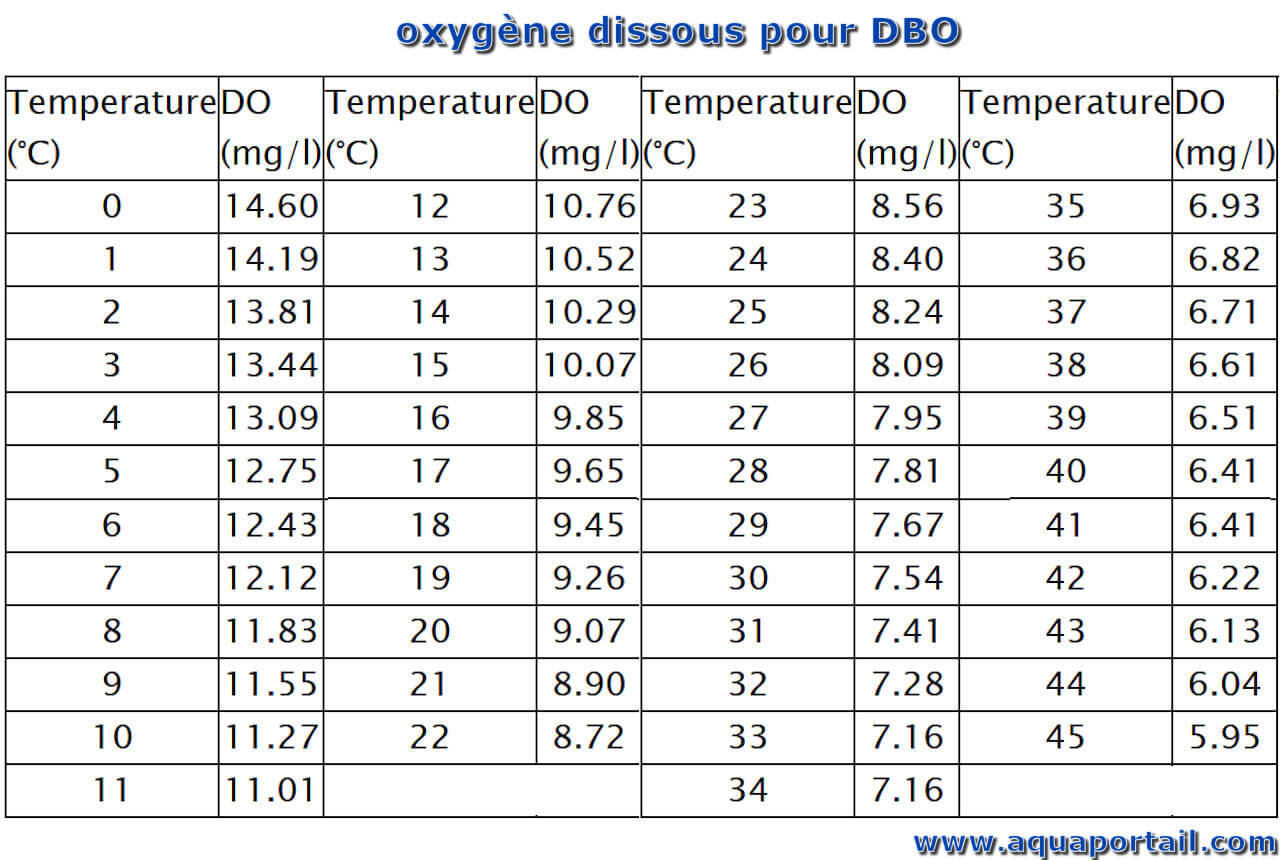
La demande chimique d'oxygène (DCO) est la mesure de la quantité de matière organique qui peut être oxydée par un oxydant chimique fort.
