Rayon ionique
Définition
Le rayon ionique peut être défini comme la taille du rayon d'un ion monoatomique d'un atome, du noyau à l'électron de valence. Le rayon ionique est difficile à mesurer en raison du chevauchement des ions dans une structure en treillis.
Les rayons ioniques des cations et des anions sont toujours plus petits ou plus grands, respectivement, que l'atome parent en raison des changements dans les répulsions électron-électron, et les tendances du rayon ionique sont parallèles à celles de la taille atomique. Une comparaison des dimensions d'atomes ou d'ions qui ont le même nombre d'électrons mais des charges nucléaires différentes, appelée série isoélectronique, montre une corrélation claire entre l'augmentation de la charge nucléaire et la diminution de la taille.
Mesure du rayon ionique :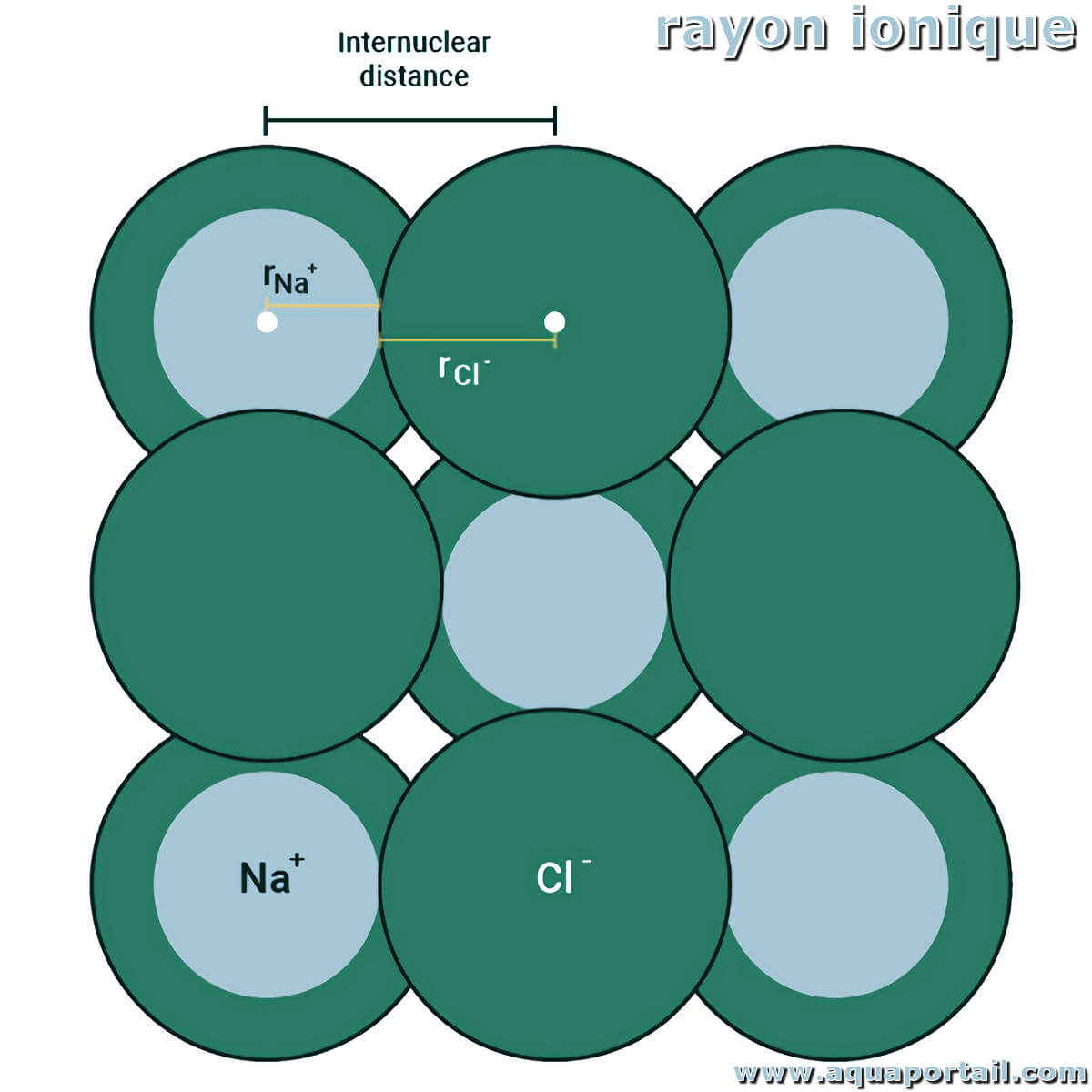
Le rayon ionique est la distance du noyau d'un ion jusqu'à laquelle il a une influence sur son nuage d'électrons. Les ions se forment lorsqu'un atome perd ou gagne des électrons. Lorsqu'un atome perd un électron, il forme un cation et lorsqu'il gagne un électron, il devient un anion.
Explications
En général, le rayon ionique diminue du groupe 1 au groupe 3 car les ions formés ont une charge nucléaire plus élevée, plus de protons, ce qui signifie que les électrons sont rapprochés du noyau et que le rayon ionique est plus petit. Cependant, cela est différent pour les éléments du groupe 5 à 7 car le rayon ionique diminue du groupe 5 au groupe 7. En effet, les ions formés dans le groupe 5 gagneraient 3 électrons et auraient une charge -3 par rapport aux ions du groupe 7 qui gagnent 1 électron. et avoir une charge de -1. La plus grande charge de -3 sur les éléments du groupe 5 signifie qu'il y a une plus grande répulsion des électrons dans les orbitales provoquant un rayon ionique plus grand. Par exemple, l'ion d'azote N3- a un rayon de 146×10-12 m.
En général, dans un groupe, le rayon ionique augmente en taille en raison du nombre croissant de couches d'électrons et du blindage accru de la charge nucléaire signifie que la répulsion des électrons peut être plus grande lorsque plus d'électrons sont ajoutés. Par exemple, en regardant le rayon ionique des ions halogénures descendant le groupe fluorure a un rayon ionique de 464×10-12 m alors que le brome a un rayon ionique de 598×10-12 m.
La détermination du rayon ionique peut être une science difficile car les ions n'existent que dans les structures en treillis et pour mesurer le rayon ionique, nous devons isoler l'ion qui est souvent influencé par la présence d'autres ions. La technique de cristallographie aux rayons X peut être utilisée pour déterminer la longueur des rayons entre les ions et est une technique puissante pour déterminer les distances entre les ions et les liaisons. Lors de la mesure du rayon ionique d'un ion, il est difficile de définir le rayon, par exemple lors de la mesure du rayon du sodium dans le chlorure de sodium, nous pouvons mesurer la longueur de la cellule unitaire cristalline du chlorure de sodium (la distance d'un sodium au chlorure à un autre sodium ion, Na-Cl-Na) qui peut être mesuré comme 564×10-12 m mais si nous voulons estimer la distance entre les noyaux de sodium et de chlorure, nous pouvons prendre la moitié de cette valeur qui est de 282×10-12 m. Cependant, cela ne donne pas la distance entre le noyau et l'électron de valence de l'ion sodium. Grâce à une série d'expériences sur différentes paires d'ions, il est possible de calculer la moyenne du rayon ionique d'un ion.
Synonymes, antonymes
Voir tous les synonymes pour "rayon ionique".0 synonyme (sens proche) pour "rayon ionique".
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à RAYON IONIQUE sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
L'expression RAYON IONIQUE est dans la page 1 des mots en R du lexique du dictionnaire.
Mots en R à proximité
ravinement rayon rayon atomique rayon épineux rayon hydraulique rayon ioniquerayon mou rayonnement ionisant rayonnement non ionisant raz de marée rbcL
En rapport avec "rayon ionique"

Un atome est la plus petite partie d'une substance qui ne peut être décomposée chimiquement.
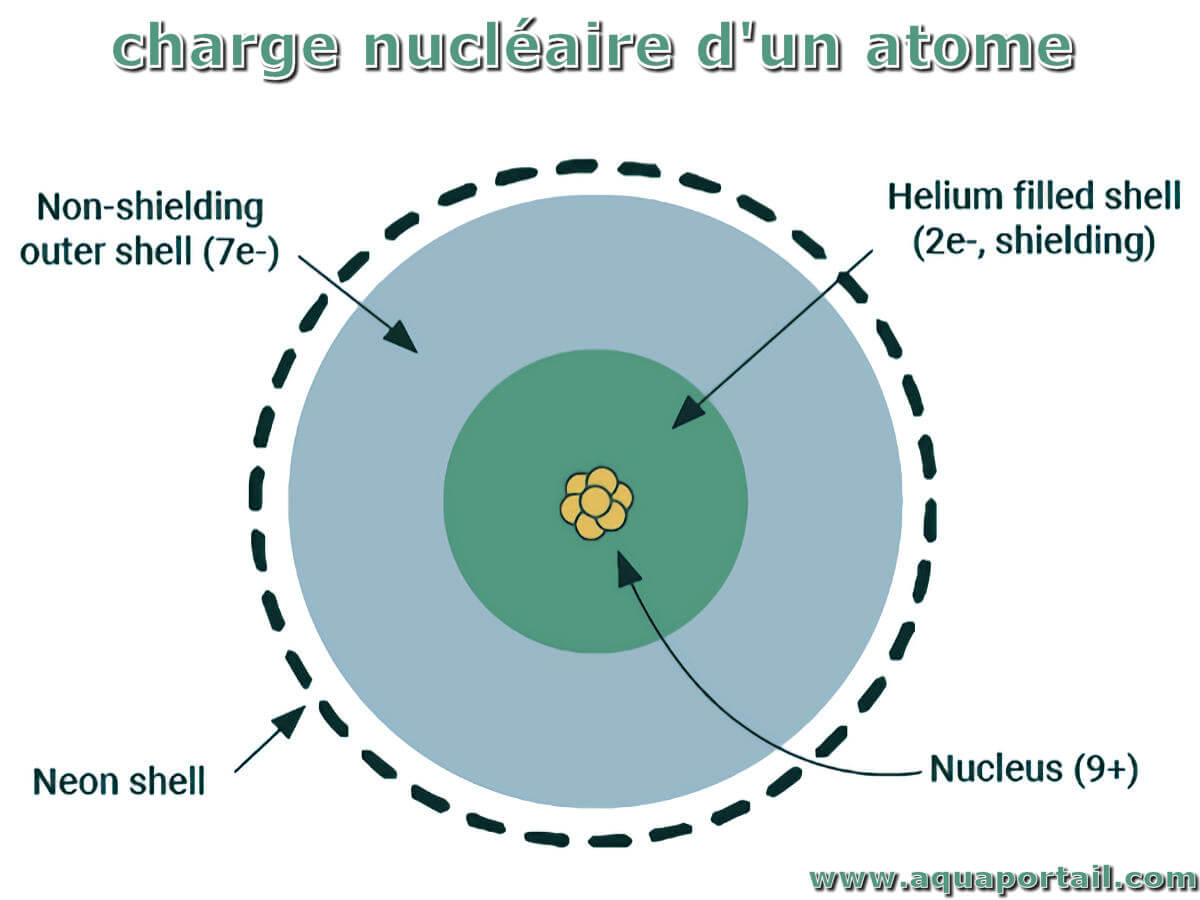
La charge nucléaire est une mesure de l'effet du nombre de protons dans le noyau et de leur capacité à attirer les électrons négatifs en orbite autour...

En physique atomique, une couche électronique, en rapport avec le niveau énergétique d'un atome, peut être considérée comme l'ensemble des orbites suivies...

Le rayon atomique est la distance mesurée entre le centre du noyau et les électrons de valence externes d'un atome.
