Charge nucléaire
Définition
La charge nucléaire est une mesure de l'effet du nombre de protons dans le noyau et de leur capacité à attirer les électrons négatifs en orbite autour du noyau.
La charge nucléaire d'un atome polyélectronique (avec plusieurs couches électroniques) est la mesure de l'effet d'attraction entre les protons du noyau et les électrons de la couche la plus externe.
La charge nucléaire efficace (effective) est l'attraction du noyau vers l'électron de valence en tenant compte du nombre de protons et du nombre d'électrons de la couche interne.
Le principe de charge nucléaire d'un élément :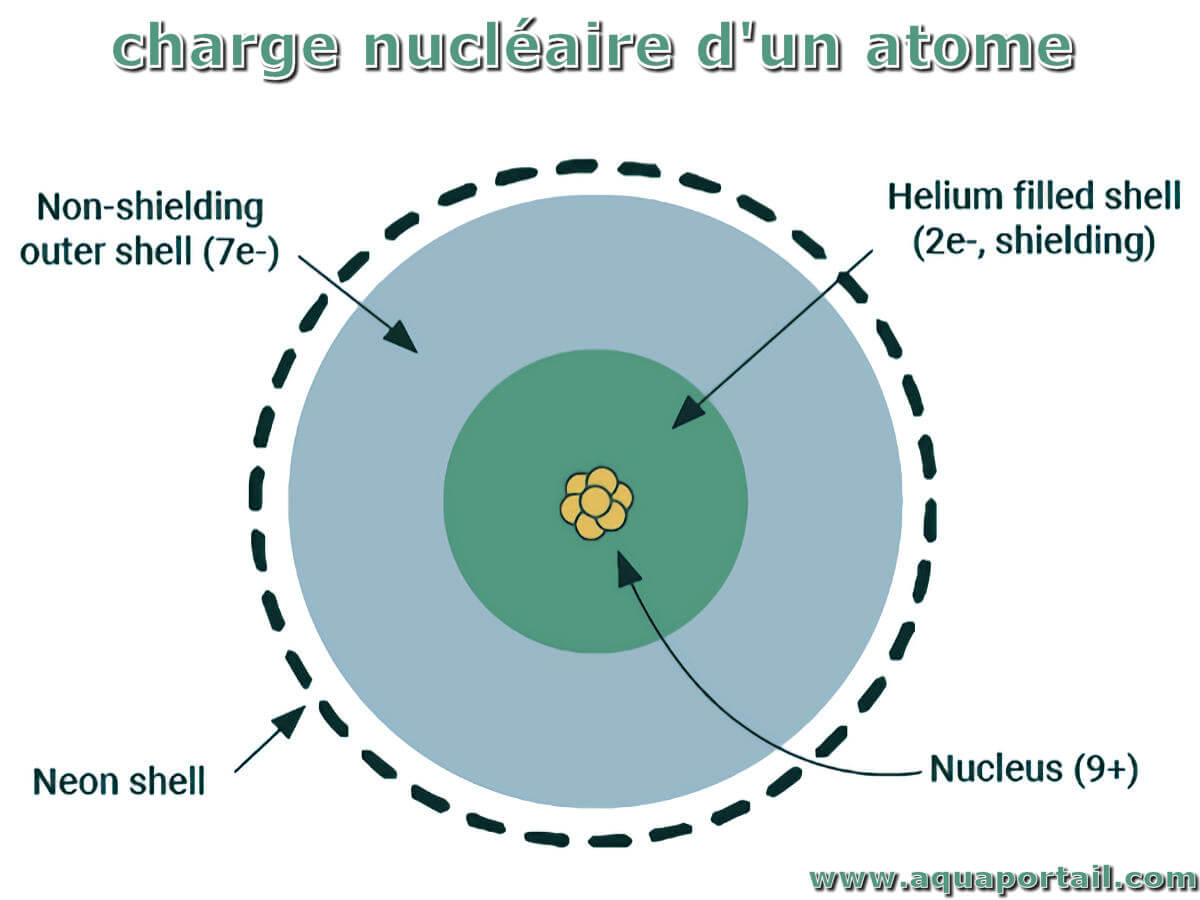
La présence d'électrons sur les couches internes d'un atome polyélectronique réduit l'effet de la charge nucléaire si on se réfère à la charge nucléaire effective (ou efficace) qui est l'effet du noyau subi par l'électron externe de l'atome. Calculer la charge nucléaire effective consiste à soustraire le nombre d'électrons de la couche interne du nombre de protons.
Explications
Les électrons sont attirés par le noyau car ils sont chargés négativement et le noyau contient des protons chargés positivement, mais en même temps, les couches de sous-orbitales d'électrons se repoussent. Il en résulte une attraction variable du noyau sur l'électron externe appelée charge nucléaire.
Nous pouvons calculer la charge nucléaire effective en soustrayant le nombre d'électrons de la couche interne du nombre de protons. Par exemple, le sodium a 10 électrons internes et 11 protons, donc 11–10 lui donne une charge nucléaire effective de +1. Mais en regardant le magnésium qui a également 10 électrons internes mais 12 protons, il a une charge nucléaire effective de +2.
Principe atomique et rayon
Les atomes sont composés d'un noyau, contenant des protons chargés positivement et des neutrons neutres, entourés d'un nuage d'électrons chargés négativement. Ces électrons chargés négativement sont disposés en couches qui forment des couches entourant le noyau. Les éléments de différents groupes du tableau périodique ont des nombres différents d'électrons dans leurs couches les plus externes. Ces électrons externes sont également appelés électrons de valence.
Charge nucléaire efficace (effective)
Les valeurs de charge nucléaire ont été déterminées pour tous les éléments chimiques d'e la table périodique. Ces valeurs sont enregistrées dans des encyclopédies, des manuels scientifiques et des articles de revues scientifiques.
La charge nucléaire est une mesure de la capacité des protons du noyau à attirer les électrons négatifs en orbite autour du noyau. Les électrons sont attirés par le noyau car il est chargé positivement, mais les électrons dans les couches internes peuvent annuler une partie de l'attraction du noyau sur les électrons les plus externes. L'attraction nette sur ces électrons externes est connue sous le nom de charge nucléaire effective.
Le noyau d'un atome contient des particules chargées positivement appelées protons. Les électrons sont attirés par le noyau car ils sont chargés négativement. Cependant, les électrons chargés négativement autour du noyau sont organisés en couches appelées orbitales qui se repoussent et annulent une partie de la charge positive du noyau. Il en résulte une attraction variable du noyau sur les électrons entourant le noyau, appelée charge nucléaire. La présence d'électrons sur les couches internes d'un atome "empêche" l'électron le plus externe de ressentir la pleine charge positive. En raison de la charge variable des électrons dans différentes orbitales, nous nous référons généralement à la charge nucléaire effective, qui est l'effet du noyau subi par l'électron le plus externe de l'atome, en tenant compte de l'effet de protection des électrons internes.
Vous pouvez calculer la charge nucléaire effective si vous connaissez le nombre d'électrons internes et le nombre de protons d'un atome, tous deux disponibles soit dans le tableau périodique, soit dans des ressources en ligne. L'équation pour calculer la charge nucléaire est Zeff = Z - S, où Zeff est la charge nucléaire effective, Z est le nombre de protons et S est le nombre d'électrons internes.
La force exercée sur un électron externe par le noyau peut être déterminée en mesurant la charge du noyau, la charge de l'électron et le rayon entre le noyau et les électrons les plus externes. Nous pouvons ensuite utiliser ces nombres avec la loi de Coloumb pour calculer la force effective du noyau sur un électron. En multipliant la constante de la loi de Coloumb k (9,0 × 109 N × m2 / C2) par q1, la charge nucléaire effective, et q2, la charge de l'électron, et en divisant par le rayon de l'atome au carré, nous pouvons trouver F, qui est la force d'attraction entre le noyau et l'électron extérieur.
Connaître la charge nucléaire effective nous permet de déterminer la quantité d'énergie nécessaire pour éliminer un électron, également connu sous le nom d'ionisation de l'atome. L'énergie d'ionisation est un concept important pour la réactivité des éléments.
Synonymes, antonymes
Voir tous les synonymes pour "charge nucléaire".0 synonyme (sens proche) pour "charge nucléaire".
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à CHARGE NUCLÉAIRE sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
L'expression CHARGE NUCLEAIRE est dans la page 4 des mots en C du lexique du dictionnaire.
Mots en C à proximité
charbon actif charge critique charge électrique charge hydraulique charge négative charge nucléairecharge positive Charles Darwin charognard Charophycées Charophyte
En rapport avec "charge nucléaire"

Un atome est la plus petite partie d'une substance qui ne peut être décomposée chimiquement.

En physique atomique, une couche électronique, en rapport avec le niveau énergétique d'un atome, peut être considérée comme l'ensemble des orbites suivies...
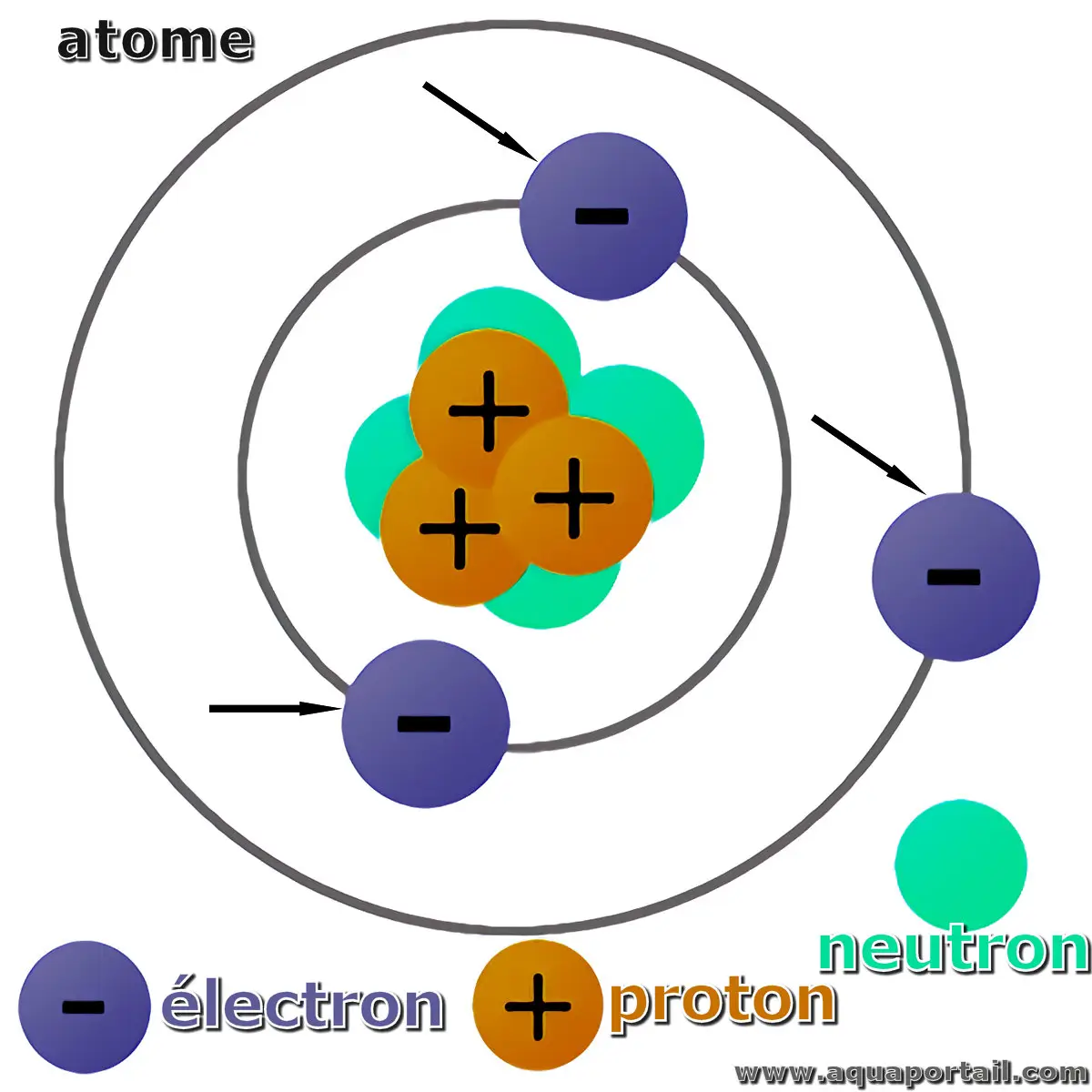
L'électron (e⁻) est une particule élémentaire chargée négativement. Les électrons liés par un atome ou un ion forment sa couche d'électrons.

Le rayon atomique est la distance mesurée entre le centre du noyau et les électrons de valence externes d'un atome.
