Solvant
Définition
Un solvant est une substance, le plus souvent liquide, qui a le pouvoir de dissoudre d'autres substances. Les molécules de solvant exercent leur action en interagissant avec les molécules de soluté et en les entourant. C'est la solvatation.
L'eau est considérée comme un solvant universel en raison du grand nombre de substances sur lesquelles elle peut agir en tant que solvant. Un solvant durable est un solvant inoffensif pour l'environnement.
Un solvant dissout un contaminant avec le temps :
Un solvant approprié pour un contaminant donné permet de diminuer la partie contaminée.
Explications
Les solvants font partie de nombreuses applications : adhésifs, composants dans les peintures, produits pharmaceutiques, pour la fabrication de matériaux synthétiques, etc.
Ils participent "facilement" à une pollution, comme une pollution de l'eau, car certains sont difficilement recyclables. Ces polluants, polluants de l'eau, mais aussi polluants des sols et polluants de l'air, doivent pouvoir entrer dans un processus de recyclage. Cela devrait être une priorité dès la conception.
Classification des solvants
Un solvant est une substance dans laquelle un soluté (un solide, un liquide ou un gaz chimiquement différent) est dilué, ce qui donne une solution; c'est habituellement le composant en plus grande quantité présent dans une solution.
Les solutés polaires seront dissous par les solvants polaires lorsque les interactions électrostatiques entre les dipôles sont établies. Les solvants apolaires dissolvent les substances apolaires par des interactions entre dipôles induits.
- Les solvants polaires : sont des substances dans les molécules desquelles la distribution du nuage électronique est asymétrique; par conséquent, la molécule présente un pôle positif et un pôle négatif séparés d'une certaine distance. Il y a un dipôle permanent. L'exemple classique du solvant polaire est l'eau. Les alcools de faible masse moléculaire appartiennent également à ce type. Les solvants polaires peuvent être subdivisés en :
- Solvants protiques polaires : contiennent une liaison OH ou NH. L'eau (HOH), l'éthanol (CH3-CH2-OH) et l'acide acétique (CH3-C(=O)OH) sont des solvants polaires protiques.
- Solvants aprotiques polaires : solvants polaires qui n'ont pas de liaisons OH ou NH. Ce type de solvant ne donne ni n'accepte de protons. L'acétone (CH3-C(=O)-CH3), l'acétonitrile, le diméthylformamide ou le THF (tétra-hydro-furane) sont des solvants aprotiques polaires.
- Les solvants apolaires : en général, ce sont des substances de type organique et dans les molécules desquelles la distribution du nuage électronique est symétrique; par conséquent, ces substances manquent de pôle positif et négatif dans leurs molécules. Ils ne peuvent pas être considérés comme des dipôles permanents.
Cela n'implique pas que certains de ses liens sont polaires. Tout dépendra de la géométrie de ses molécules. Si les moments dipolaires individuels de leurs liaisons sont compensés, la molécule sera, dans son ensemble, apolaire. Certains solvants de ce type sont : l'éther éthylique, le benzène, le toluène, le xylène, les cétones, l'hexane, le cyclohexane, le tétrachlorure de carbone est celui qui se dissout ou va se dissoudre.
Le chloroforme, en revanche, possède un moment dipolaire considérable du fait que le fait d'avoir trois chlores dans sa molécule électronégative fait que le carbone acquiert une charge positive partielle et l'hydrogène une charge partielle négative, ce qui lui confère une certaine polarité. Un cas particulier est celui des liquides fluorés, qui se comportent comme des solvants plus apolaires que les solvants organiques classiques.
Solvants organiques
Les solvants les plus largement utilisés aujourd'hui sont les solvants organiques, des composés organiques volatils utilisés seuls ou en combinaison avec d'autres agents, sans modification chimique, pour dissoudre les matières premières, les déchets ou les matériaux.
Ils sont aussi utilisés comme agent de nettoyage pour dissoudre la saleté, soit en tant que solvant, soit en tant que milieu de dispersion, soit en tant que modificateur de viscosité, soit en tant qu'agent tensio-actif.
L'utilisation de ces solvants libère des composés organiques volatils (COV) dans l'atmosphère, qui ont des problèmes importants pour l'environnement. Certains COV provoquent la dégradation de la couche d'ozone, comme le 1,1,1-trichloroéthane, le tétrachlorure de carbone, les CFC et les HCFC.
Parmi les solvants organiques les plus remarquables, on trouve le méthanol, l'éthanol, l'acétone, le chloroforme, le toluène ou le xylène, entre autres.
L'eau utilisée comme solvant
L'eau H2O, appelée solvant universel, est le meilleur choix en tant que solvant, d'un point de vue environnemental, car elle n'est ni inflammable, ni toxique, ni contaminante, bien qu'elle présente l'inconvénient d'avoir une faible solubilité avec les résines.
Le moment dipolaire élevé de l'eau et sa facilité à former des ponts hydrogène font de l'eau un excellent solvant. Une molécule ou un ion est soluble dans l'eau s'il peut interagir avec les molécules d'eau par des liaisons hydrogène ou des interactions de type ion-dipôle.
La solubilité des ions dans l'eau avec des anions ayant des atomes d'oxygène peut former des liaisons hydrogène, puisque l'oxygène agit comme un accepteur de ceux-ci.
De plus, l'attraction de l'anion sur le dipôle d'eau doit être prise en compte. Il en va de même pour Cl- ou F-, qui ont des paires d'électrons solitaires et peuvent agir comme accepteurs de ponts d'hydrogène. D'autre part, les cations tels que Na+, K+, Ca++ ou Mg++ sont entourés de molécules d'eau auxquelles ils sont liés par des interactions de type ion-dipole; les atomes d'oxygène sont orientés vers le cation.
Lorsque la température et la pression augmentent, les propriétés de l'eau varient. Par exemple, la constante diélectrique diminue et devient plus semblable à celle des solvants organiques, ce qui aggrave la solubilisation des substances ioniques.
À haute température et pression, il dissout les composés organiques, les processus se déroulant en phase homogène et avec lui la séparation du soluté est facilitée (par refroidissement), en pouvant éliminer les résidus.
Solvants néotériques
Les solvants néotériques peuvent être obtenus à partir de matières premières renouvelables, étant une alternative aux solvants dérivés du pétrole, dont un exemple sont ceux dérivés de la biomasse. Ces solvants néotériques sont : les liquides fluorés, les liquides ioniques, les fluides supercritiques.
La plupart de ces solvants ont une faible toxicité, une faible volatilité, ne sont pas corrosifs ou cancérigènes. En outre, beaucoup d'entre eux sont obtenus à partir de déchets végétaux, ce qui les rend économiquement compétitifs.
Les solvants néotériques ou alternatifs sont des composés avec lesquels il est envisagé de remplacer ceux déjà connus comme solvants classiques dans leur utilisation industrielle, en raison de leur importance pour la protection de l'environnement, en raison de leur possibilité de réutilisation, de recyclage et de leur toxicité faible ou nulle.
Voir aussi l'activité ionique.
Solvants contre contaminants
Les contaminants solubles sont des contaminants liquides (huile, par exemple) qui se mélangeront et seront dilués par un solvant et des contaminants solides (sels, par exemple) qui peuvent être dissous par un solvant.
En choisissant un solvant approprié pour un contaminant donné et en immergeant une partie contaminée dans un récipient de ce solvant, alors, sans agitation, le solvant commencera à faire son travail en mélangeant et en diluant ou en dissolvant le contaminant avec lequel il entre en contact.
Bientôt, cependant, le solvant en contact avec le contaminant devient contaminé par le contaminant ou saturé de celui-ci. Une fois cela arrivé, le "nettoyage" s'arrête ! Une bonne analogie peut être trouvée dans n'importe quelle cuisine.
Tout le monde sait que vous pouvez mettre un plat sale dans de l'eau, même de l'eau savonneuse, mais si vous laissez une nuit, aucune trace de résidu ne sera enlevée si vous n'ajoutez pas un peu d'huile de coude. Un trempage de nuit ne supprime pas, malheureusement, totalement les contaminants.
Pour que le plat soit totalement propre, il faut utiliser une éponge, un torchon ou tout ce que vous utilisez pour laver la vaisselle et, bien sûr, terminer le travail nécessite un rinçage.
Le nettoyage des pièces n'est pas vraiment différent du lavage de vaisselle. Une fois que cette couche saturée de solvant se développe, la seule façon de poursuivre le processus de nettoyage est de remplacer le solvant saturé par du solvant frais.
Les nettoyeurs de pièces font ceci en utilisant des pulvérisateurs, une agitation partielle, une turbulation, un bullage, un brossage (occasionnellement) et d'autres moyens de fournir une assistance mécanique. Le but de n'importe quel moyen mécanique est d'agiter le solvant de sorte que le solvant usé soit remplacé par du solvant frais.
Synonymes, antonymes
Voir tous les synonymes pour "solvant".1 synonyme (sens proche) de "solvant" :
- dissolvant
1 antonyme (sens contraire) :
Les mots ou les expressions apparentés à SOLVANT sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
Le mot SOLVANT est dans la page 3 des mots en S du lexique du dictionnaire.
Mots en S à proximité
solution neutre solution normale solution saline solution tampon solution tamponnée solvantsolvant organique solvatation soma somatiquesomatocoele
En rapport avec "solvant"

En chimie, le soluté est un des deux composants d'une solution, avec le solvant. La substance dissolvante est appelée un solvant tandis que la substance...
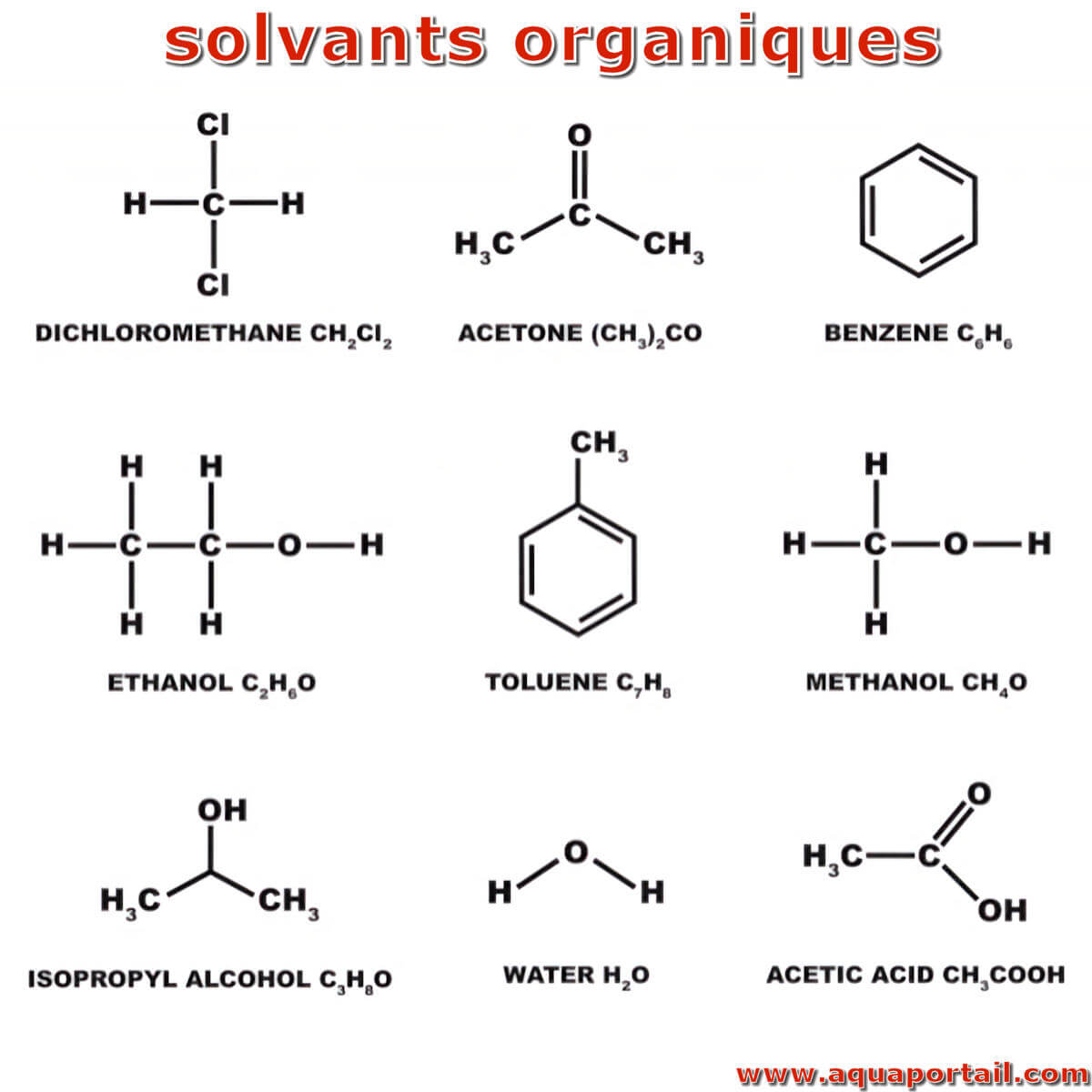
Le solvant organique est une substance à base de carbone capable de dissoudre ou de disperser une ou plusieurs autres substances.

La solvatation est le processus de formation d'interactions entre des molécules d'un solvant avec des molécules ou des ions d'un soluté.

Un contaminant qualifie un élément organique ou chimique, ou une substance contenue dans l'environnement (air, eau, sédiments, etc.
