Zwitterion
Définition
Un zwitterion est un composé chimique moléculaire neutre, une molécule ou un ion ayant des groupes fonctionnels séparés chargés positivement et négativement. Les zwitterions sont simultanément chargés électriquement et électriquement neutres. Ils contiennent des charges positives et négatives, mais la charge nette sur la molécule est nulle.
Un zwitterion :
Un zwitterion est un composé qui n'a pas de charge électrique globale, mais comprend différentes sections chargées positivement et négativement. Le zwitterion a, en nombre égal, des charges électriques formelles d'une unité et de signes opposés.
Explications
Le zwitterion est un ion possédant à la fois des charges électriques positives et négatives qui s'annulent. Par conséquent, les zwitterions sont pour la plupart électriquement neutres (la charge formelle nette est généralement nulle). Les zwitterions sont parfois appelés "sels internes" ou "ions dipolaires".
Les aminoacides sont le meilleur exemple de zwitterion car ils contiennent un groupe amine (basique) et un groupe carboxylique (acide) qui s'annule électriquement.
Le zwitterion est la forme d'acides aminés la plus biologiquement pertinente car c'est leur forme la plus abondante dans les organismes vivants : ils sont synthétisés sous la forme zwitterionique et sont essentiellement toujours sous cette forme à pH neutre.
Un zwitterion est une molécule ayant une charge formelle nette de zéro, mais des charges formelles négatives et positives sur les atomes individuels au sein de sa structure. Les atomes chargés doivent être reliés par une ou plusieurs liaisons covalentes.
Le transfert de protons permet à la glycine d'exister sous des formes neutres, ioniques et zwitterioniques. L'acétone a des contributeurs de résonance neutres (significatifs) et zwitterioniques (non significatifs).
Réactions thermiques à travers les zwitterions
Les zwitterions peuvent être utilisés comme matières premières dans des réactions de cyclopropanation ou peuvent être générés in situ dans les mélanges réactionnels (généralement dans des conditions basiques à partir d'un sel d'onium).
Contrairement à la nature électrophile de la plupart des cétocarbènes et des cétocarbénoïdes liés aux métaux, un comportement nucléophile est généralement observé dans les ylures de cétocarbénoïdes, en conséquence de la présence d'un atome de carbone anionique conjugué à un carbonyle lié à un hétéroatome d'onium. En conséquence, les alcènes pauvres en électrons peuvent être efficacement cyclopropanés à l'aide d'ylures de cétocarbénoïdes sans avoir besoin d'un catalyseur.
Un mécanisme de réaction par étapes impliquant un intermédiaire zwitterionique est la voie la plus courante dans les réactions de cyclopropanation d'ylures avec des alcènes déficients en électrons.
Point isoionique et titrage des acides α-aminés
Un zwitterion a un ion carboxylate négatif et un ion ammonium. Le pH auquel la concentration du zwitterion prédomine est le point isoionique. Pour les acides aminés neutres, le point isoionique se situe à mi-chemin entre les valeurs de pKα du groupe acide carboxylique et du groupe ammonium.
Pour les acides aminés neutres, le point isoionique est proche de 7. Les acides aminés acides ont des points isoioniques inférieurs à 7. Pour les acides aminés acides, le groupe acide carboxylique de la chaîne latérale de l'aspartate et de l'acide glutamique existe sous forme d'ion carboxylate à un pH proche de 7. Pour protoner cet ion carboxylate, la solution doit être acide.
Les acides aminés basiques ont des points isoioniques supérieurs à 7. Pour les acides aminés basiques, le groupe fonctionnel basique de la chaîne latérale a tendance à être protoné à un pH proche de la neutralité. Ainsi, il existe deux ions ammonium et un seul ion carboxylate. Afin d'éliminer un proton de l'ion ammonium, la solution doit être basique.
Ampholytes et zwitterions
Les ampholytes et les zwitterions sont des molécules avec au moins deux valeurs de pKa, dont au moins une est acide et au moins une est basique.La distribution des espèces pour le clioquinol (un ampholyte) et l'ampicilline (un zwitterion) sont différentes.
Les deux molécules ont deux valeurs de pKa. Dans le clioquinol, le pKa de base est inférieur au pKa acide, donc à des valeurs de pH entre les valeurs de pKa, la molécule est neutre. Cependant, le pKa acide de l'ampicilline est inférieur au pKa de base et la molécule est chargée sur toute l'échelle de pH. Les ampholytes sont les plus lipophiles et les moins solubles sous leur forme neutre.
Cependant, les zwitterions sont toujours chargés; ils sont rarement lipophiles et ils sont souvent solubles dans l'eau à n'importe quel pH. Les équations suivantes sont utilisées pour l'ionisation et la distribution des espèces d'ampholytes et de zwitterions diprotonés. Puisqu'il y a deux ionisations, les constantes d'ionisation doivent être étiquetées Ka1 et Ka2.
Synonymes, antonymes
Voir tous les synonymes pour "zwitterion".2 synonymes (sens proche) de "zwitterion" :
- hybride chimique
- ion dipolaire
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à ZWITTERION sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
Le mot ZWITTERION est dans la page 1 des mots en Z du lexique du dictionnaire.
Mots en Z à proximité
zootomie zooxanthelle zooxanthellés zoozygote zostère zwitterionzygapophyse zygomatique zygomorphe zygomycète zygophylle
En rapport avec "zwitterion"
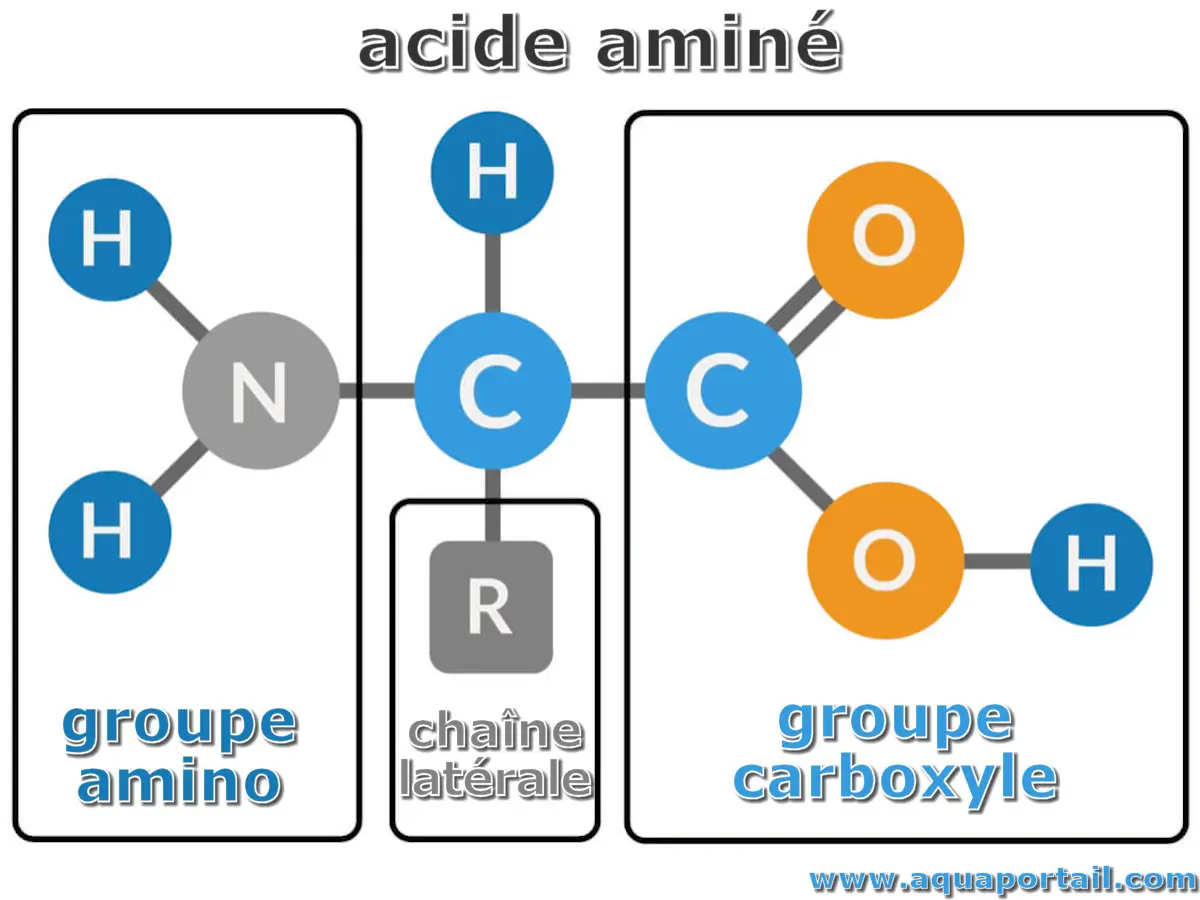
Un acide aminé est la molécule fondamentale qui sert de composant aux protéines. Une protéine est constituée d'une ou plusieurs chaînes d'acides aminés...

Un aminoacide, ou acide aminé, exprime les qualités d'un composé organique contenant à la fois le groupe amino (NH₂ azoté ou -NR₂ substitué) et le groupe...

Un ampholyte est une molécule contenant à la fois une fonctionnalité acide et une fonctionnalité basique.
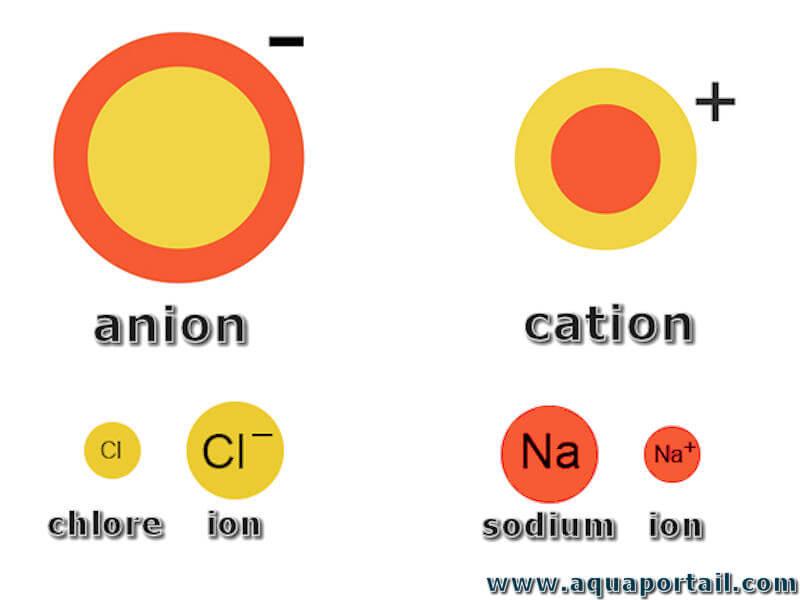
Un anion possède plus d'électrons que de protons, ce qui lui confère une charge nette négative.
