Oxyanion
Définition
Un oxyanion (oxoanion) est un ion composé d'atomes d'oxygène O et d'un autre élément. Les oxyanions peuvent être classés selon leur structure et leur composition, avec une distinction faite entre les oxyanions monomères et polymères. Un grand nombre d'éléments chimiques forment des oxyanions, comme les ions sulfate et carbonate. L'oxyanion le plus connu est probablement l'ADN. La famille d'oxyanions la plus étendue est celle des polyoxomolybdates.
Les oxyanions du chlore :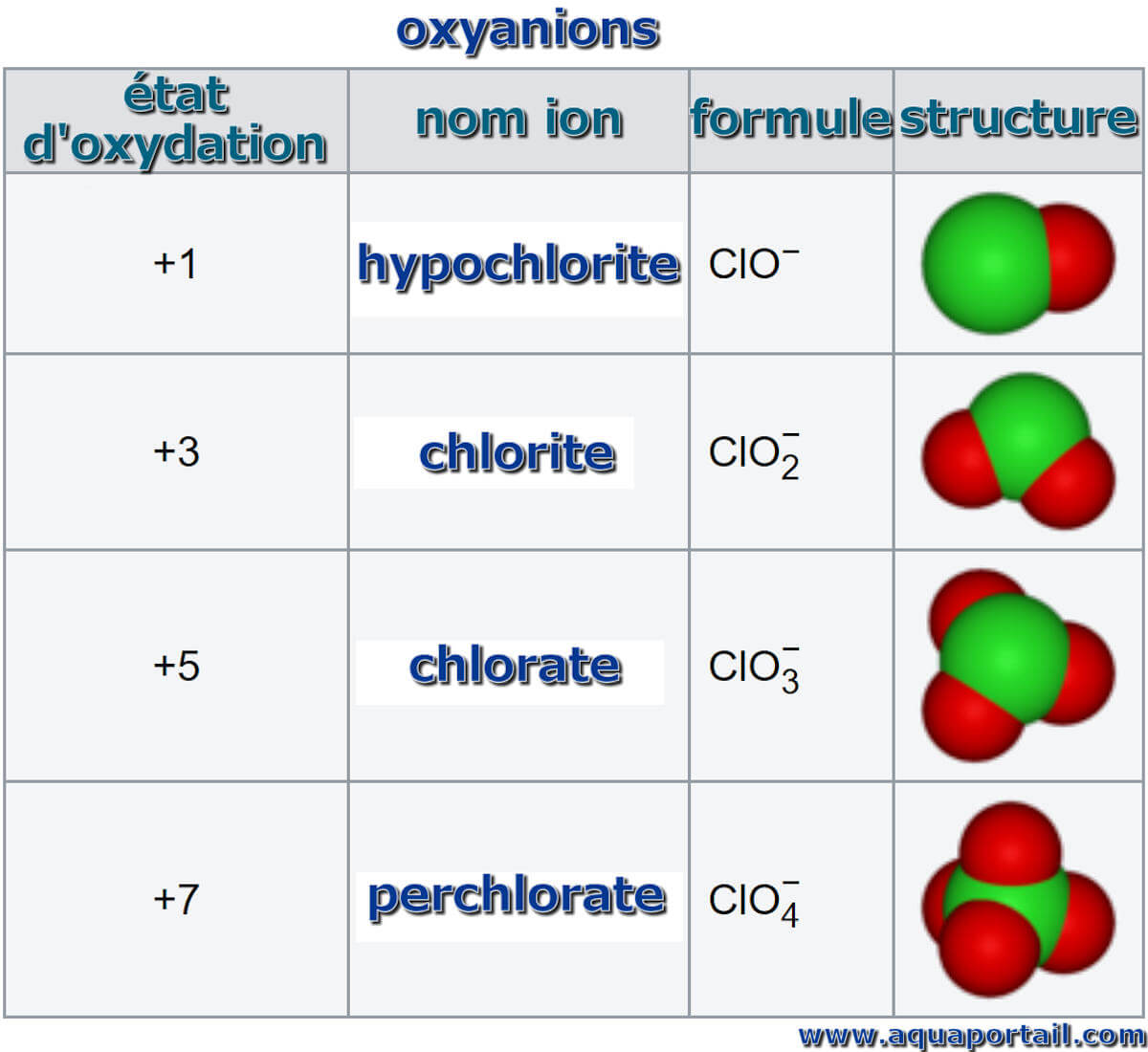
Le chlore a quatre oxyanions possibles : hypochlorite, chlorite, chlorate, perchlorate. La différence entre chaque est le nombre d'ions oxygène.
Explications et classification
La formule chimique générale d'un oxyanion est : AxOyz-, avec A un élément chimique quelconque (sauf le fluor). L'oxyacide correspondant à un oxyanion a pour formule : HzAxOy. Voir aussi un ion polyatomique.
Les oxyanions portent chacun leur propre nom, avec un suffixe indiquant l'état d'oxydation de l'élément central. Les anions contenant de l'oxygène (oxyanions) sont tous nommés avec une terminaison -ate ou -ite. L'oxyanion le plus courant d'un élément donne la terminaison -ate. Pour d'autres oxyanions, les états d'oxydation peuvent être différents de ceux-ci, mais l'ordre des préfixes et des suffixes reste le même. Les oxyanions et leurs oxyacides conjugués sont nommés en fonction de l'état d'oxydation de l'atome non oxygène.
Le nitrate (NO3-), le nitrite (NO2-), le sulfite (SO32-), le sulfate (SO42-) et l'hypochlorite (ClO-) sont tous des oxyanions.
Les oxyanions ont des rôles environnementaux très importants. On peut citer le cas de la prévalence des espèces d'arsenic dans les zones affectées par l'arsenic sous forme d'oxyanions. La surface de l'eau présente normalement des conditions oxydantes et dans ces conditions, les espèces d'arsenic ont tendance à prédominer sous forme d'arsenic pentavalent, conservant ses formes oxyanioniques H2AsO4- et HAsO42-.
Oxyanions monomères
Les oxyanions monomères sont formés par une liaison covalente d'un élément central avec les atomes d'oxygène environnants. Le nombre d'atomes d'oxygène et la charge de l'anion sont déterminés par l'état d'oxydation de l'élément central et sa position dans le tableau périodique.
Par exemple, les éléments de la deuxième période sont limités à un nombre de coordination maximum de 4. Cependant, aucun de ces éléments ne forme des oxyanions avec un nombre de coordination aussi élevé. Plus commun est le numéro de coordination 3, comme dans le carbonate (CO32−) et le nitrate (NO3-). Les deux oxyanions (avec le carbone et l'azote comme élément central, respectivement) possèdent une structure plane trigonale.
Les éléments de la troisième période sont beaucoup plus flexibles pour former des oxyanions, et ils existent également sous des formes polymères. Lorsque l'élément en question a son état d'oxydation le plus abondant, des oxyanions tétraédriques se forment. Pour le silicium, le phosphore, le soufre et le chlore, il s'agit respectivement de silicate (SiO44-), de phosphate (PO43-), de sulfate (SO42-) et de perchlorate (ClO4-).
Ces oxyanions viennent dans d'innombrables sels et se trouvent également dans la nature sous forme minérale. Des états d'oxydation inférieurs de l'élément central conduisent à d'autres oxyanions. La géométrie moléculaire change avec un état d'oxydation modifié. Cela est dû au fait qu'avec l'augmentation du nombre d'oxydation, le nombre de paires isolées diminue.
Oxyanions polymères
Plusieurs métaux de transition, ainsi que certains non-métaux (en particulier le phosphore et le soufre), forment des oxyanions polymères. Dans ce cas, un atome d'oxygène agit comme un ligand pontant entre les centres métalliques, comme dans l'anion dichromate, pyrophosphate et pyrosulfate. Lorsque cela intervient à plusieurs reprises, des chaînes ou des structures annulaires peuvent se former.
Des exemples de ces types de structures sont les polyphosphates et les inosilicates. Un exemple extrême en cristallographie sont les tectosilicates (comme le quartz), où le silicium intégré dans un réseau d'oxygène. Les quatre atomes d'oxygène environnants servent ici de ligand de pontage. Les métavanadates forment des structures à longue chaîne, comme dans le métavanadate d'ammonium. La structure de coordination entourant le vanadium est tétraédrique.
Les structures annulaires peuvent être considérées comme des chaînes de polyoxoanions dont les extrémités sont connectées les unes aux autres. Le triphosphate cyclique (P3O93-) en est un exemple.
Les oxyanions octaédriques sont présents dans les métaux de transition plus gros. Ceux-ci peuvent exister sous forme monomérique, mais les amas polymériques tridimensionnels - appelés polyoxométalates - sont plus courants. Ces clusters peuvent être compris comme constitués de blocs de construction octaédriques avec des côtés communs. La formation de côtés communs présente deux avantages : premièrement, la tension de pontage provoquée par les atomes d'oxygène de pontage est réduite, et deuxièmement, la densité de charge de l'anion est réduite. Un exemple typique est l'anion polymolybdate. La formation de polyoxométalates peut être considérée comme une hypothétique réaction de condensation des oxyanions monomères.
Une réaction similaire existe avec des solutions aqueuses de tungstates. Lorsqu'une solution de tungstate de sodium est traitée avec du chlorure d'hydrogène, les polytungstates jaunes précipitent.
Propriétés acido-basiques
La plupart des oxyanions sont des bases faibles qui peuvent être protonées assez facilement en acides ou sels acides correspondants. Par exemple, l'anion phosphate peut être protoné en acide phosphorique par étapes successives : (PO43- + 3 H+ ⇌ HPO42- + 2 H+ ⇌ H2PO4- + H+ ⇌ H3PO4.
La mesure dans laquelle ces réactions se déroulent est déterminée par les constantes de dissociation (pK a) et le pH. L'adénosine monophosphate a une valeur p K a de 6,21 et sera donc protonée à pH 7 pendant 10 %. Une force motrice importante dans ces réactions est la neutralisation de la charge. En revanche, les oxyanions tels que le perchlorate et le permanganate sont particulièrement difficiles à protoner, même avec des acides forts tels que l'acide sulfurique.
Synonymes, antonymes
Voir tous les synonymes pour "oxyanion".1 synonyme (sens proche) de "oxyanion" :
- oxoanion
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à OXYANION sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
Le mot OXYANION est dans la page 3 des mots en O du lexique du dictionnaire.
En rapport avec "oxyanion"
Un anion possède plus d'électrons que de protons, ce qui lui confère une charge nette négative.
Ce qui est de nature anionique mentionne une charge négative, au contraire de cationique (charge positive).
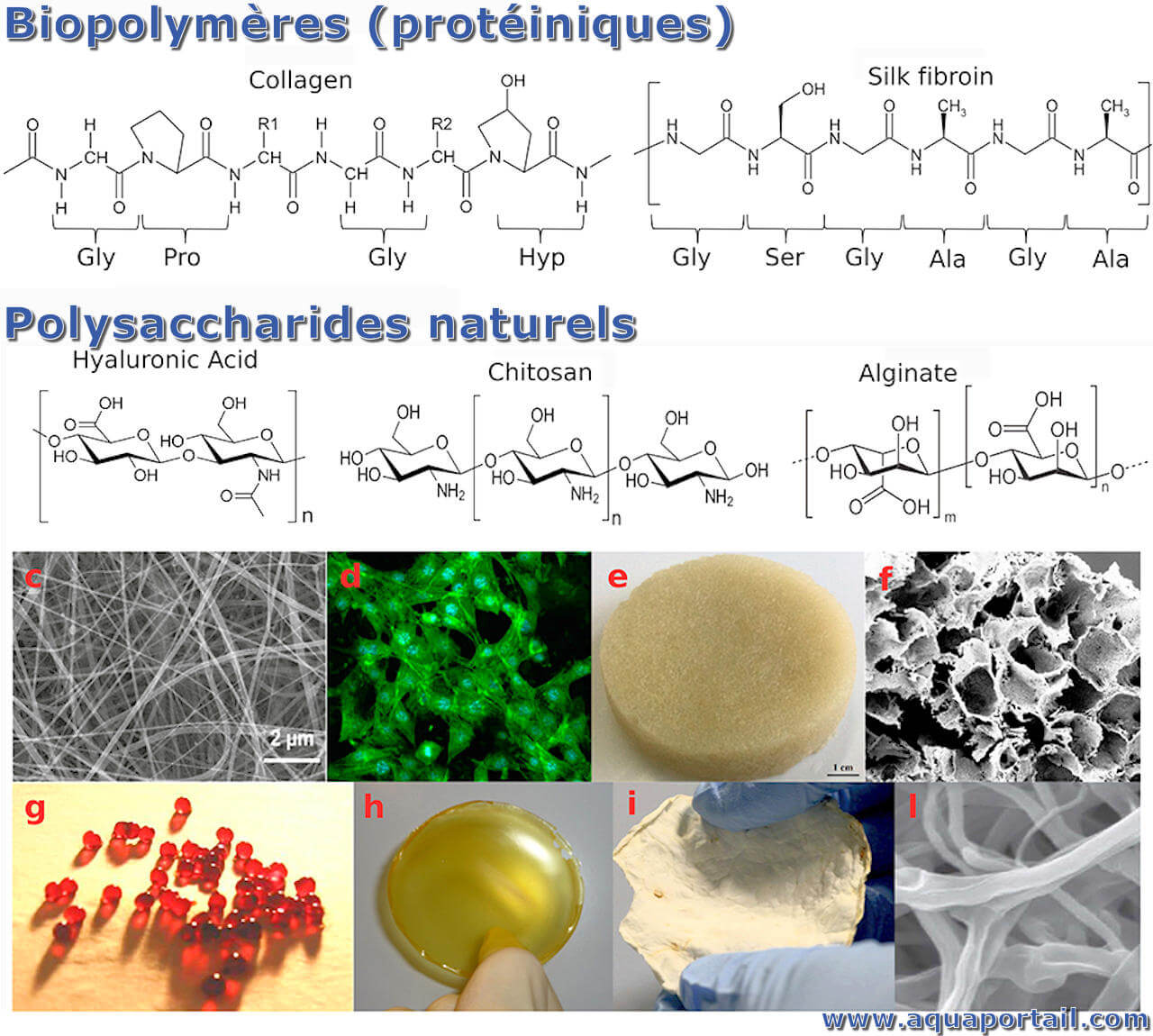
Un biopolymère est une macromolécule biologique qui résulte de la polymérisation de molécules plus simples ou monomères.

Un carbanion est une contraction d'un carbone sur un anion, avec une charge négative sur le carbone.
