Neurotrophique
Définition
Un facteur neurotrophique (neurotrophe) est défini comme une protéine soluble endogène régulant la survie, la croissance, la plasticité morphologique et la synthèse, ou la synthèse de protéines pour les fonctions différenciées des neurones.
Le facteur neurotrophique dérivé du cerveau (tropomyosine) :
Schéma proposant les rôles à multiples facettes du facteur neurotrophique dérivé du cerveau (FNDC)-tropomyosine liée à la signalisation de la kinase B (TrkB) dans la myélinisation du système nerveux central (SNC). Flèches en pointillés : résultat hypothétique de la signalisation TrkB; flèches pleines : mécanisme rapporté et résultat de la signalisation TrkB.
Explications
Dans le schéma neurotrophique ci-dessus : (a) Le processus de myélinisation nécessite que la cellule progénitrice oligodendrocyte (OPC) entre en contact avec l'axone et se différencie en oligodendrocyte mature qui enveloppe l'axone de myéline. Le déclenchement du potentiel d'action (AP) par les neurones actifs entraîne la libération de FNDC le long de l'axone. La signalisation FNDC-TrkB (b) pourrait influencer la survie et la différenciation des OPC dans le développement et après une lésion de la myéline et (c) favorise la myélinisation dépendante de l'activité en modulant la neurotransmission glutamatergique (NMDAR; AMPAR). Il est bien établi que (d) la signalisation FNDC-TrkB via la kinase extracellulaire 1/2 (Erk1/2) favorise la synthèse des protéines de myéline et cela influence l'épaisseur de la gaine de myéline. Les mécanismes moléculaires qui sous-tendent cet effet ne sont pas connus et on suppose que la cascade FNDC-TrkB-Erk entraîne une activation transcriptionnelle contrôlant l'expression de la protéine de myéline.
Facteur neurotrophique du cerveau
Le facteur neurotrophique dérivé du cerveau (FNDC) joue un rôle vital dans le développement neuronal et la plasticité dans la santé et la maladie. Des études récentes utilisant des souris mutantes pour manipuler sélectivement la signalisation du FNDC dans les types de cellules souhaités, en combinaison avec des modèles animaux de maladie démyélinisante, ont démontré que le FNDC non seulement potentialise la myélinisation normale du système nerveux central au cours du développement, mais améliore la récupération après une lésion de la myéline.
Cependant, les mécanismes précis par lesquels le facteur neurotrophique dérivé du cerveau améliore la myélinisation dans le développement et la réparation ne sont pas clairs. Certains des progrès récents sont réalisés dans la compréhension de l'influence que le FNDC exerce sur le processus de myélinisation pendant le développement et après une blessure.
Le processus de myélinisation est étroitement contrôlé par des facteurs de transcription clés qui réagissent à une gamme de signaux extracellulaires, notamment des molécules et des ligands sécrétés ou exprimés à la surface des axones. Des preuves significatives impliquent le facteur neurotrophique dérivé du cerveau (FNDC) neurotrophine en tant que molécule pro-myélinisante clé. Une compréhension précise des mécanismes cellulaires et moléculaires par lesquels le FNDC engage des cascades de signalisation intracellulaires essentielles à la myélinisation a le potentiel d'éclairer de nouvelles approches thérapeutiques pour promouvoir la remyélinisation.
Cellules neurotrophiques
Les cellules neurotrophiques sont des neurotrophines, une famille de protéines qui induisent la survie, le développement et le fonctionnement des neurones. Elles appartiennent à une classe de facteurs de croissance, des protéines sécrétées qui peuvent signaler à des cellules particulières de survivre, de se différencier ou de se développer.
Effets neurotrophiques
Les effets neurotrophiques peuvent être considérés comme une stratégie thérapeutique destinée à augmenter la prolifération, la différenciation, la croissance et la régénération, tandis que les effets neuroprotecteurs ralentissent ou arrêtent la progression de l'atrophie neuronale ou de la mort cellulaire après l'apparition de la maladie ou le déclin clinique.
Hypothèse neurotrophique
L'hypothèse neurotrophique fournit une explication de la façon dont les champs cibles influencent la taille des populations neuronales qui les innervent. Cette hypothèse est née de travaux sur le facteur de croissance nerveuse (NGF), le membre fondateur de la famille des neurotrophines des protéines sécrétées.
Utilisation de facteurs neurotrophiques
L'utilisation de facteurs neurotrophiques comme agents thérapeutiques est une nouvelle stratégie pour restaurer et maintenir la fonction neuronale lors de troubles neurodégénératifs tels que la sclérose en plaques. Les réponses immunitaires innées et adaptatives contribuent à la pathologie des troubles neurodégénératifs.
Facteur neurotrophique ciliaire
Le facteur neurotrophique ciliaire (CNTF) appartient à une famille de cytokines, dont le facteur inhibiteur de la leucémie (LIF) et l'interleukine-6, qui maintiennent la survie des neurones ciliaires ainsi que des motoneurones. Le CNTF est produit par les cellules de Schwann, le tissu oculaire et dans le SNC principalement par les astrocytes.
Autres facteurs neurotrophiques
Les fonctions des facteurs neurotrophiques extérieurs au système nerveux ont été décrites. Le facteur neurotrophique dérivé de la glie (FNDC), membre de la superfamille des facteurs de croissance transformants β, est une protéine de 18 kDa qui se lie à l'une des deux sous-unités de récepteur, GFRα-1 et GFRα-2. Ce complexe ligand-récepteur s'associe alors à Ret, un récepteur tyrosine kinase qui, comme les récepteurs Trk, subit une dimérisation et devient catalytiquement actif. Les protéines adaptatrices de liaison à la phosphotyrosine telles que Shc se lient ensuite au récepteur Ret et interviennent dans les cascades de signalisation en aval telles que la voie MAP kinase. Des études in vitro et in vivo ont établi le FNDC comme un puissant facteur trophique pour les neurones dopaminergiques. L'administration exogène de FNDC empêche la mort des cellules des motoneurones et réduit l'atrophie du système dopaminergique nigro-strié et est donc considérée comme un agent thérapeutique potentiel pour la maladie de Parkinson (MP).
Les cytokines sont un groupe hétérogène de médiateurs polypeptidiques associés à l'activation du système immunitaire et aux réponses inflammatoires à propriétés trophiques. Ils sont étudiés en tant qu'agents thérapeutiques pour le traitement de divers troubles neurodégénératifs ainsi que des lésions nerveuses. Le facteur neurotrophique ciliaire (CNTF) appartient à une famille de cytokines, dont le facteur inhibiteur de la leucémie (LIF) et l'interleukine-6, qui maintiennent la survie des neurones ciliaires ainsi que des motoneurones. Le CNTF est produit par les cellules de Schwann, le tissu oculaire et dans le SNC principalement par les astrocytes. Le récepteur CNTFα signale à travers la kinase soluble, JAK, et le transducteur de signal et l'activateur de la voie de signalisation de la transcription-3 et conduit à l'activation de MAPK et JNK, entraînant des effets de prosurvie des cellules cibles.
Le CNTF favorise la survie des neurones moteurs in vitro et chez les animaux nouveau-nés après axotomie et il a été démontré qu'il augmente la myélinisation des axones en régénération. Les souris déficientes en CNTF souffrent d'une dégénérescence et d'une atrophie légères et progressives des motoneurones et ont été associées à la sclérose latérale amyotrophique (SLA), à la sclérose en plaques et à plusieurs modèles de la maladie de Huntington (HD). Le LIF est un polypeptide de 20 kDa qui utilise des voies de signalisation communes similaires au CNTF avec des actions pro-survie sur les oligodendrocytes, les motoneurones et les cellules précurseurs hématopoïétiques. Les souris déficientes en LIF ont moins de cellules souches hématopoïétiques et présentent une activation des cellules T altérée. L'administration de LIF aux nerfs axotomisés améliore la régénération et la myélinisation tout en augmentant la masse musculaire.
Le facteur de croissance glial (GGF) appartient à une famille de protéines appelées neurégulines et agit via les hétérodimères des récepteurs erbB2, erbB3 et erbB4 présents sur les neurones sensoriels, moteurs et sympathiques primaires. Le GGF stimule la prolifération des cellules de Schwann, régulant les cellules neuronales et gliales au cours du développement de la jonction neuromusculaire et de la régénération des nerfs périphériques. Les cellules de Schwann sont une source cruciale de facteurs neurotrophiques et vitales pour le processus de régénération axonale et leur prolifération est médiée par le GGF.
Synonymes, antonymes
Voir tous les synonymes pour "neurotrophique".1 synonyme (sens proche) de "neurotrophique" :
- neurotrophe
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à NEUROTROPHIQUE sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
Le mot NEUROTROPHIQUE est dans la page 1 des mots en N du lexique du dictionnaire.
Mots en N à proximité
neurotoxine neurotoxique neurotransmetteur neurotrope neurotrophine neurotrophiqueneurovégétatif neurula neurulation neuston neustonique
En rapport avec "neurotrophique"
La neurotensine est un tridécapeptide présent dans le système nerveux central (SNC) et le tractus gastro-intestinal.

Une neurotoxine est une toxine qui agit spécifiquement sur le tissu du système nerveux, même à faible dose.

Un neurotransmetteur est une substance chimique endogène qui permet aux neurones de communiquer entre eux dans tout le corps via la transmission synaptique.
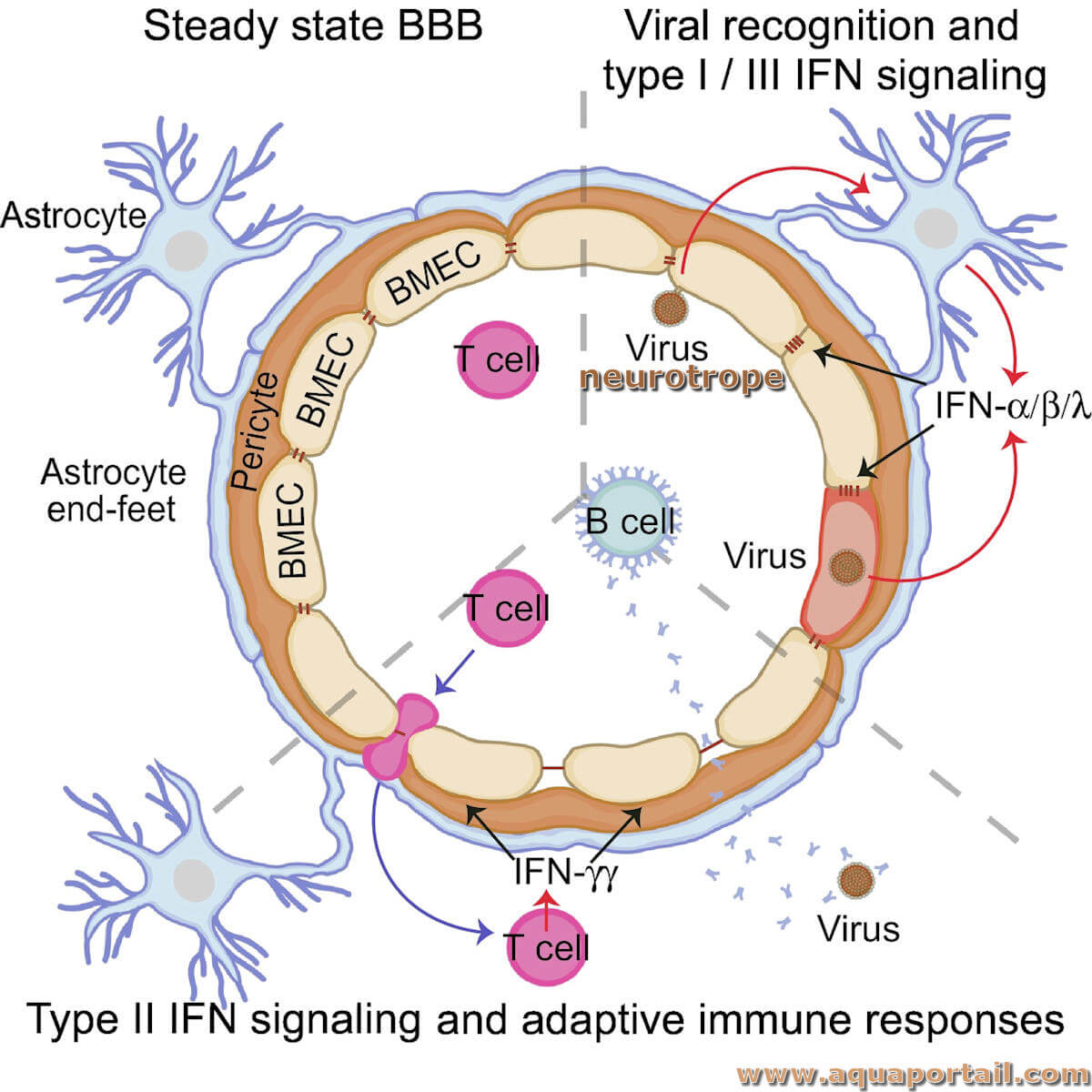
Une souche neurotrope se fixe sur le tissu nerveux, en relation avec un neurone. En médecine, une substance (ou micro-organisme) neurotrope atteint ou se fixe...
