Transaminase
Définition
Une transaminase (aminotransférase) est un type d'enzyme qui provoque le transfert d'une substance chimique appelée groupe amino d'une molécule à une autre. Les transaminases interviennent dans de nombreux processus de l'organisme, comme la synthèse des acides aminés.
Une aspartate transaminase :
Une transaminase est une enzyme qui catalyse une réaction de transamination particulière. Vue d'une aspartate transaminase (aminotransférase) de la bactérie Escherichia coli avec un cofacteur de pyridoxal 5′-phosphate.
Explications
Une transaminase est une enzyme favorisant la transamination. Les aminotransférases sont un groupe d'enzymes qui catalysent l'interconversion des acides aminés et des oxoacides par transfert de groupes aminés. La spécificité de chaque enzyme détermine l'acide aminé qui sert d'autre donneur de groupements aminés.
Les enzymes transaminases sont des enzymes dépendantes du phosphate de pyridoxal capables de transférer une amine d'une molécule donneuse à une cétone prochirale, entraînant la formation d'une amine chirale.
La catalyse dépend du cofacteur pyridoxalphosphate. Plus de 70 transaminases spécifiques de substrats ont été identifiées, parmi lesquelles la 4-aminobutyrate transaminase est une cible thérapeutique pertinente pour le traitement de l'épilepsie. Des taux sériques élevés de transaminases, en particulier d'alanine aminotransférase et d'aspartate aminotransférase, sont révélateurs d'une atteinte hépatique.
Ces dernières années, une plus grande liberté d'action et un plus grand nombre d'enzymes transaminases disponibles ont entraîné une augmentation du nombre d'ω-transaminases utilisées dans la synthèse des amines chirales. En substance, la transaminase prend une cétone et un donneur d'amine et, à l'aide du cofacteur phosphate de pyridoxal, forme une nouvelle amine et une cétone chirales. Bien entendu, il s'agit d'une réaction d'équilibre qui doit souvent être orientée vers les produits souhaités.
Les donneurs d'amine sont généralement l'alanine, l'isopropylamine et l'α-méthylbenzylamine. L'équilibre peut être obtenu chimiquement ou physiquement et dépend fortement des caractéristiques de chaque réaction.
lire plus de détails pour une transaminase (aminotransférase)...
Synonymes, antonymes
Voir tous les synonymes pour "transaminase".1 synonyme (sens proche) de "transaminase" :
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à TRANSAMINASE sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
Le mot TRANSAMINASE est dans la page 3 des mots en T du lexique du dictionnaire.
Mots en T à proximité
traitement secondaire des donnéestraitement tertiairetrame trame verte tranquilliseur transaminasetransamination transcapsidation Transcaucasie transcriptase transcriptase inverse
En rapport avec "transaminase"
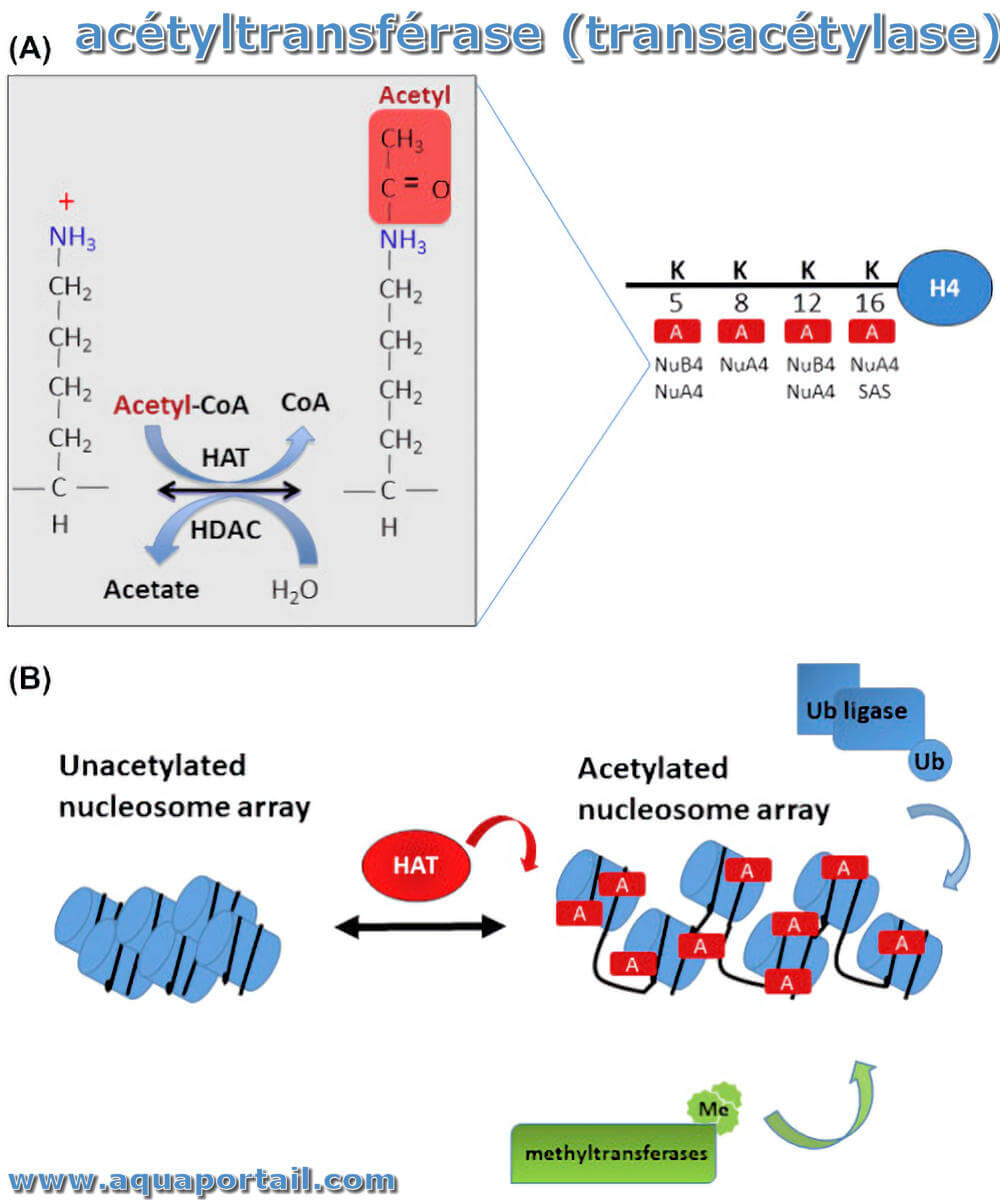
Une acétyltransférase est une enzyme qui transfère un groupe acétyle de l'acétyl CoA aux acides aminés lysine.
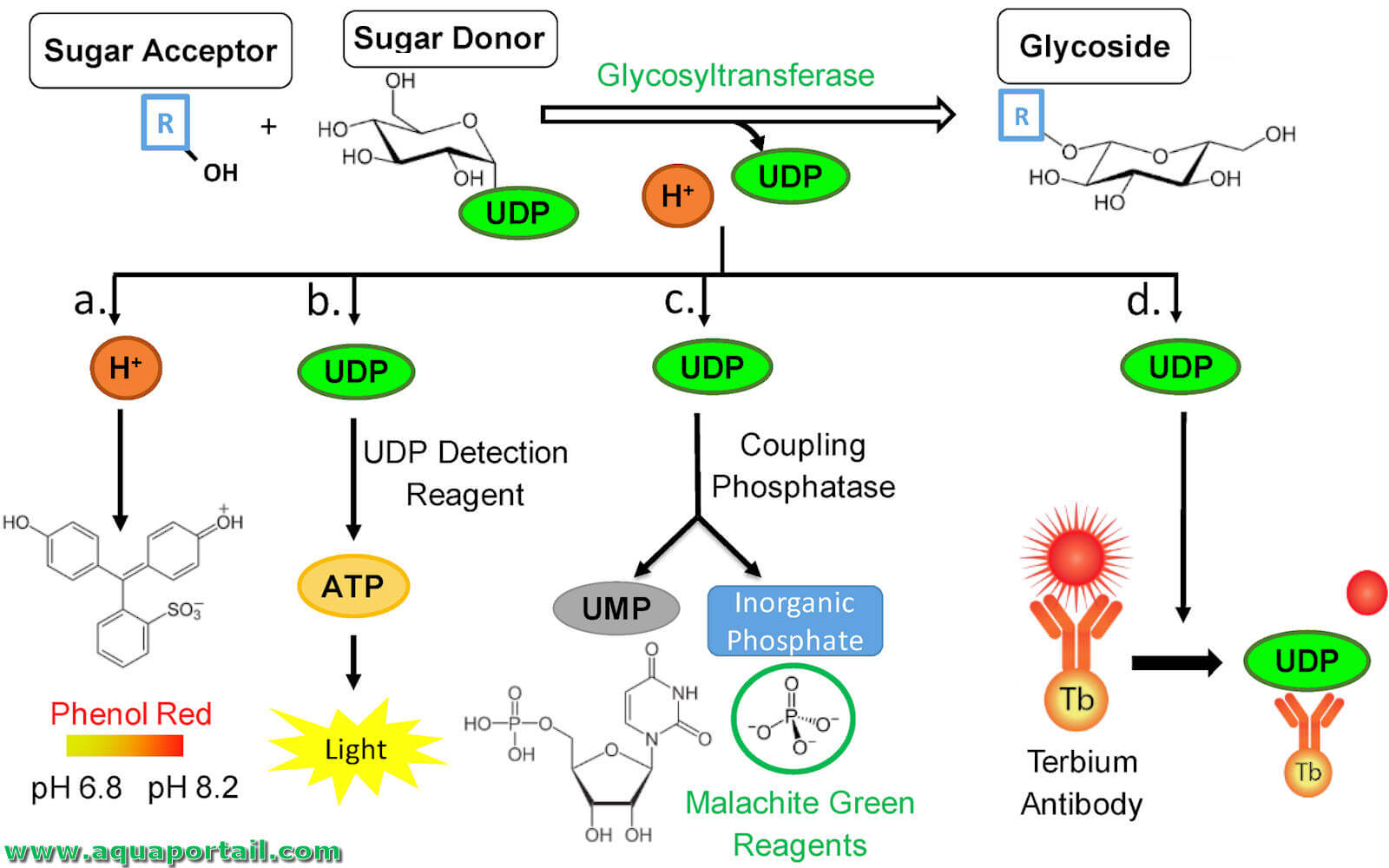
Une glycosyltransférase est une enzyme membranaire du réticulum endoplasmique, de l'appareil de Golgi et de la membrane plasmique qui catalyse la liaison d'un...
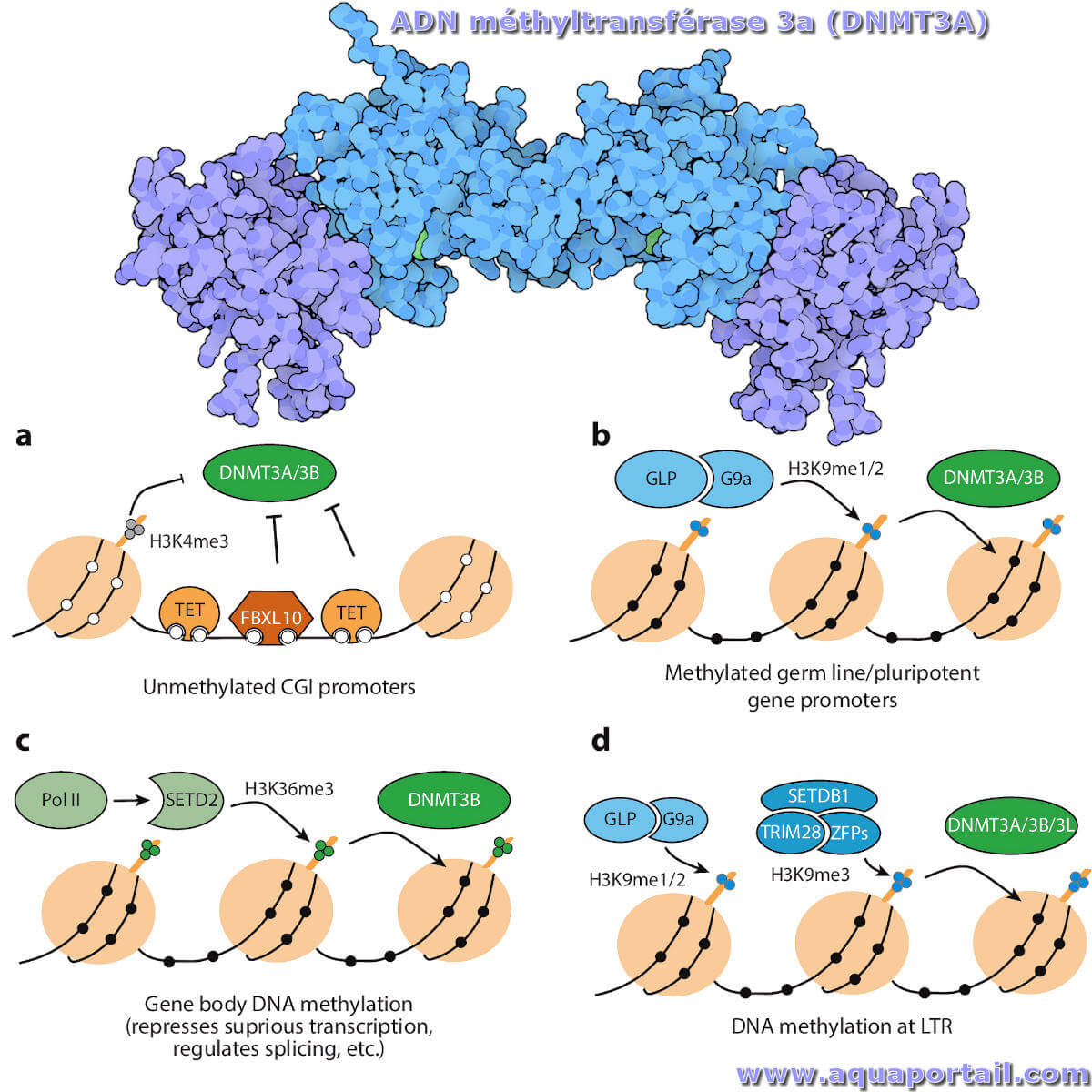
Une méthyltransférase est une enzyme qui catalyse le transfert d'un groupe méthyle du donneur de méthyle S-adénosyl-L-méthionine vers leurs substrats.
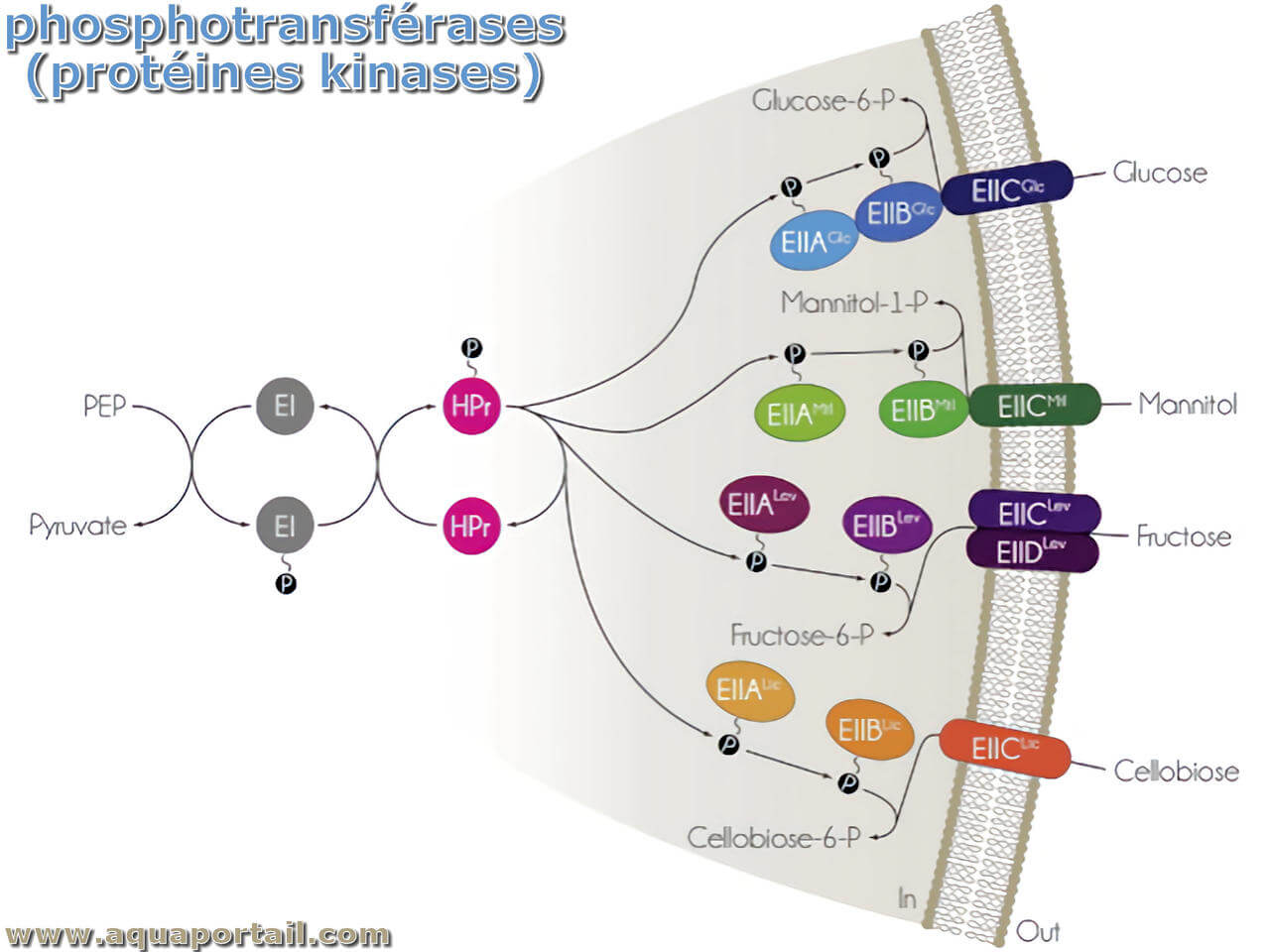
La phosphotransférase est une voie de transduction du signal impliquant un groupe phosphoryle provenant du phosphoénolpyruvate transféré au glucide transloqué...
