Potentiel Hydrogène
Définition
Le pH, ou potentiel Hydrogène, traduit l'acidité vraie ou l'alcalinité d'une solution, autrement dit sa concentration en ions H+. La conductivité électrique, très faible mais mesurable, d'une eau bidistillée, parfaitement pure, montre qu'elle contient 0,000 001 g/l d'ions H+, et autant d'ions OH-.
Cette eau (comme toute solution parfaitement neutre) contient donc 1 × 10-7 ions H+, ce qu'il est plus facile d'écrire pH = 7 (logarithme décimal, changé de signe, de la concentration en ions hydrogène). Une solution normale d'un acide fort, totalement dissocié, contient 1 gramme/litre d'ions H+; son pH est donc de 0 (antilog 0 = 1).
Le pH d'une solution normale d'une base, totalement dissociée, est égal à 14. Une solution acide a donc un pH inférieur à 7, une solution alcaline un pH supérieur à 7, une solution neutre un pH égal à 7. À une acidité croissante correspondent, par conséquent, des chiffres décroissants.
Le pH en courbe :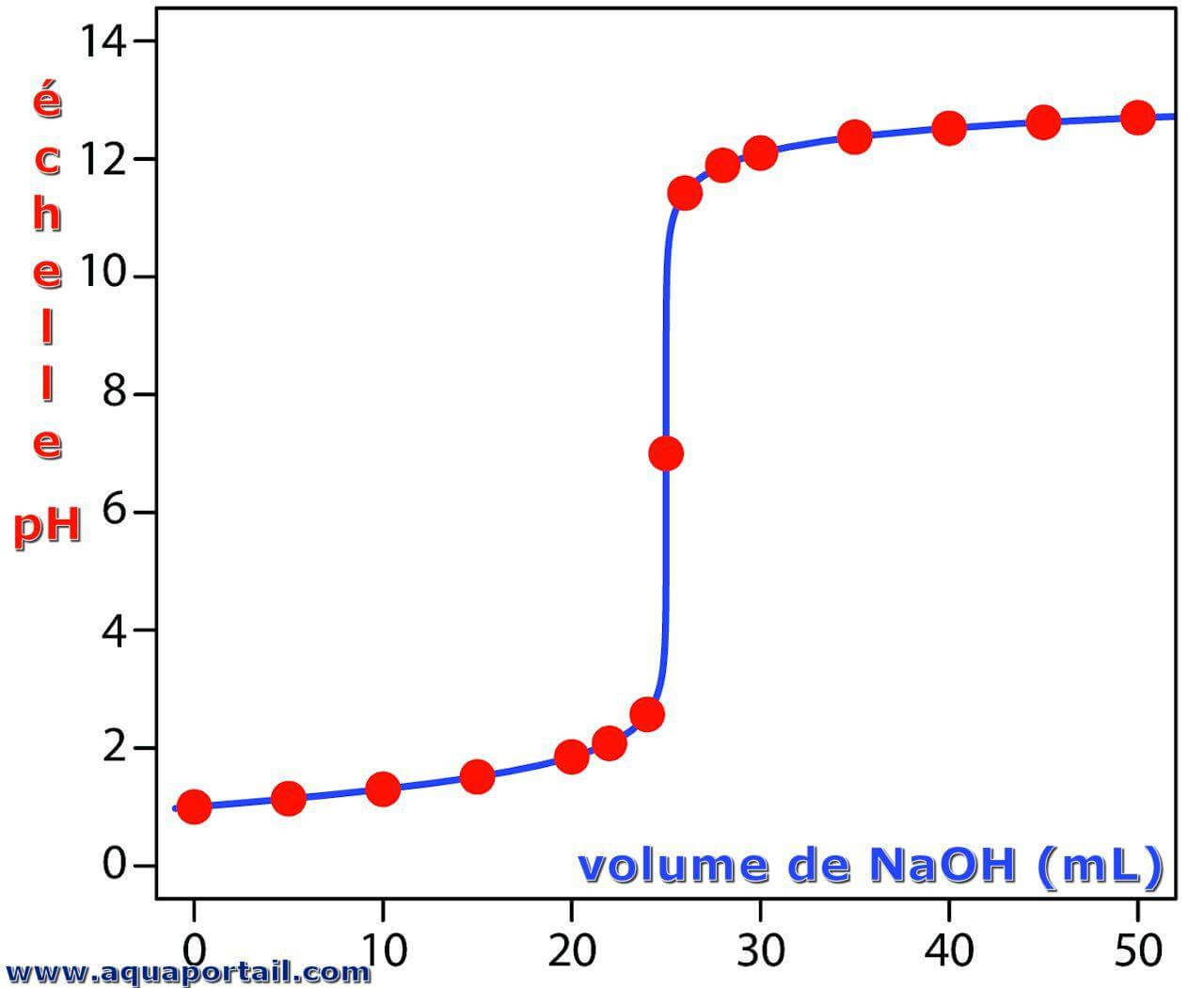
Le potentiel hydrogène (pH) varie de 0 à 14 sur l'échelle. L'échelle de pH est traçable et applicable à un ensemble de solutions standards dont le pH est établi par un accord international.
Explications
La mesure du pH se réalise à 25 °C pour un test et, dans l'eau, les conventions sont les suivantes :
- Si pH < 7, la solution est acide;
- si pH = 7, la solution est neutre;
- Si pH > 7, la solution est basique.
Voir la page détaillée sur le pH en aquarium. Le pH des solutions aqueuses peut être mesuré avec une électrode de verre et d'un pH-mètre ou un indicateur colorimétrique et non seulement avec un "simple" test pH comme en aquarium.
Par définition simple en chimie, le pH (potentiel Hydrogène) est une échelle numérique utilisée pour spécifier l'acidité ou la basicité (alcalinité) d'une solution aqueuse. le pH mesure l'activité de protons (H+). Dans l'eau, l'ion H+ est sous la forme de l'ion oxonium. Le pH mesure l'acidité ou la basicité d'une solution. En 1909, Le Dr. Sörensen a défini l'acidité d'une solution : pH = -log[H+]. L'échelle de pH évolue de 0 à 14.
Contrairement à la croyance populaire, la valeur du pH peut être inférieure à 0 ou supérieure à 14 pour les acides très forts et les bases très fortes.
Comme nous venons de le voir dans la définition, l'acidité d'une solution est proportionnelle à la concentration en ions H+. Il existe dans une solution un équilibre entre les ions H+ et les ions OH-. Une eau distillée, à température et pression standard, possède un pH de 7. C'est la neutralité de l'eau. L'eau à l'état basal est capable de se dissocier en ion H+ et OH-, ce procédé est l'autoprotolyse de l'eau. On constate une concentration en ions H+ à 10^-7 et une concentration en ions OH- identique.
L'eau se comporte comme une base et comme un acide, on obtient cette formule chimique : 2H2O ↔ H3O+ + OH-.
On peut également apprécier l'équilibre entre H+ et OH- grâce à cette formule : [H+] x [OH-] = 10-14. Donc dans une eau acide, avec un pH < 7, [H+] > [OH-]
Pour un pH minimal de O, on a une concentration de 10 mol/L de H+. Pour un pH maximal de 14, on a une concentration de 10-14 de H+.
Un constat, une variation d'une unité de pH fait varier par 10 la concentration en ions H+. Un exemple, lors du passage d'une eau d'un pH de 7 à 9, on observe une variation par 100, c'est à dire qu'il y aura 100 fois moins d'ions H+ et 100 fois plus d'ions OH-.
Le pH de l'aquarium, au niveau biologique, est toujours proche de la neutralité soit un pH de 7. En aquariophilie, on observera des pH de 5,0 à 8,5. Il existe une grande relation entre le pH et d'autres paramètres de l'eau tel que le TH (GH) ou le TAC (KH).
Il existe de nombreux facteurs influençant le pH :
- Facteurs physiques : éclairage, température...
- Facteurs chimiques : CO2, dioxygène O2 dissous...
- facteurs biologiques : faune et flore.
Le pH est également un important indicateur de la santé du bac, ainsi une variation demande une étude rapide du problème : pH et CO2 : la variation du taux de CO2 est un élément clé des variations de pH. Les sources de CO2 sont la respiration des poissons et des végétaux, la production par les bactéries, la dégradation des matières organiques... L'élimination du CO2 se fait grâce au brassage, à l'aération, à l'éclairage (photosynthèse), aux changements d'eau...
Voici la liste des réactions chimiques : CO2 + H2O → H2CO3 → H+ + HCO3 → 2H+ + CO32- (carbonates et bicarbonates) ou CaCO3 + CO2 + H2O → Ca++ + 2HCO3-.
Le pH dans l'aquarium varie tout le temps, notamment avec une variation nycthémérale du pH : une diminution du pH a lieu la nuit en rapport avec la production de CO2 par les végétaux, les urines des poissons; une augmentation du pH a lieu la journée en rapport avec la photosynthèse, production de O2 et consommation de CO2. Ces variations sont limités dans un bac correctement équilibré, et normales, avec un pouvoir tampon standard.
Mesurer son pH consiste à faire un test pH : les indicateurs papiers sont trop peu précis en aquariophilie; les tests colorimétrique offre une gamme de colorants qui changent de teinte en fonction du pH, très utile, assez précis; la mesure électrométrique est très cher, et n'aboutit pas à un aquarium pas cher; elle mesure la différence de potentiel entre deux électrodes, et elle nécessite un étalonnage mensuel.
Faire varier son pH pour l'augmenter ou le baisser volontairement est habituel en aquariophilie. Pour augmenter le pH, on peut utiliser du bicarbonate de sodium ou mieux du sable issu de l'érosion du corail (voir sable de corail) que l'on placera dans le filtre. Pour diminuer le pH, on peut utiliser de la tourbe (après diminution du GH), injecter du CO2. Il est conseillé de ne jamais utiliser de produit chimique pour modifier son pH. Un pH acide ne s'obtient qu'avec une dureté faible, et inversement.
Synonymes, antonymes
Voir tous les synonymes pour "potentiel Hydrogène".1 synonyme (sens proche) de "potentiel Hydrogène" :
- pH
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à POTENTIEL HYDROGÈNE sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
L'expression POTENTIEL HYDROGENE est dans la page 8 des mots en P du lexique du dictionnaire.
Mots en P à proximité
potentiel d'écotoxicité potentiel de l'eau potentiel de membrane potentiel de pression potentiel électrique potentiel Hydrogènepotentiel postsynaptique potentille potomètre Pottiacées pou du poisson
En rapport avec "potentiel Hydrogène"

Une acidité, une alcalinité, est une force d'un acide ou d'une base : les propriétés acides (ou basiques = alcalines) d'une solution sont dues aux ions H⁺...
L'acidité de l'eau est une quantité, exprimée en milliéquivalents par litre d'eau, de base forte qui doit être utilisée pour neutraliser les acides forts...

Un acide est une substance qui, lorsqu'elle est dissoute dans l'eau, produit une concentration accrue d'ions hydrogène.

Une base est une substance, un composé chimique, qui peut accepter des ions hydrogène (protons) ou plus généralement, donner une paire d'électrons de valence.
