Liaison ionique
Définition
Une liaison ionique est l'attraction électrostatique qui unit des ions de charges opposées dans les composés ioniques. Les types d'éléments formant des liaisons ioniques sont les métaux et les non-métaux.
Exemple de liaison ionique :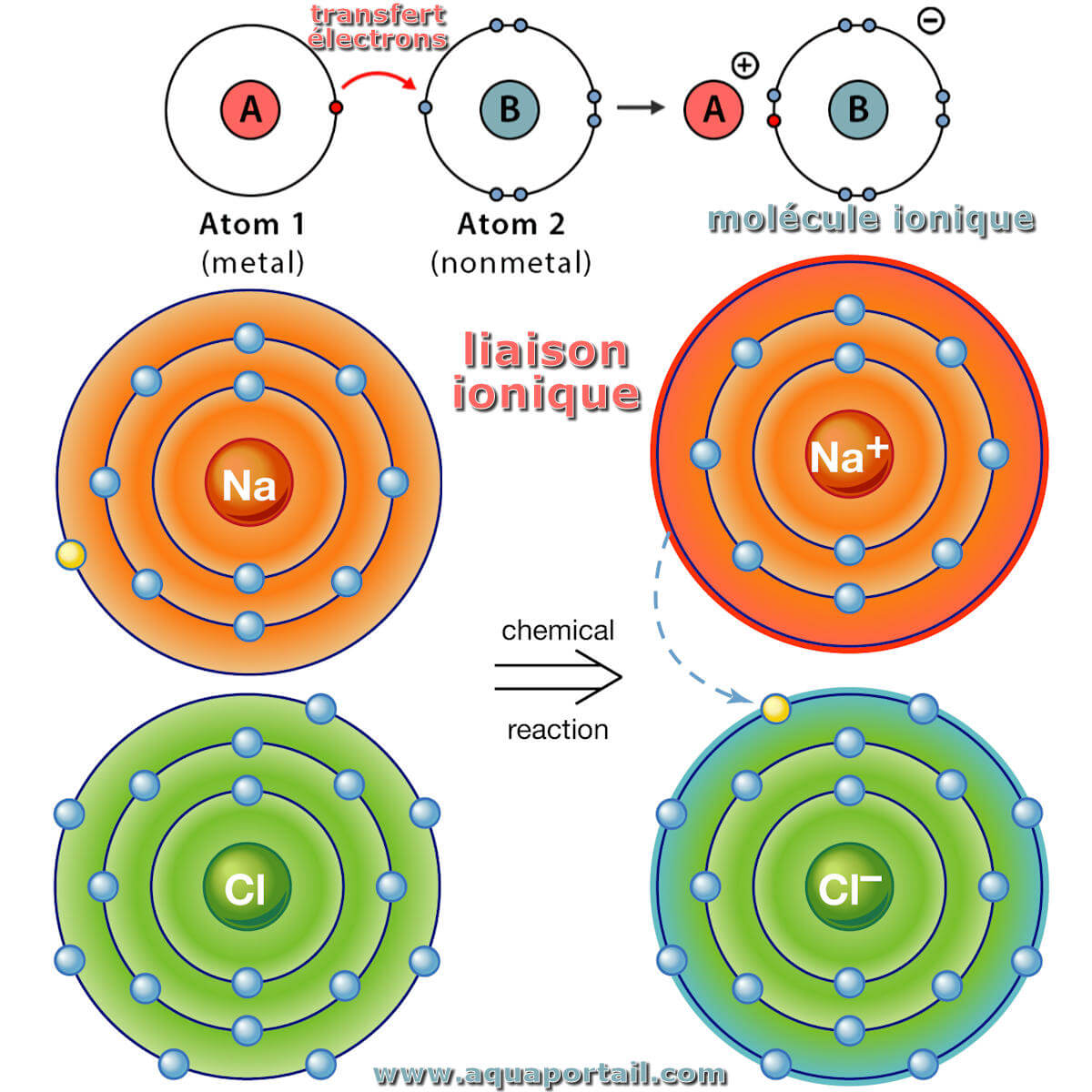
La liaison ionique se forme lorsque les électrons de valence (les plus externes) d'un atome sont transférés de manière permanente à un autre atome en suivant la règle de l'octet.
Explications
La liaison ionique est le transfert complet d'électrons de valence entre les atomes. C'est un type de liaison chimique qui génère deux ions de charge opposée. Dans les liaisons ioniques, le métal perd des électrons pour devenir un cation chargé positivement, tandis que le non-métal accepte ces électrons pour devenir un anion chargé négativement. Lorsque les deux ions se combinent via une liaison ionique, ils forment des composés ioniques.
En qualité de liaison électrovalente, la liaison ionique est à différencier de la liaison covalente.
L'électronégativité est une propriété d'un atome, mesurant la force avec laquelle il attire ou retient les électrons. Les liaisons ioniques se forment lorsqu'il y a une différence d'électronégativité élevée entre les atomes. La grande différence d'électronégativité se traduit par une attraction électrostatique entre les électrons d'un atome et les noyaux de l'autre atome. Lorsque les atomes transfèrent des électrons, ils atteignent une configuration électronique de gaz inerte stable. En conséquence, les sphères les plus externes (valence) des atomes sont complètes.
Dans les liaisons ioniques, on distingue la liaison simple (-), la liaison double (=) et la liaison triple (≡).
La liaison ionique est la force d'attraction électrostatique entre un ion métallique chargé positivement et un ion non métallique chargé négativement. Les métaux forment des ions positifs car ils perdent des électrons pour devenir stables.
Propriétés
Les liaisons ioniques affectent les propriétés des composés ioniques, principalement les propriétés physiques :
- Implique le transfert d'électrons d'un atome à un autre.
- Formé entre un métal et un non-métal avec une forte différence d'électronégativité afin que le non-métal puisse attirer les électrons du métal.
- L'attraction entre les noyaux et les électrons est électrostatique avec séparation des charges. Elles sont les plus réactives de toutes les liaisons dans le milieu approprié.
- La force est directement proportionnelle à la quantité de charges et inversement proportionnelle à la distance entre les ions chargés.
- Les composés ioniques ont des points de fusion et d'ébullition élevés. Les atomes sont maintenus ensemble dans une structure en treillis et il faut beaucoup d'énergie pour fondre les composés.
- Les composés ioniques ont généralement une structure en treillis et sont cristallins à température ambiante.
- Les composés ioniques sont cassants, et ils se cassent le long des plans où la pression est appliquée.
- Le composé ionique se dissout dans l'eau et d'autres solvants polaires très doucement. Les cristaux se décomposent en ions, qui sont les vecteurs de l'électricité. De plus, les composés ioniques conduisent également l'électricité à l'état fondu.
- Les composés ioniques sont insolubles dans les solvants non polaires.
- Les composés ioniques présentent une vitesse de réaction élevée.
- Les liaisons ne sont pas directionnelles, c'est pourquoi les composés ioniques ne présentent pas d'isomérie.
Synonymes, antonymes
Voir tous les synonymes pour "liaison ionique".1 synonyme (sens proche) de "liaison ionique" :
- liaison électrovalente
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à LIAISON IONIQUE sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
L'expression LIAISON IONIQUE est dans la page 2 des mots en L du lexique du dictionnaire.
Mots en L à proximité
liaison de van der Waals liaison disulfure liaison double liaison génétique liaison génomique liaison ioniqueliaison peptidique liaison simple liaison triple liane liant
En rapport avec "liaison ionique"

La force de van der Waals est une force à courte portée existant à la fois dans les phases gazeuse et liquide en raison de la fluctuation des nuages...

La force électrostatique est la force d'attraction ou de répulsion entre deux particules chargées.
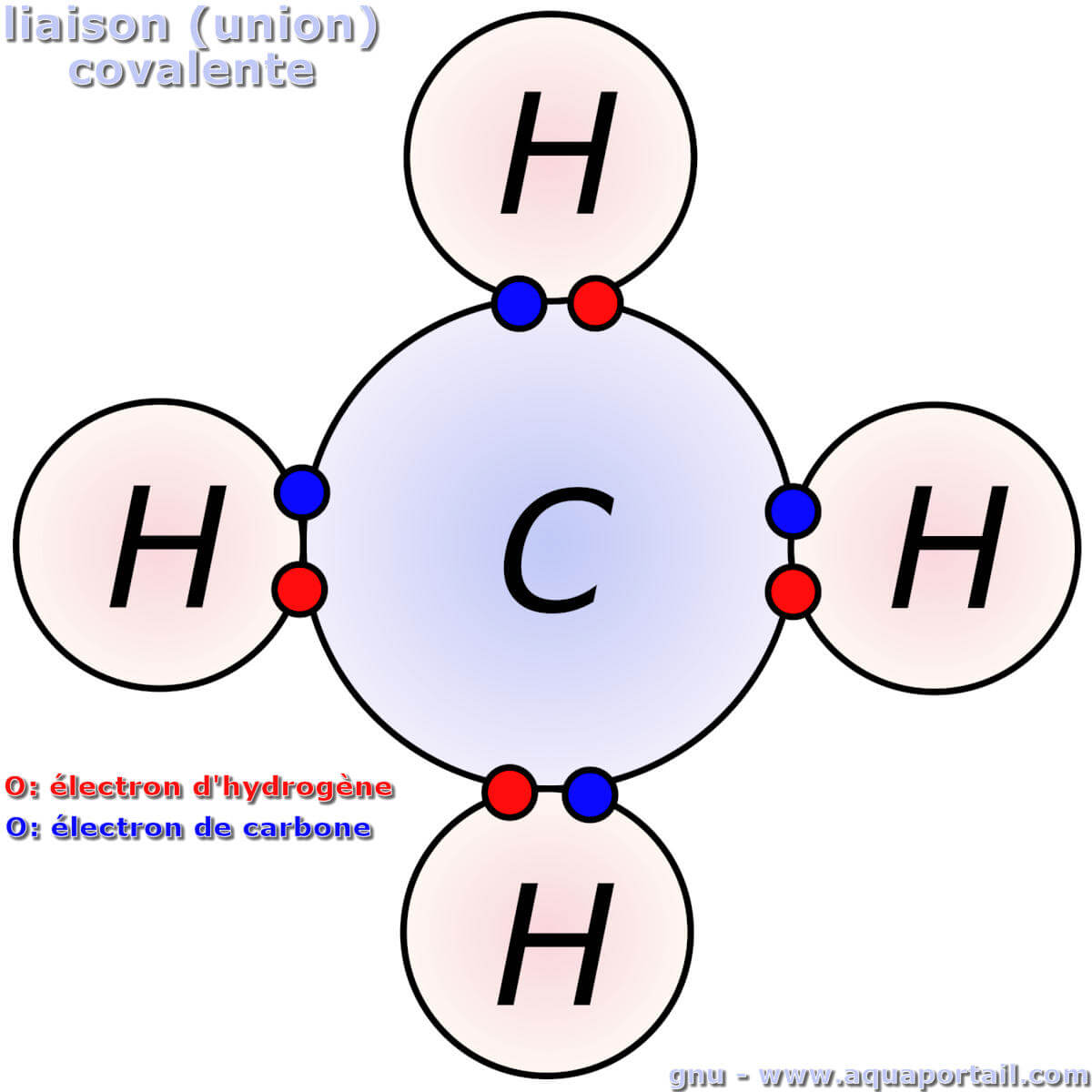
Une liaison covalente est l'union de deux atomes non métalliques par le partage d'électrons dans une molécule.

La liaison simple est la liaison ionique la plus simple avec des éléments métalliques et non métalliques dans la substance.
