Point de congélation
Définition
Le point de congélation indique précisément la température de solidification d'un liquide ou d'une substance contenant de l'eau dans des conditions données, avec un changement de pression ou de température par exemples. La congélation, la cristallisation, la gélification ou la solidification sont les inverses de l'ébullition ou la liquéfaction.
Un thermomètre avec la température de congélation :
Le point de congélation de l'eau est aussi le point de fusion de l'eau.
Explications
Pour la plupart des substances, le point de congélation est l'opposé strict du point de fusion, même si ces deux point sont le plus souvent identiques et égaux. Mais ce n'est pas toujours le cas : par exemple, l'agar-agar fond à 85 °C et se solidifie de 31 à 40 °C; ce processus est connu sous le nom d'hystérésis.
Contrairement au point d'ébullition, le point de congélation ou le point de cristallisation d'une substance est peu affecté par la pression et, par conséquent, peut être utilisé pour caractériser les composés organiques et pour vérifier leur pureté.
En raison de l'aptitude de certaines substances à la surfusion, le point de congélation n'est pas considéré comme une propriété caractéristique d'une substance. Lorsque le "point de congélation caractéristique" d'une substance est déterminé, la méthodologie actuelle est presque toujours le principe de l'observation de la disparition plutôt que de la formation de la glace, c'est-à-dire du point de fusion.
Le point de congélation d'un solvant est abaissé lorsqu'un autre composé est ajouté, ce qui signifie qu'une solution a un point de congélation inférieur à celui d'un solvant pur. Ce phénomène est utilisé dans des applications techniques pour éviter le gel, par exemple en ajoutant du sel ou de l'éthylène glycol à l'eau. Ce phénomène est appelé la dépression du point de congélation.
Voir aussi le point triple de l'eau.
Normalement, le point de congélation de l'eau et le point de fusion sont 0 °C ou 32 °F. La température peut être plus basse en cas de surfusion ou de présence d'impuretés dans l'eau susceptibles de provoquer une dépression du point de congélation. Sous certaines conditions, l'eau peut rester un liquide aussi froid que -10 °C !
Comment l'eau peut-elle rester jusque-là en dessous de son point de congélation habituel ? La réponse est que l'eau a besoin d'un germe de cristal ou d'une autre petite particule (noyau) sur laquelle former des cristaux. Alors que la poussière ou les impuretés offrent normalement un noyau, l'eau très pure ne cristallisera pas avant que la structure des molécules d'eau liquide ne se rapproche de celle de la glace solide.
Synonymes, antonymes
Voir tous les synonymes pour "point de congélation".3 synonymes (sens proche) de "point de congélation" :
- point de cristallisation
- point de solidification
- température de congélation
3 antonymes (sens contraire) :
- point d'ébullition
- point de fusion
- température de fusion
Les mots ou les expressions apparentés à POINT DE CONGÉLATION sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
L'expression POINT DE CONGELATION est dans la page 6 des mots en P du lexique du dictionnaire.
Mots en P à proximité
point amphidromique point chaud point critique point d'ébullition point de compensation point de congélationpoint de flétrissement point de jauge point de repère point de rosée point végétatif
En rapport avec "point de congélation"

La congélation est le passage d'un état liquide à un état solide par perte de chaleur, en faisant chuter la température en dessous de 0°C (point...

La cryoclastie, gélivation ou gélifraction, est un processus consistant dans la fragmentation des roches en raison des tensions produites lors...
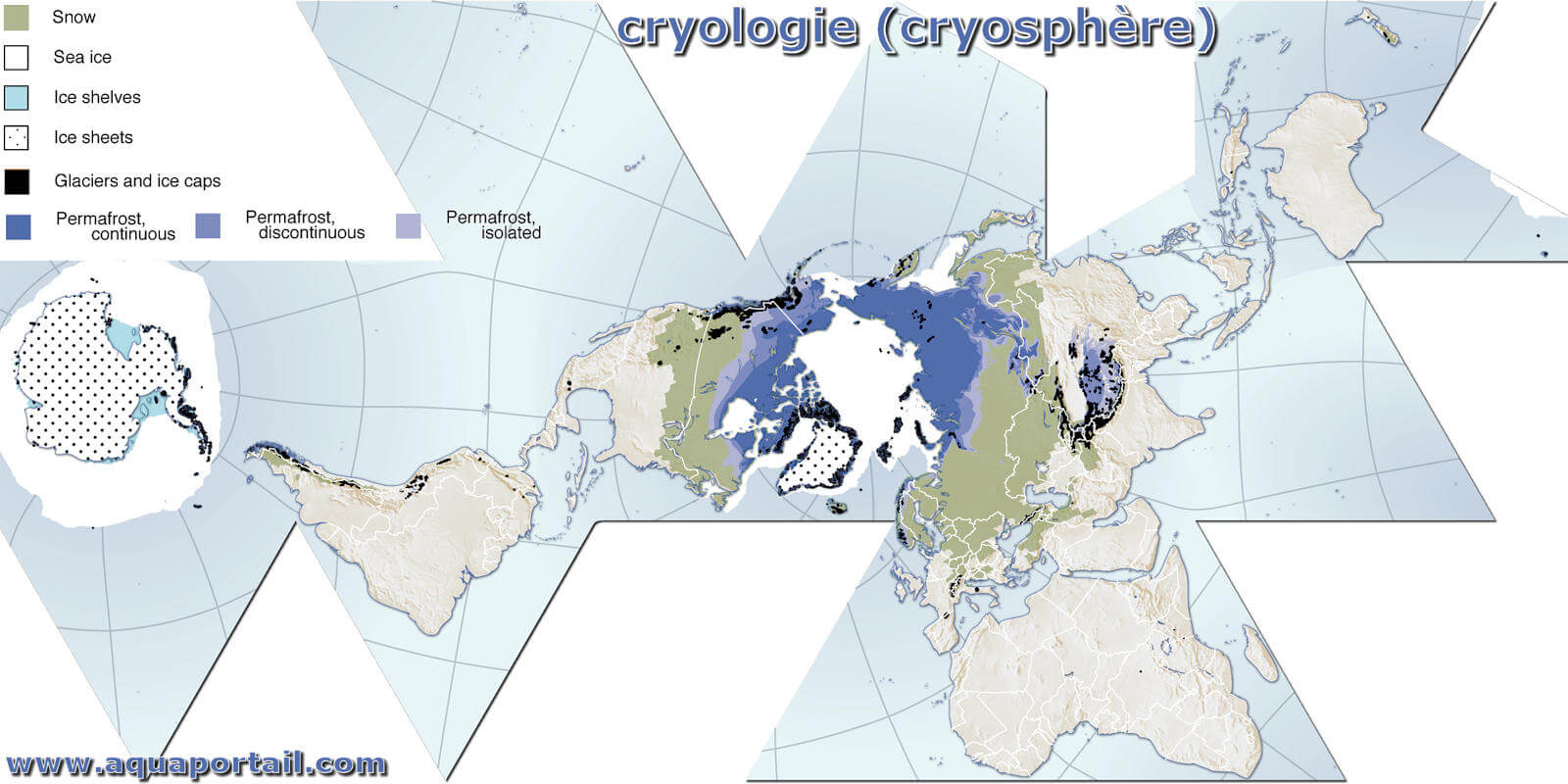
La cryologie est la science du froid dont le sujet est l'étude de l'eau à l'état solide, par exemple la glace, la neige, la grêle, le grésil, etc.

Un organisme cryophile aime le froid, il résiste au gel et vit à basse température. En botanique, les algues ou les plantes cryophiles qualifient un type...
