Activité ionique
Définition
Une activité ionique est une grandeur rendant compte des phénomènes d'interactions entre ions en solution qui augmentent lorsque la concentration augmente. Elle correspond à la notion de concentration efficace d'un ion.
L'activité ionique d'une particule :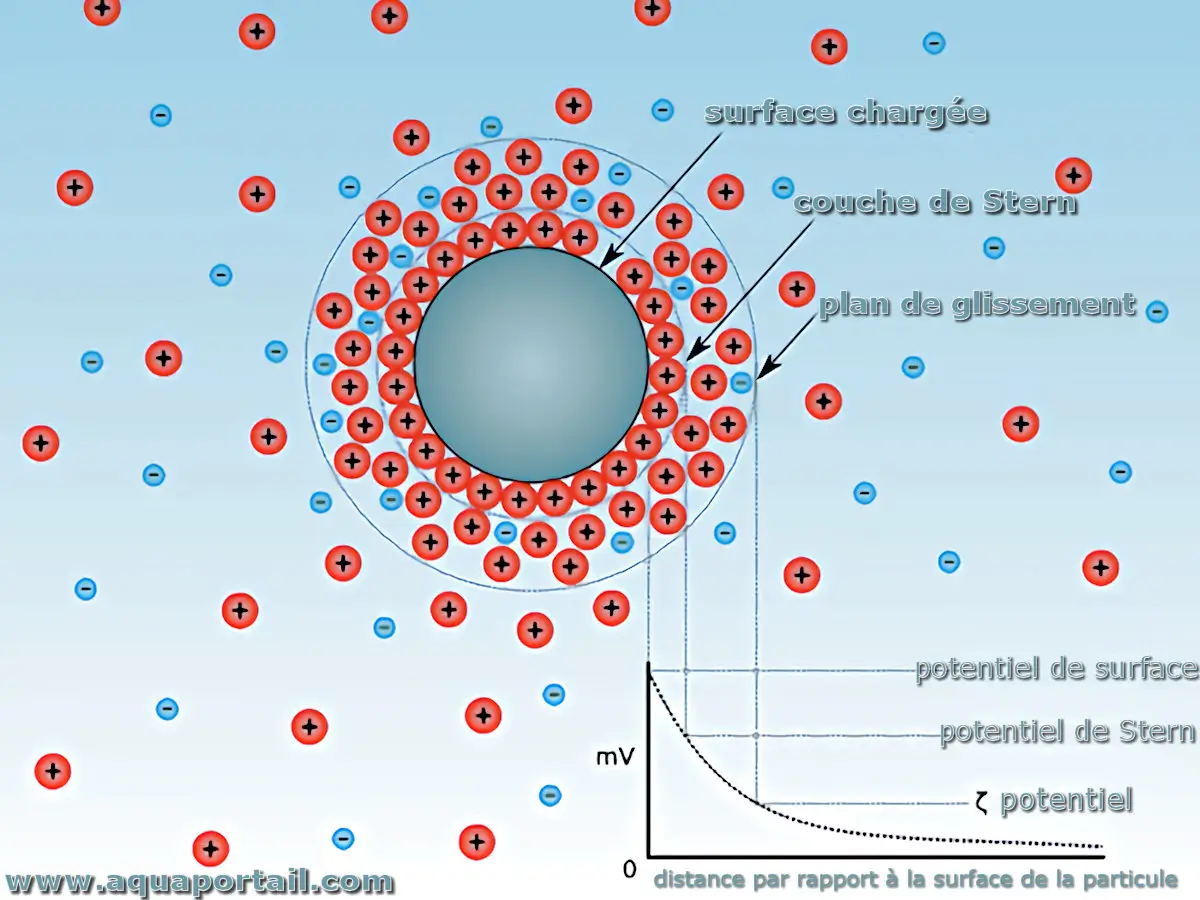
L'activité ionique fait référence à la concentration d'ions dans une solution, ajustée par un facteur appelé coefficient d'activité. Cette relation est représentée par l'expression : Activité (a) = Coefficient d'activité (y) × Concentration ionique (C). Diagramme illustrant la concentration ionique et la différence de potentiel en fonction de la distance par rapport à la surface chargée d'une particule en suspension dans un milieu de dispersion.
Explications
L'activité d'un ion est le produit de la concentration de cet ion par son coefficient d'activité. Ce dernier tend vers 1 lorsque la concentration tend vers 0, d'où l'approximation selon laquelle la concentration se confond avec l'activité en solution diluée.
Les propriétés des solutions électrolytiques peuvent s'écarter considérablement des lois utilisées pour dériver le potentiel chimique des solutions. Dans les solutions non électrolytiques, les forces intermoléculaires sont principalement constituées d'interactions de van der Waals faibles, qui une un dépendance r-7, et à des fins pratiques, cela peut être considéré comme idéal.
Cependant, dans les solutions ioniques, il existe des interactions électrostatiques significatives entre les molécules soluté-solvant et soluté-soluté. Ces forces électrostatiques sont régies par la loi de Coulomb, qui a un dépendance r-2. Par conséquent, le comportement d'une solution électrolytique s'écarte considérablement de celui d'une solution idéale. C'est pourquoi l'activité des composants individuels est utilisée et non la concentration ionique pour calculer les écarts par rapport au comportement idéal.
En 1923, Peter Debye et Erich Hückel ont développé une théorie qui permettrait de calculer le coefficient d'activité ionique moyen de la solution, γ±, et pourrait expliquer comment le comportement des ions en solution contribue à cette constante.
La théorie de Debye-Hückel (loi limitative Debye-Hückel) est basée sur trois hypothèses sur la façon dont les ions agissent en solution :
- Les électrolytes se dissocient complètement en ions en solution.
- Les solutions d'électrolytes sont très diluées, de l'ordre de 0,01 M.
- Chaque ion est entouré en moyenne d'ions de charge opposée.
Synonymes, antonymes
Voir tous les synonymes pour "activité ionique".1 synonyme (sens proche) de "activité ionique" :
- activité des ions
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à ACTIVITÉ IONIQUE sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
L'expression ACTIVITE IONIQUE est dans la page 2 des mots en A du lexique du dictionnaire.
Mots en A à proximité
activateur biologiqueactivation d'un acide aminéactivine activité enzymatique activité géologique activité ioniqueactophile aculé aculéolé acumen acuminé
En rapport avec "activité ionique"

La balance ionique est basée sur le principe de neutralité électrique, ce qui signifie que la concentration équivalente d'ions chargés positivement...
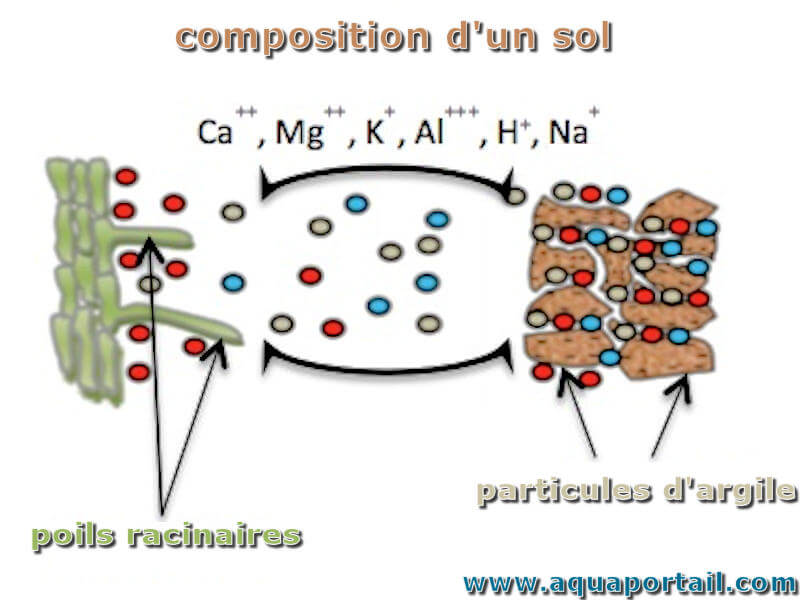
La capacité d'échange cationique (CEC) est la capacité totale d'un sol à contenir des cations échangeables.
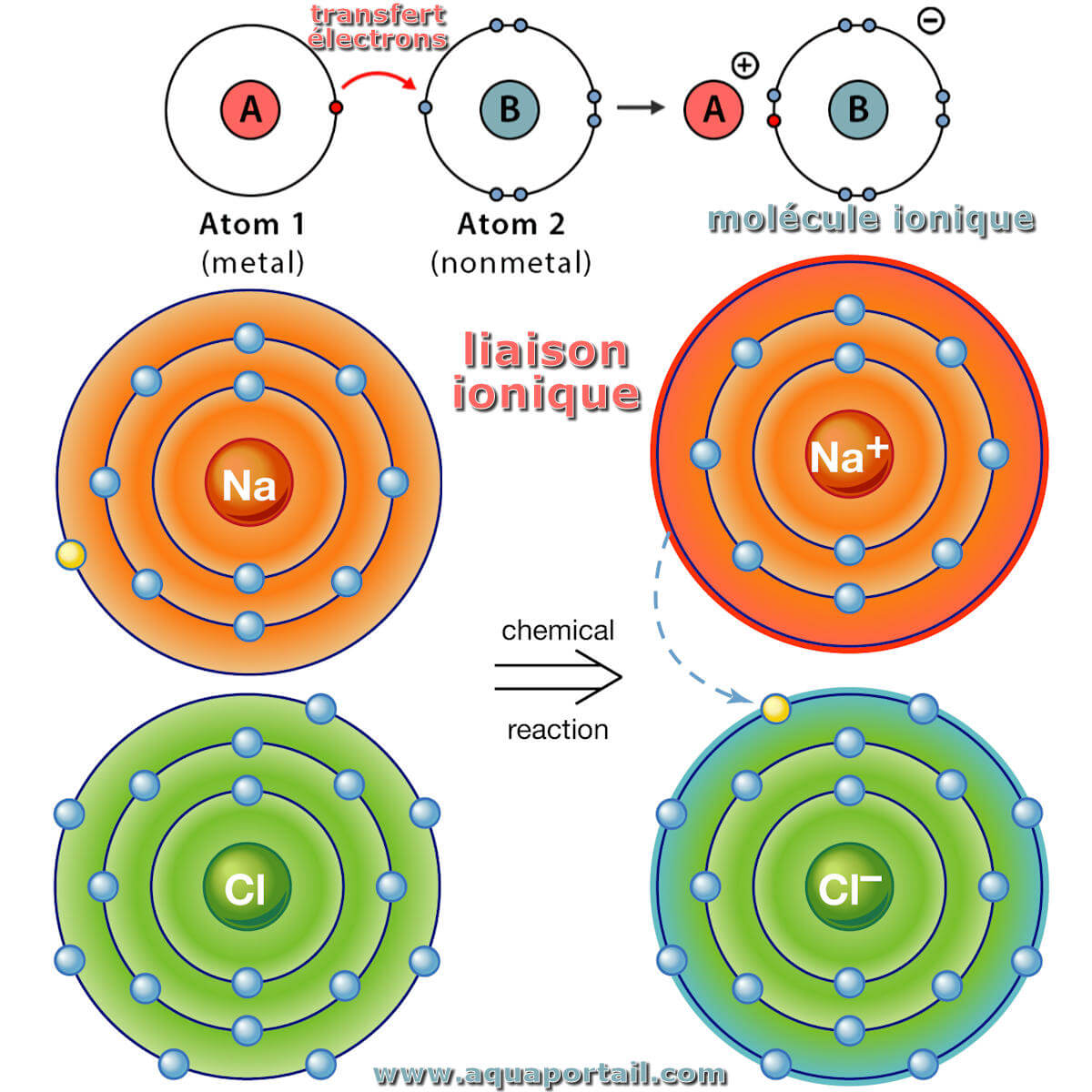
Une liaison ionique est l'attraction électrostatique qui unit des ions de charges opposées dans les composés ioniques.
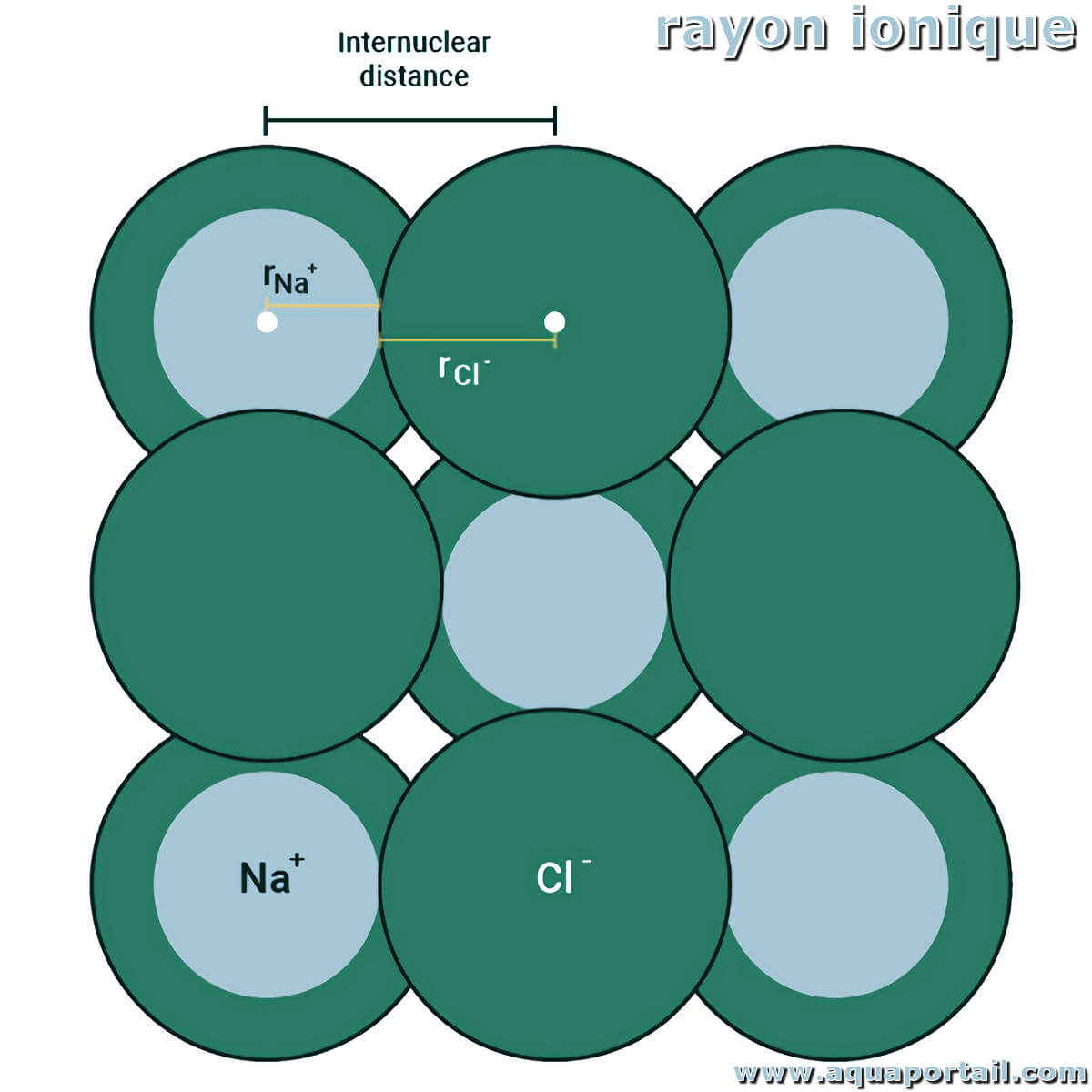
Le rayon ionique peut être défini comme la taille du rayon d'un ion monoatomique d'un atome, du noyau à l'électron de valence.
