Molécule
Définition
Une molécule est un groupe d'atomes solidement liés entre eux pour former le plus petit échantillon d'un corps pur (élément simple ou composé). Les plus petites molécules sont composées de seulement deux atomes, identiques ou différents (O2, NaCl).
Une molécule :
La molécule est un groupe d'atomes liés entre eux, représentant la plus petite unité fondamentale d'un composé chimique pouvant participer à une réaction chimique.
Explications
Les molécules simples sont constituées d'au moins deux atomes du même élément ou différents. Les molécules complexes sont constituées de plus de deux atomes du même élément ou d'éléments différents, par exemple le carbonate de calcium (CaCO3). Leurs liaisons chimiques tendent à être plus fortes que celles des molécules simples.
Le nombre de noyaux atomiques constituant une molécule est un nombre déterminé. Ainsi, un cristal de NaCl(s) n'est pas une molécule : c'est un réseau ionique constitué d'un nombre indéterminé d'atomes (avec s différent de 1).
Exemples de molécule simple : le dioxygène O2 est une molécule formée de seulement 2 atomes d'oxygène; le sel de table NaCl est une molécule constituée d'1 atome de sodium et d'1 atome de chlore.
Exemple de molécule complexe : le glucose C6H12O6 (un sucre) est une molécule groupant 6 atomes de carbone, 12 atomes d'hydrogène et 6 atomes d'oxygène.
Les molécules biologiques, comme les protéines et l'ADN, des macromolécules, peuvent être constituées de plusieurs milliers d'atomes.
Le nitrate est une molécule :
La molécule de nitrate a pour formule chimique NO3-, formée d'1 atome d'azote et de 3 atomes d'oxygène. Une molécule est la plus petite particule d'une substance possédant toutes les propriétés physiques et chimiques de cette substance.
L'une des molécules triatomiques les plus abondantes de l'univers est le cation trihydrogène H3+. Bien qu'abondant dans l'espace, où il est stabilisé par la très basse température et la faible densité de la matière, le cation trihydrogène est rare sur Terre.
lire plus de détails pour une molécule...
Synonymes, antonymes
Voir tous les synonymes pour "molécule".6 synonymes (sens proche) de "molécule" :
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à MOLÉCULE sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
Le mot MOLECULE est dans la page 4 des mots en M du lexique du dictionnaire.
Mots en M à proximité
moina moisissure molariforme molarité molasse moléculemolécule de signal molécule de signalisation molécule élémentaire molécule organique molécule prébiotique
En rapport avec "molécule"
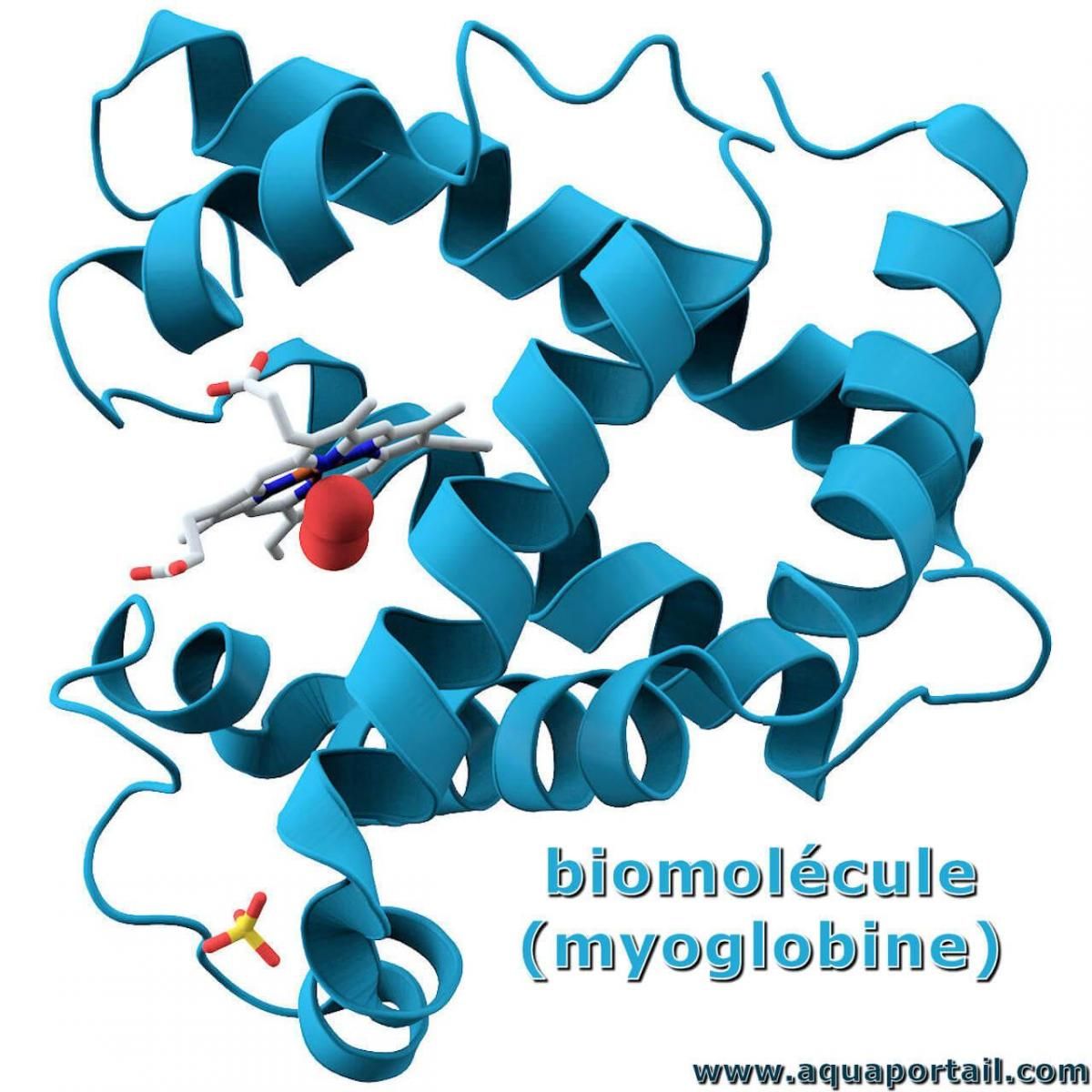
Les biomolécules sont les molécules organiques les plus essentielles, impliquées dans la maintenance et les processus métaboliques des organismes vivants.
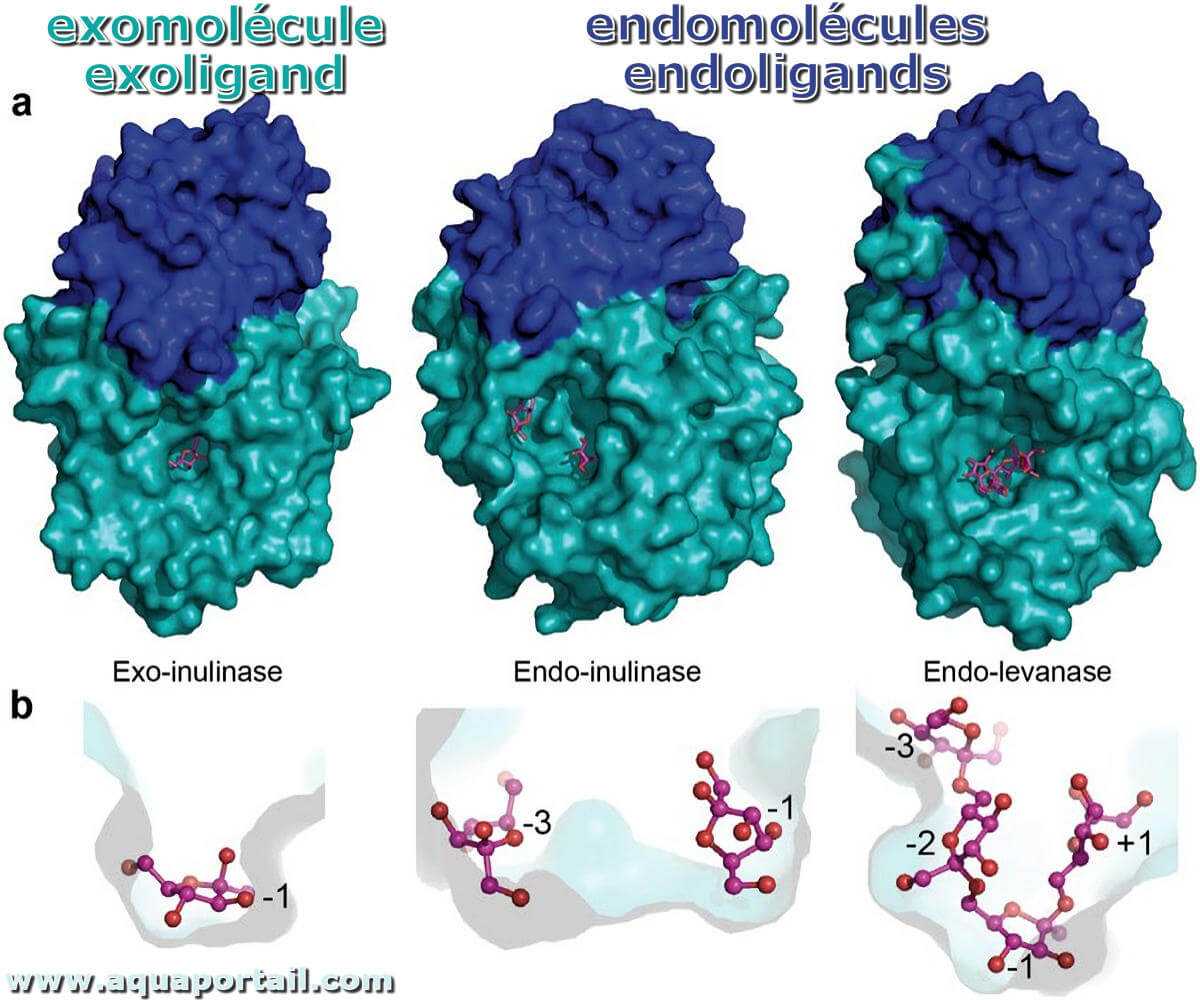
Une exomolécule complexante est un ligand, un exoligand qui est une molécule organique excrétée par les micro-organismes et ayant des propriétés...

Une macromolécule est une molécule contenant un très grand nombre d'atomes, comme une protéine, un acide nucléique ou un polymère synthétique.
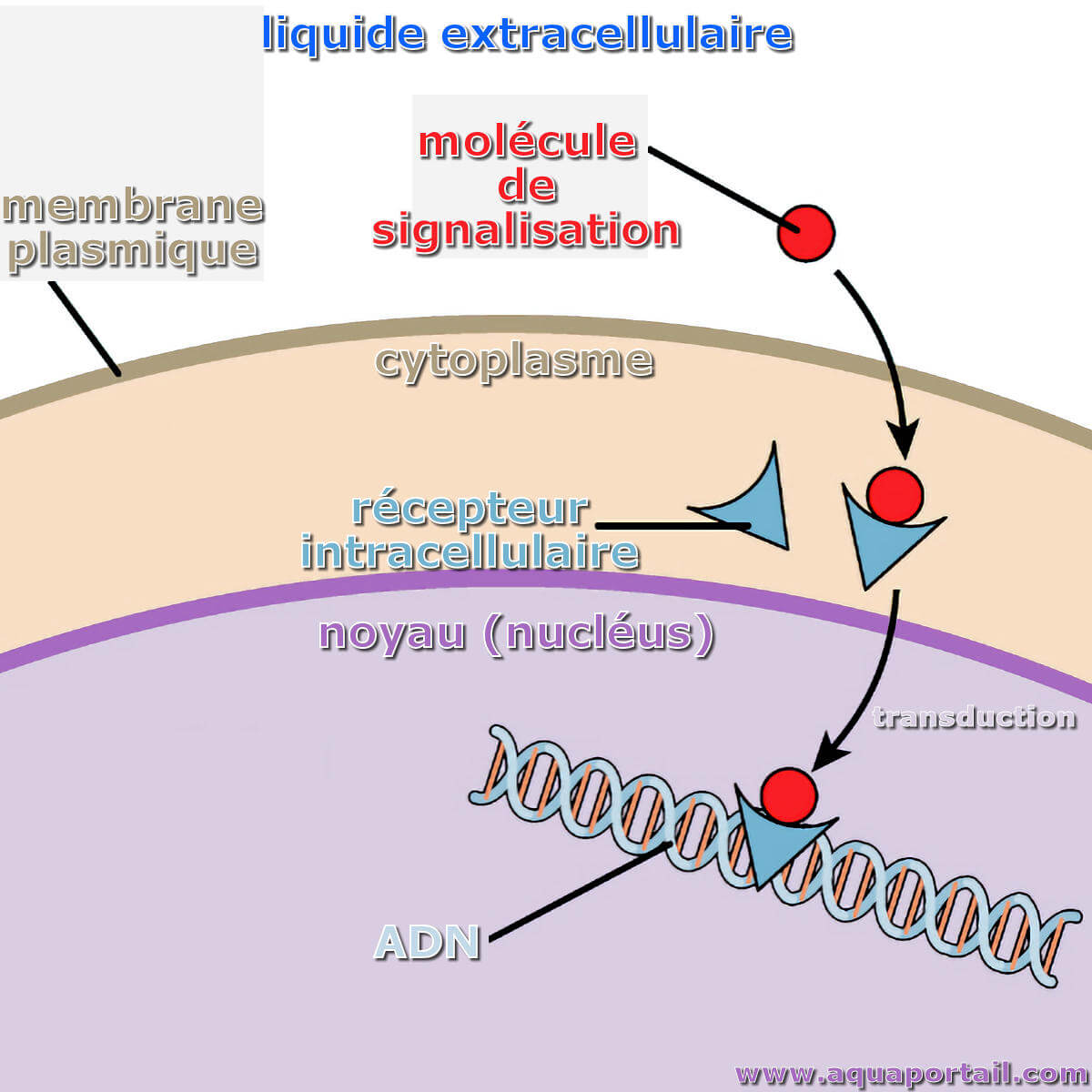
Une molécule de signal (signalisation cellulaire) est une molécule extracellulaire, de nature biochimique variée, qui donne une information à une cellule...
