Modèle de Bohr
Définition
Le modèle de Bohr représente les électrons comme des particules occupant des niveaux d'énergie distincts et quantifiés, visualisés sous forme d'anneaux concentriques autour du noyau. Chaque anneau, orbitale ou couche, correspond à un niveau d'énergie spécifique où résident les électrons, les couches externes indiquant des électrons possédant une énergie plus élevée.
Atome d'azote selon le modèle de Bohr :
Le modèle de Bohr d'un atome d'azote montre des protons et des neutrons dans le noyau et des électrons disposés en couches (orbitales atomiques) autour de celui-ci. Dans le modèle de Rutherford–Bohr, les électrons sont représentés par des points bleus disposés sur un anneau autour du noyau.
Explications
La théorie de Bohr a affiné le modèle atomique en introduisant des orbitales atomiques fixes (couches électroniques) pour le mouvement des électrons, chacune possédant un niveau d'énergie spécifique, contrairement à la théorie de Rutherford qui se concentrait sur le noyau.
Niels Bohr (1885–1962) a proposé trois idées principales entre 1911 et 1918 :
- 1. Les électrons orbitent autour du noyau sur des trajectoires circulaires discrètes, de rayons et d'énergies fixes, appelées états stationnaires, sans émettre d'énergie. L'équation est : En = (1/n2)E1. Son modèle a clarifié le mouvement des électrons dans des niveaux d'énergie stables, contrairement au mouvement indéfini de Rutherford.
- 2. Les électrons peuvent passer d'une orbite à une autre en absorbant ou en libérant une énergie égale à la différence entre leurs niveaux d'énergie, conformément au principe de conservation de l'énergie. L'absorption d'énergie fait passer les électrons à des niveaux d'énergie supérieurs (excitation), tandis que la libération d'énergie les fait passer à des niveaux inférieurs (relaxation), avec émission de photons. Si l'énergie du photon ne correspond pas à cette différence, aucune transition n'a lieu. Ces interactions sont fondamentales en spectroscopie : la spectroscopie d'absorption concerne les orbitales de haute énergie, et la spectroscopie d'émission concerne les transitions de basse énergie.
- 3. Le moment angulaire de l'électron est quantifié, déterminé par Ln = nh/2π, où n est le niveau de l'orbite et h est la constante de Planck.
Limitations
Le modèle atomique de Bohr, bien que révolutionnaire, présente plusieurs limitations.
Il combine des éléments de physique classique et quantique. Si le concept d'électrons se déplaçant sur des orbites circulaires provient de la physique classique, la quantification de leur quantité de mouvement et de leurs niveaux d'énergie repose sur les principes de la physique quantique.
Ce modèle n'explique pas de manière satisfaisante les "états stationnaires" des électrons. Autrement dit, il ne parvient pas à expliquer pourquoi les électrons restent sur leurs orbites spécifiques sans spiraler vers le noyau sous l'effet de l'attraction électrostatique.
De plus, le modèle de Bohr ne permet pas de prédire les intensités relatives ni la luminosité des raies spectrales. Ses prédictions sont très précises pour l'atome d'hydrogène, mais perdent en précision lorsque la charge nucléaire effective augmente dans les atomes ou les ions possédant un plus grand nombre de protons.
L'examen des raies spectrales à un grossissement plus élevé révèle une série de raies plus fines, appelées raies hyperfines. Le modèle de Bohr n'explique pas l'origine de ces raies hyperfines.
De plus, on observe un dédoublement des raies spectrales lorsqu'un échantillon de gaz est soumis à un champ électrique (effet Stark) ou à un champ magnétique (effet Zeeman). Le modèle de Bohr et ses postulats ne permettent pas d'expliquer ces phénomènes.
Synonymes, antonymes
Voir tous les synonymes pour "modèle de Bohr".2 synonymes (sens proche) de "modèle de Bohr" :
- modèle de Rutherford–Bohr
- théorie de Bohr
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à MODÈLE DE BOHR sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
L'expression MODELE DE BOHR est dans la page 4 des mots en M du lexique du dictionnaire.
Mots en M à proximité
MNHN mobilité mode abrité mode battu mode d'appariementmodèle de Bohrmodification modification post-traductionnelle modification racémique moelle moelle épinière
En rapport avec "modèle de Bohr"
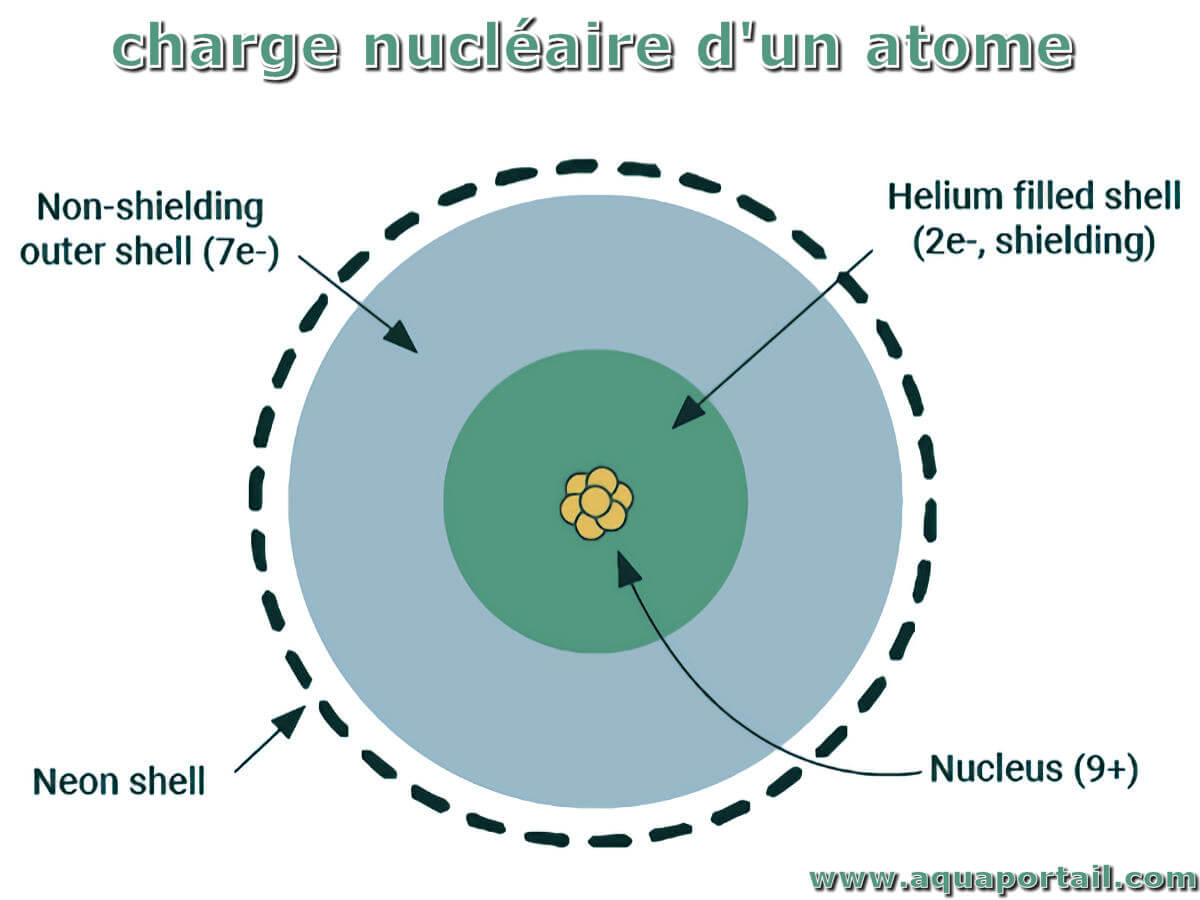
La charge nucléaire est une mesure de l'effet du nombre de protons dans le noyau et de leur capacité à attirer les électrons négatifs en orbite autour...

En physique atomique, une couche électronique, en rapport avec le niveau énergétique d'un atome, peut être considérée comme l'ensemble des orbites suivies...

Une orbitale atomique fait référence à une équation mathématique qui décrit l'énergie et la probabilité de trouver des électrons dans une région spécifique...
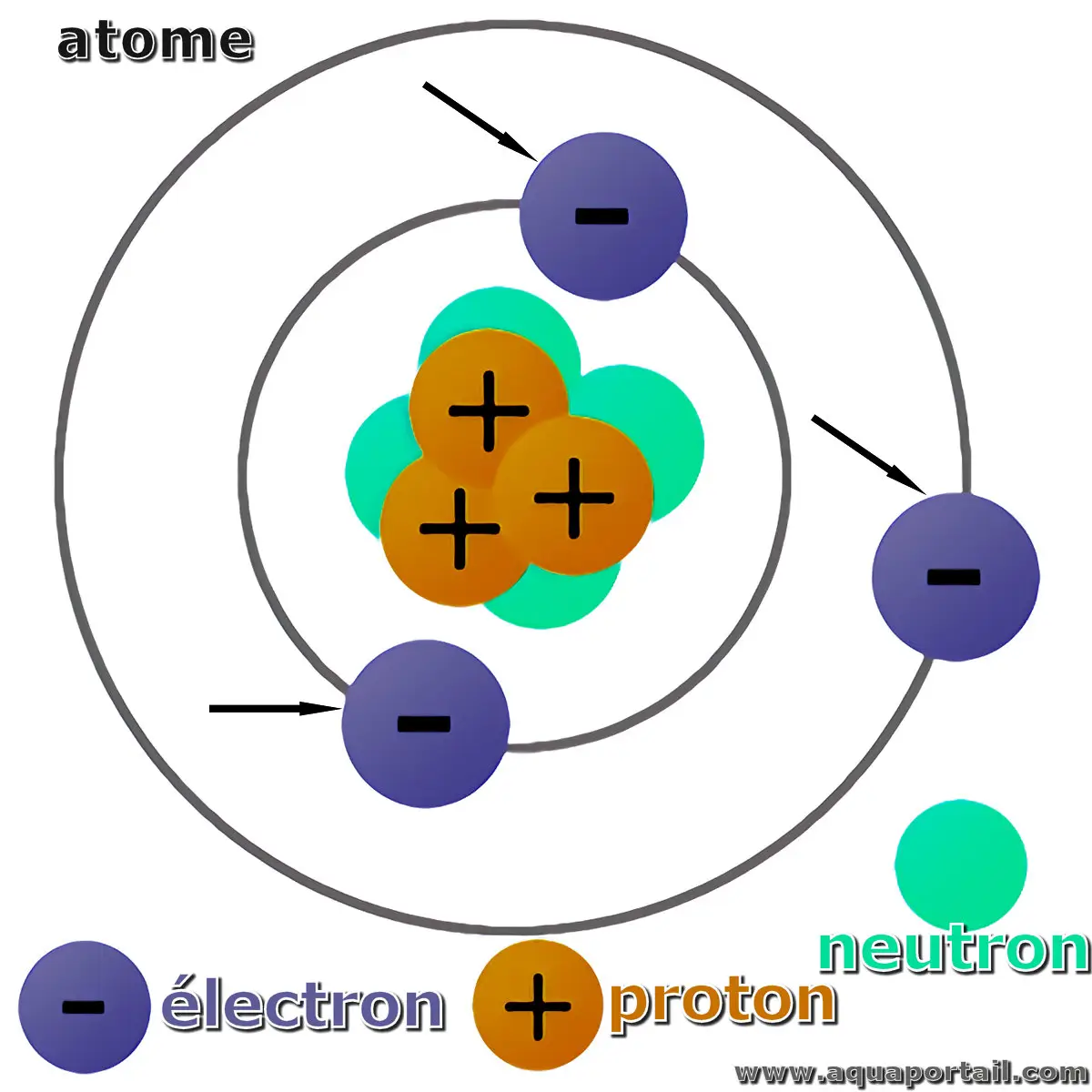
L'électron (e⁻) est une particule élémentaire chargée négativement. Les électrons liés par un atome ou un ion forment sa couche d'électrons.
