Apoptose
Définition
L'apoptose, ou mort cellulaire programmée, est un processus contrôlé au cours duquel une cellule subit des modifications moléculaires conduisant à sa destruction et son élimination. Elle aide l'organisme à supprimer les cellules superflues ou dysfonctionnelles, sans provoquer d'inflammation.
Processus d'apoptose :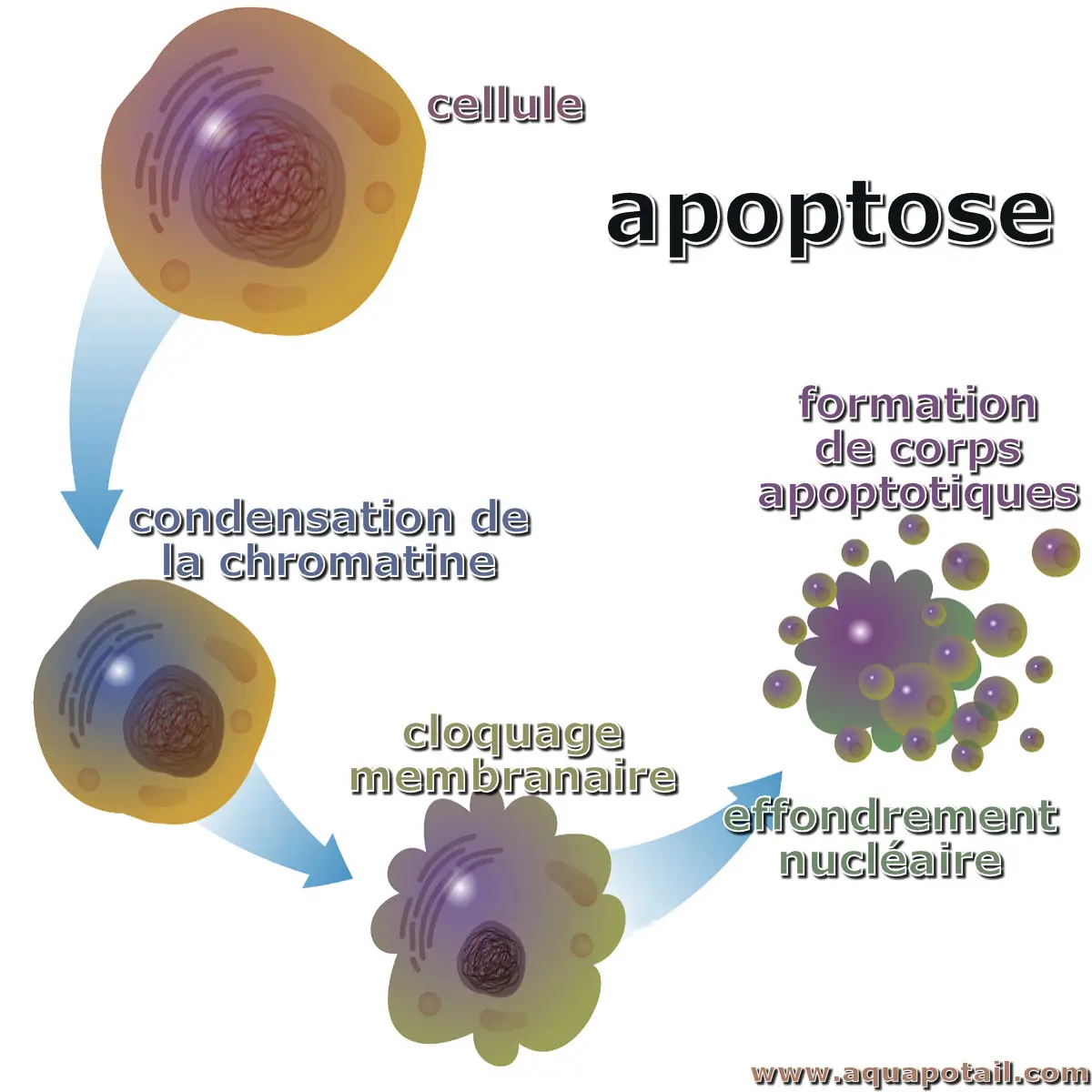
L'apoptose désigne un processus appelé mort cellulaire programmée, comme si la cellule se suicidait. Lorsque cela intervient, une chorégraphie de voies et de protéines cellulaires s'active pour la tuer sans trop de dégâts. Ainsi, l'apoptose est un processus génétiquement dirigé d'autodestruction cellulaire, caractérisé par la fragmentation de l'ADN nucléaire et activé par la présence d'un stimulus.
Explications
L'apoptose est le processus de mort cellulaire programmée. Elle est utilisée au début du développement pour éliminer les cellules indésirables, par exemple celles situées entre les doigts d'une main en développement. Chez l'adulte, l'apoptose sert à débarrasser l'organisme des cellules irrémédiablement endommagées.
Mécaniquement, l'apoptose est un processus génétiquement régulé d'autodestruction cellulaire, caractérisé par la fragmentation de l'ADN nucléaire. Elle peut être initiée en réponse à des stimuli spécifiques, jouant ainsi un rôle essentiel dans le maintien de l'homéostasie cellulaire et de la santé des tissus.
Le processus d'apoptose peut être bloqué dans les cellules cancéreuses. L'apoptose survient normalement dans les cellules présentes dans l'organisme depuis assez longtemps pour être usées et devoir laisser la place à de nouvelles cellules jeunes et bien portantes. L'apoptose peut donc être normale, et son absence peut conduire au cancer.
Apoptose et nécrose d'une cellule :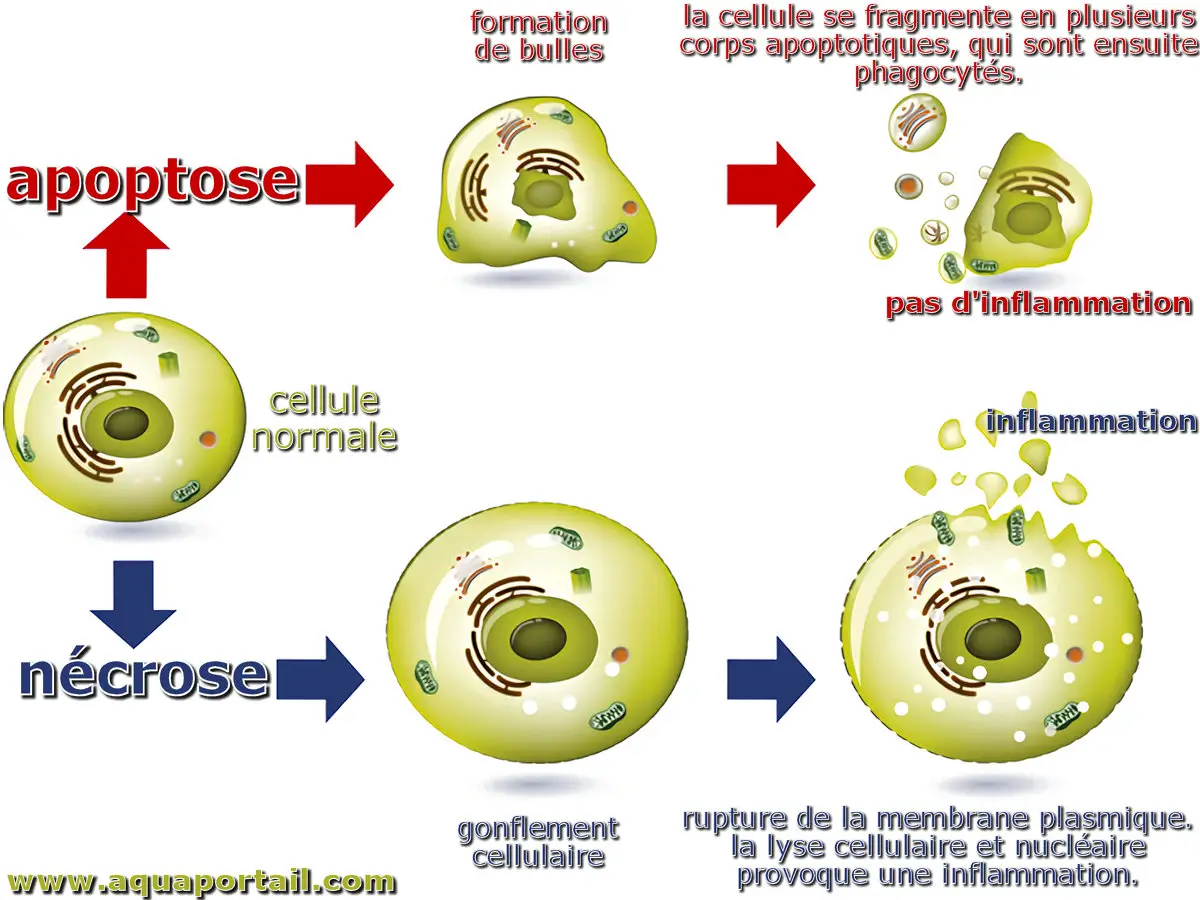
L'apoptose est un type de mort cellulaire programmée où une série d'étapes moléculaires entraîne la mort d'une cellule. C'est une méthode utilisée par l'organisme pour se débarrasser des cellules inutiles ou anormales. L'apoptose ne provoque aucune inflammation quand la nécrose induit une inflammation tissulaire à cause des cellules détruites. La ferroptose est un modèle spécifique de nécrose.
Une apoptose excessive chez un être humain peut entraîner plusieurs maladies dites neurodégénératives, où les cellules meurent alors qu'elles ne sont pas censées mourir. Elles reçoivent des messages d'un endroit, que nous ignorons pour la plupart, leur ordonnant de mourir. C'est ce qui existe dans une certaine partie de la partie inférieure du cerveau, provoquant la maladie de Parkinson. C'est également le cas de la maladie de Huntington, de la maladie d'Alzheimer, de la maladie de Charcot et de plusieurs autres maladies neurodégénératives.
lire plus de détails pour l'apoptose...
Synonymes, antonymes
Voir tous les synonymes pour "apoptose".2 synonymes (sens proche) de "apoptose" :
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à APOPTOSE sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
Le mot APOPTOSE est dans la page 7 des mots en A du lexique du dictionnaire.
Mots en A à proximité
apophyse apoplasme apoplaste apoprotéine apoptogène apoptoseapoptotique apopyle aporogamie aposématique aposématisme
En rapport avec "apoptose"
L'autolyse est un processus par lequel une cellule s'autodétruit. L'autolyse est une destruction (lyse autogène) de cellules ou de tissus par leurs propres...

La ferroptose est un type de mort cellulaire programmée, une nécrose caractérisée par une peroxydation lipidique dépendante du fer, aboutissant...
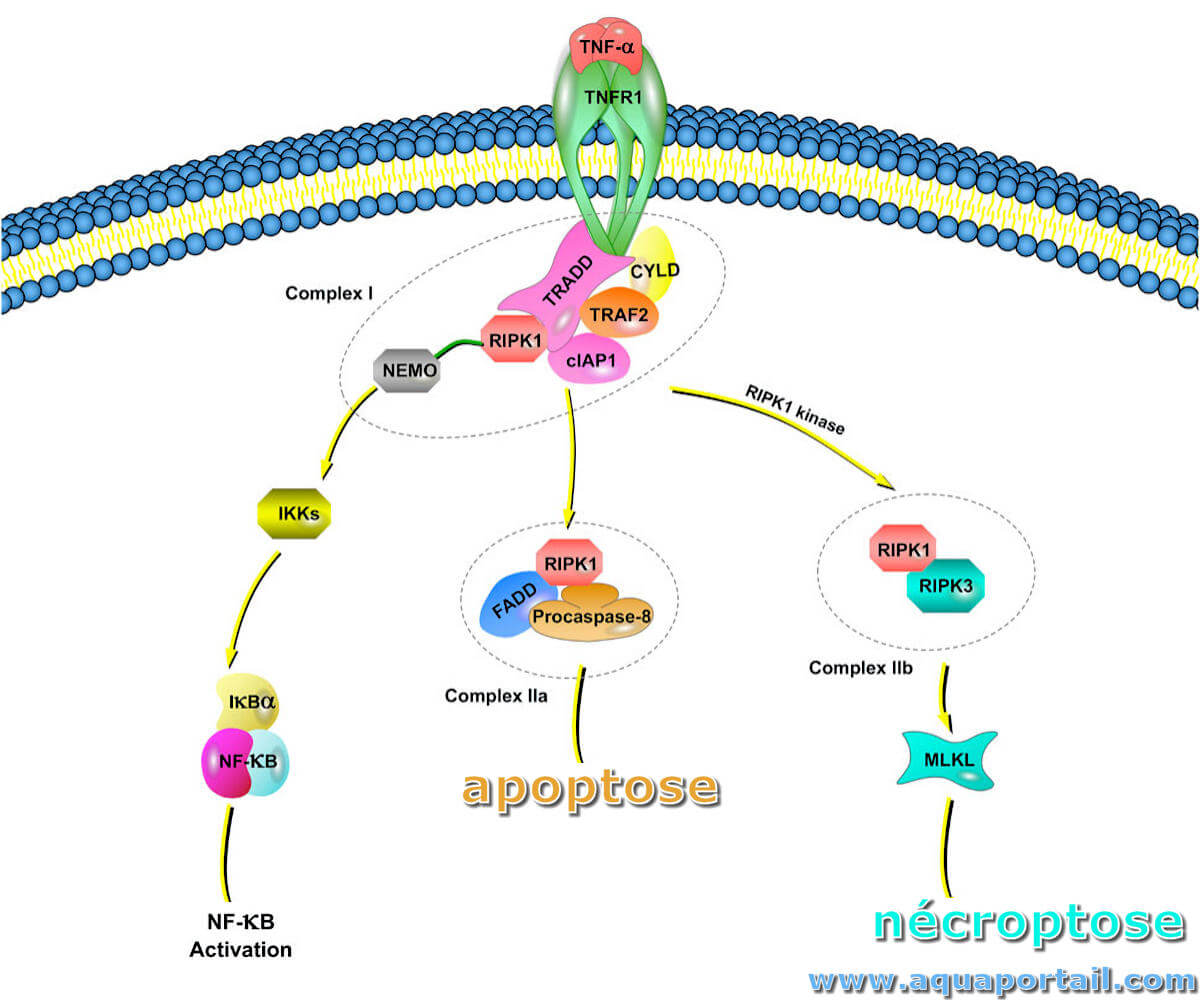
La nécroptose est une version régulée de la voie de mort cellulaire nécrotique, indépendante de la caspase.
La nécrose est la dernière étape de la mort cellulaire. En biologie, la nécrose est la mort et la décomposition d'un tissu organique. Elle est une altération...
