Hématie (érythrocyte)
Définition
Une hématie est un type de cellule sanguine (érythrocyte ou globule rouge) produit dans la moelle osseuse. Sa principale fonction, comme tout globule rouge, est de transporter l'oxygène et autres gaz des poumons vers tout l'organisme.
Des hématies (érythrocytes) :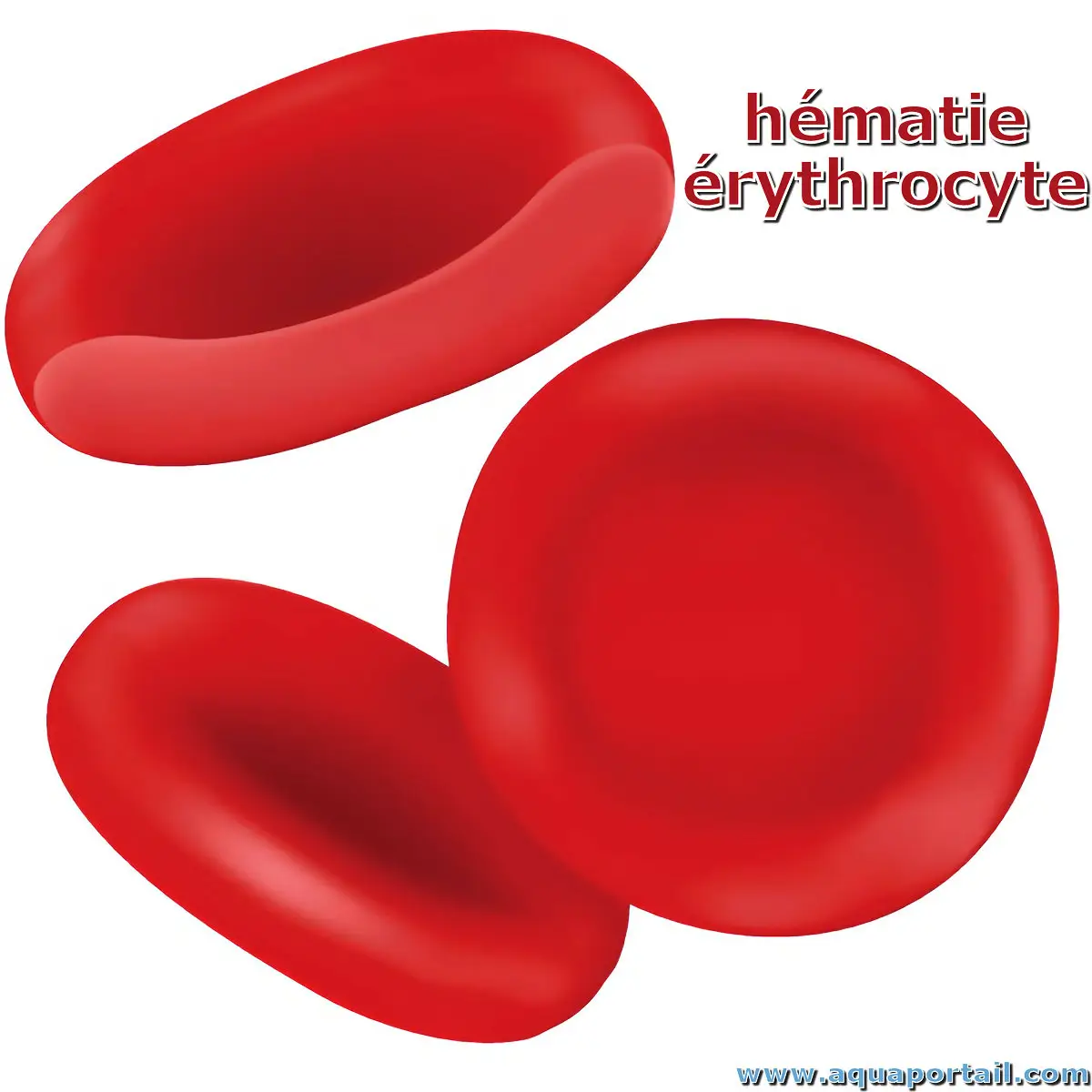
Les hématies sont un type de cellules sanguines fabriquées dans la moelle osseuse et présente dans le sang. Chez les mammifères, elles sont aussi appelées les érythrocytes.
Explications
Une hématie est généralement de forme biconcave et dépourvue de noyau chez l'humain. Les hématies contiennent l'hémoglobine, un pigment qui donne sa couleur rouge au sang et transporte l'oxygène et le dioxyde de carbone vers et depuis les tissus.
Les hématies sont les composants fonctionnels du sang responsables du transport des gaz et des nutriments dans l'organisme humain. Elles transportent également les déchets, comme le dioxyde de carbone, vers nos poumons pour être expirés. Leur forme et leur composition uniques permettent à ces cellules spécialisées d'assurer leurs fonctions essentielles. Le rôle des hématies est crucial dans l'étude de nombreux processus pathologiques touchant divers systèmes de l'organisme.
Chez les mammifères, une hématie s'appelle un érythrocyte, mais elle prend d'autres appellations chez d'autres animaux (anisocytes et poïkilocytes). Les hématies humaines vivent environ 120 jours dans la moelle osseuse où elles sont produites..
Formes des diverses hématies :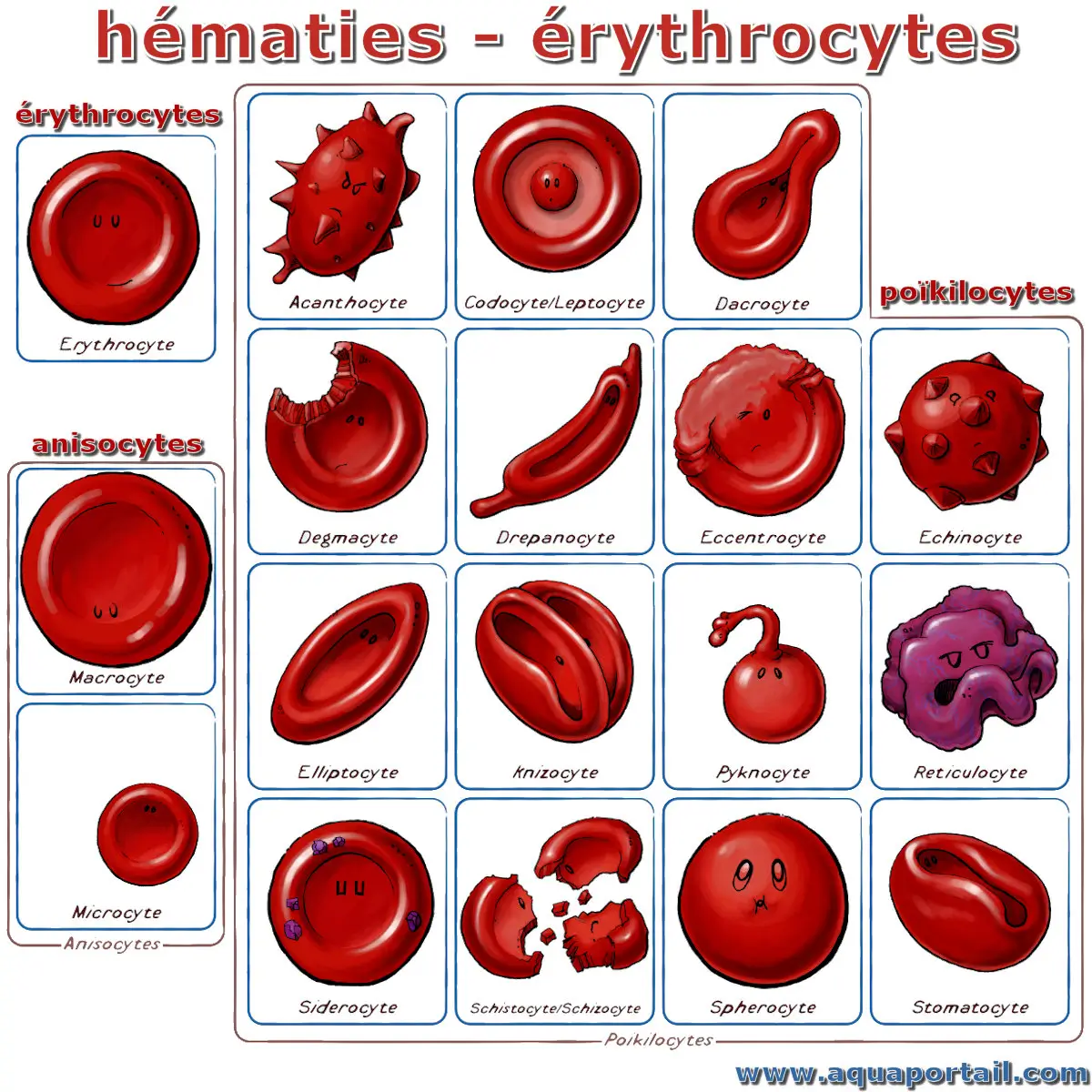
Les différents types d'hématies, dont les 3 principaux groupes : érythrocites, anisocytes et poïkilocytes.
Les hématies peuvent être visualisées par microscopie optique et microscopie électronique, chacune révélant des détails spécifiques de la structure des érythrocytes.
Une hématie (érythrocyte) en rouge :
L'hématie apparaît à droite (en rouge) accompagnée d'une cellule de plaquette sanguine (thrombocyte, au milieu, jaune) et un lymphocyte T (à gauche, bleu).
lire plus de détails pour une hématie...
Synonymes, antonymes
Voir tous les synonymes pour "hématie".6 synonymes (sens proche) de "hématie" :
1 antonyme (sens contraire) :
Les mots ou les expressions apparentés à HÉMATIE sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
Le mot HEMATIE est dans la page 1 des mots en H du lexique du dictionnaire.
Mots en H à proximité
helobios hélocrène hélophyte héma-hémohémagglutination hématiehématocrite hématocyte hématogène hématologie hématophage
En rapport avec "hématie"
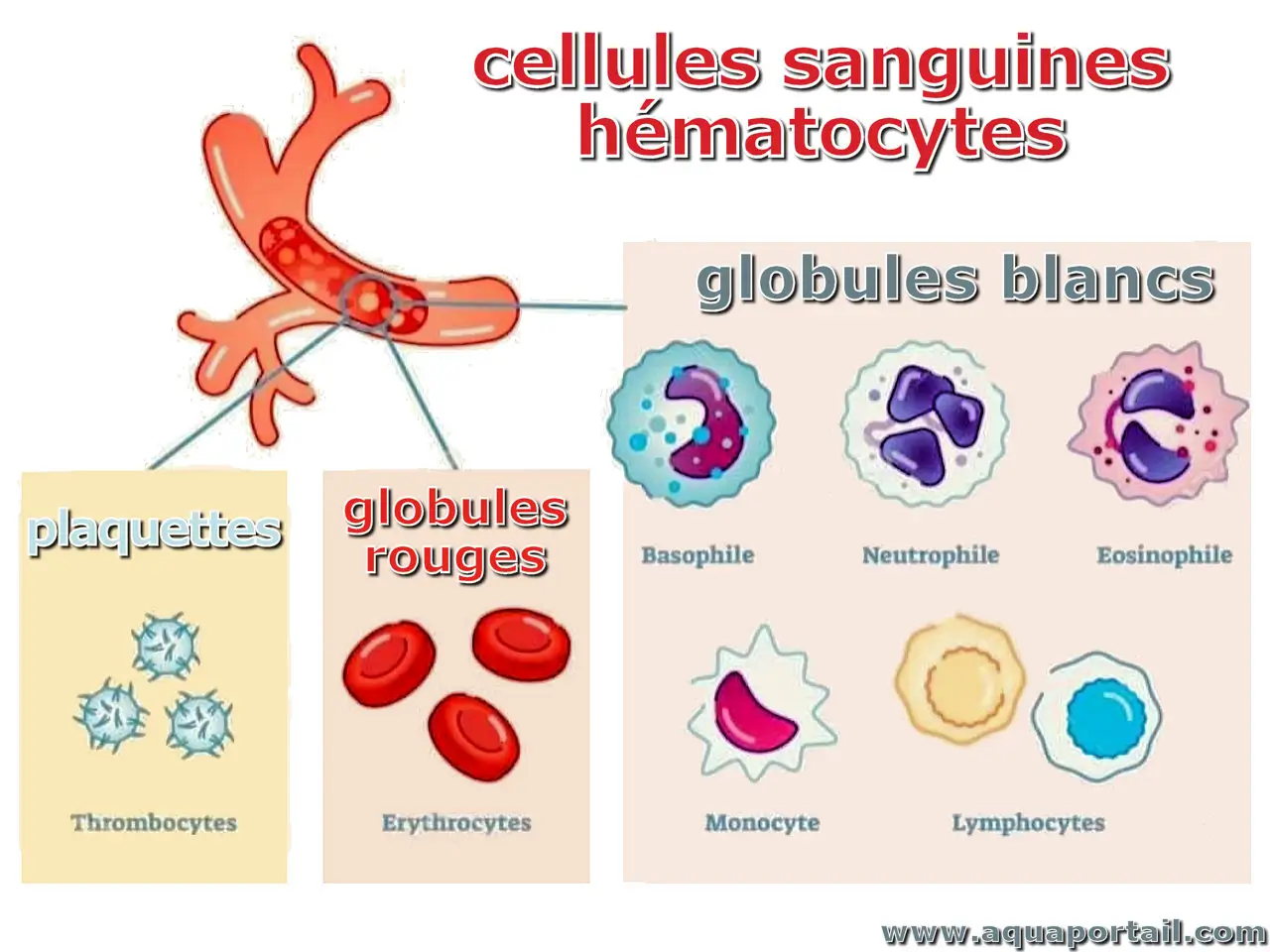
Une cellule sanguine (hématocyte) est l'un des trois organites du sang (plaquettes sanguines, globules blancs, globules rouges) produits par hématopoïèse.

Un globule rouge (érythrocyte, hématie) est le principal élément du sang, sous la forme d'un globule sanguin.
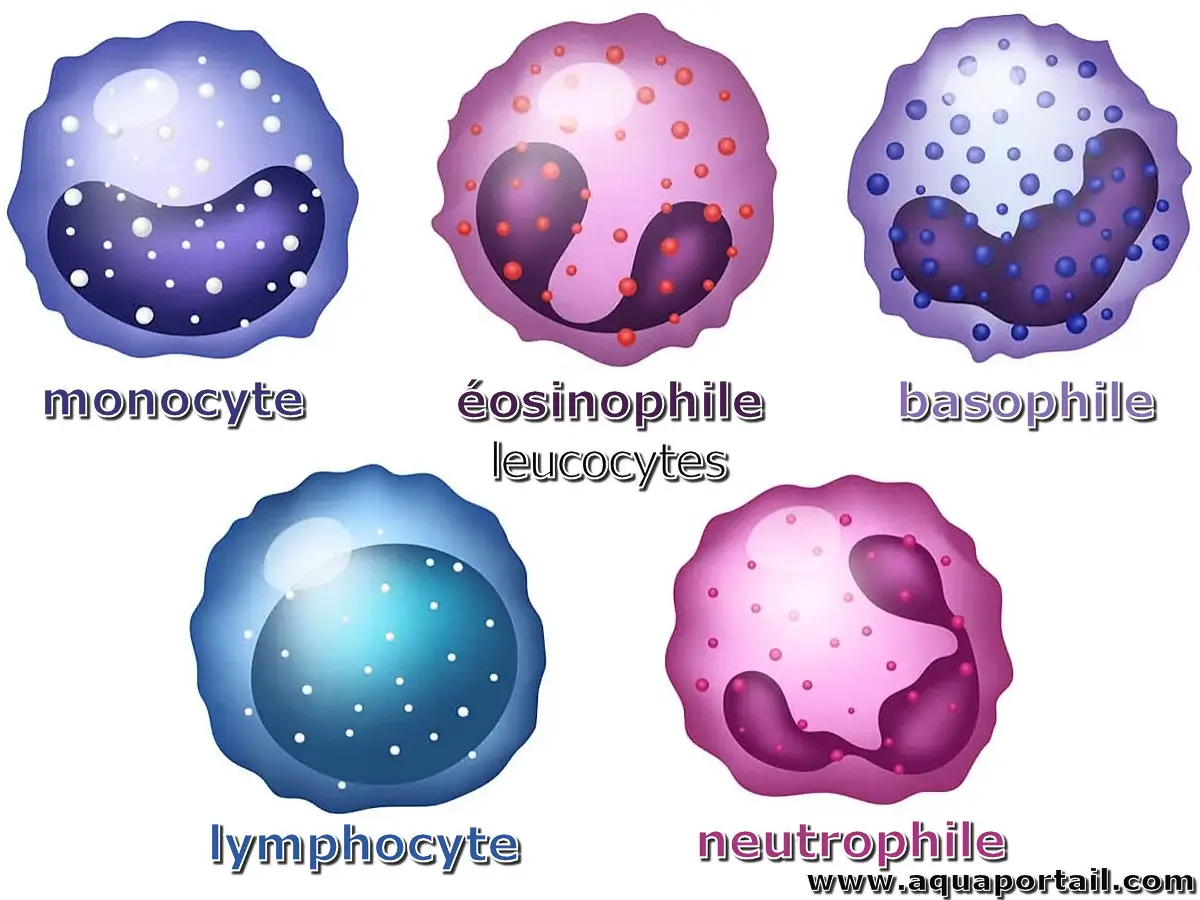
Les leucocytes regroupent un ensemble de cellules qui régissent l'immunité innée et adaptative.
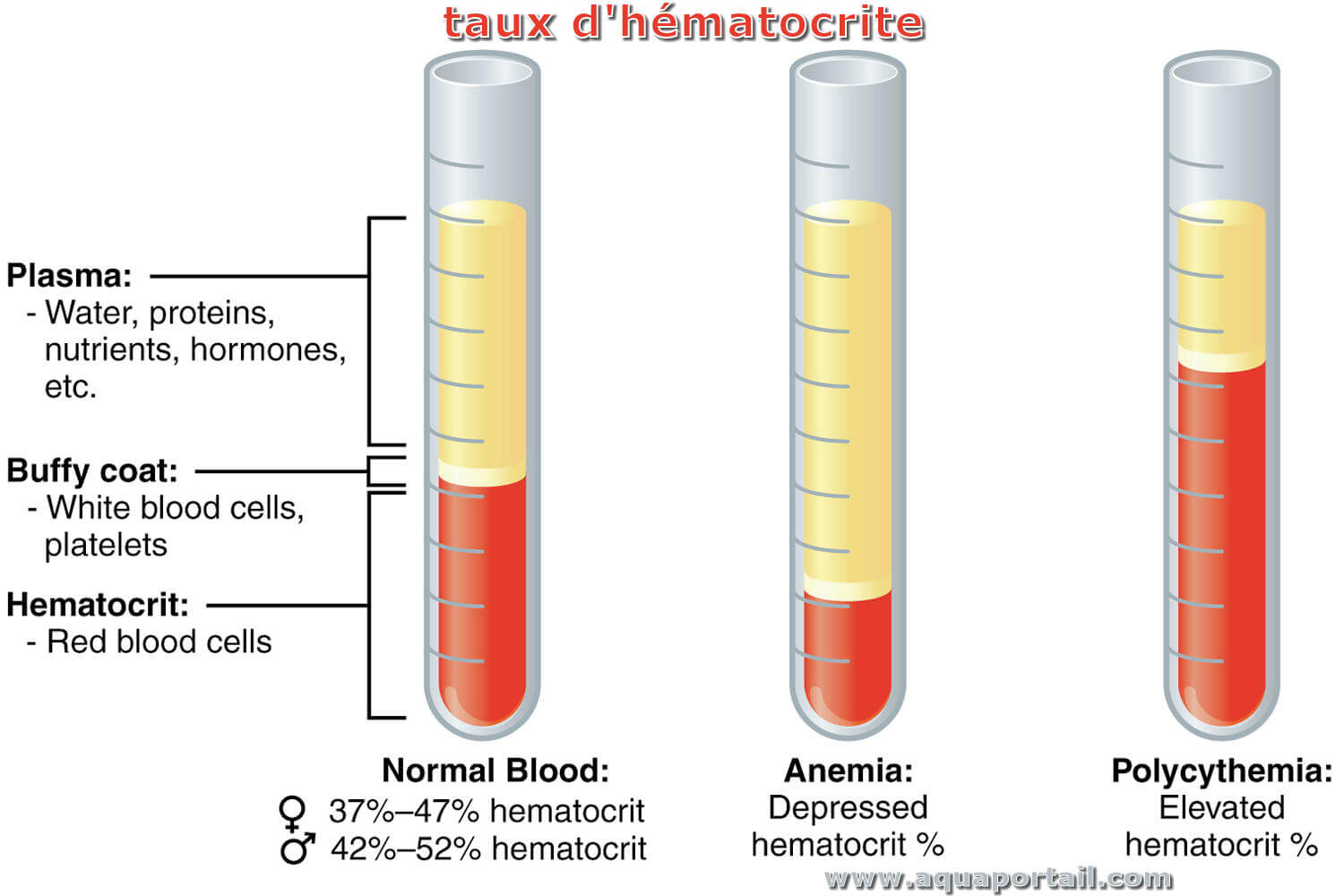
Un hématocrite est le rapport du volume des globules sanguins (hématies) sur le volume sanguin total.
