Gaz dissous
Définition
Un gaz dissous est tout simplement un gaz qui a été dissous dans un autre matériau. Cela crée une solution, un mélange, dans lequel le gaz est le soluté, le composant mineur, et l'autre matériau, généralement un liquide, est le solvant, le composant principal.
Les eaux naturelles sont plus ou moins en contact avec l'air. La plupart des gaz dissous sont absorbés dans l'air ainsi que le CO2 qui peut provenir en partie du sol et des roches en contact avec l'eau.
Les gaz dissous dans l'eau :
Les gaz dissous existent dans la plupart des eaux naturelles (douces ou marines) ou purifiées.
Explications
Voir aussi le dégazage de l'eau (les gaz dissous sont l'oxygène et l'hydrogène) et le dégagement d'oxygène.
Toute eau purifiée est produite en éliminant les impuretés des eaux naturelles ou municipales. Il est utile de considérer les gaz éventuellement présents dans ces eaux d'alimentation, leur devenir au fur et à mesure que les eaux sont purifiées et toute contamination potentielle par ces mêmes gaz ou par d'autres gaz pendant ou après la purification.
Les eaux municipales sont obtenues en traitant les eaux naturelles pour les rendre potables. Ces processus ont tendance à avoir très peu d'effet sur la teneur en gaz dissous de l'eau, augmentant généralement leur contact avec l'air ambiant et réduisant la variabilité due aux sources locales.
Chaque gaz atmosphérique est en équilibre avec le gaz dissous dans l'eau. La quantité dissoute dans l'eau dépend de la température et de la pression partielle du gaz dans l'atmosphère.
La quantité maximale d'un gaz pur pouvant être dissoute par unité de volume est appelée la solubilité du gaz. La concentration molaire d'un gaz, i, dissous dans l'eau au contact de l'air est donnée par : [gazi](aq) = Pi/K où Pi est sa proportion volumique dans l'air et K est sa constante d'équilibre.
Dans l'eau
Les concentrations de gaz dissous dans l'eau varient en fonction de la température, de la pression atmosphérique et de l'emplacement. En résumé, dans l'eau d'alimentation destinée à la purification, il y a des concentrations d'oxygène et d'azote à des niveaux de moins de 10 ppm et seulement des traces de gaz rares. Le niveau de CO2 dans l'eau est influencé par d'autres facteurs.
Les effets des technologies standards de purification de l'eau sur l'oxygène dissous, l'azote et les gaz inertes sont négligeables. Ces gaz passeront directement à travers les membranes d'osmose inverse, la lumière UV, les micro et ultrafiltres, les résines échangeuses d'ions et les unités d'électrodéionisation (déionisation EDI) et n'utiliseront aucune capacité des médias de purification.
Tout effet mineur dû, par exemple, à des changements locaux de pression aura tendance à être compensé par un équilibrage avec l'atmosphère de tout récipient de stockage.
L'eau d'alimentation provenant des approvisionnements municipaux est susceptible de se réchauffer lorsqu'elle est purifiée en laboratoire et, par conséquent, l'eau purifiée est plus susceptible d'être saturée en azote et en oxygène.
Gaz carbonique
Le dioxyde de carbone se comporte très différemment des autres gaz présents dans l'air. Lorsqu'il se dissout dans l'eau, il réagit pour établir une série d'équilibres :
Équation du CO2 dissous dans l'eau : CO2 + H2O ↔ H2CO3 ↔ H+ + HCO3- ↔ 2H+ + CO32-.
Une petite fraction du dioxyde de carbone dissous dans l'eau réagit rapidement pour former de l'acide carbonique. Celui-ci, à son tour, se dissocie partiellement pour former des ions hydrogène, bicarbonate et carbonate. Le CO2 continuera à se dissoudre jusqu'à ce que l'équilibre soit atteint.
La situation est encore compliquée par la présence d'ions carbonate et bicarbonate dans les eaux naturelles dures. Ces concentrations peuvent être relativement élevées, entraînant des niveaux élevés d'acide carbonique et de CO2 dissous. Dans ces circonstances, les concentrations de CO2 dissous peuvent atteindre 60 ppm ou plus.
Comme les autres gaz, le CO2 passera inchangé à travers les filtres et le traitement UV. Cependant, en raison de son équilibre avec les ions bicarbonate et carbonate, il peut en effet être retenu sur les résines échangeuses d'anions. Au fur et à mesure que les ions bicarbonate et carbonate sont éliminés de la résine, davantage de CO2 se transformera en bicarbonate jusqu'à ce qu'il n'en reste plus.
Eau ultrapure
Après avoir éliminé les gaz dissous pour purifier l'eau, l'eau ultrapure contenue dans le purificateur a une résistivité de 18,15 MΩ.cm et contient des niveaux inférieurs au ppb de toutes les impuretés, à l'exception de l'oxygène et de l'azote dissous.
Dès que cette eau ultrapure est versée dans un récipient du laboratoire, elle entre en contact avec l'air. Les teneurs en oxygène et en azote ne changent pas de manière significative mais le CO2 sera rapidement absorbé de l'air.
Des ions hydrogène, bicarbonate et carbonate seront produits et la résistivité tombera à environ 1,3 MΩ.cm. Dans la pratique normale de laboratoire, cela est inévitable. La conductance élevée des ions hydrogène fait que ce changement ne correspond qu'à une concentration de 0,5 mg/L de CO2 en solution.
Cela n'affecte pas la plupart des expérimentations et, avec de bonnes pratiques de laboratoire, la pureté de l'eau n'est pas affectée par ailleurs.
Synonymes, antonymes
Voir tous les synonymes pour "gaz dissous".0 synonyme (sens proche) pour "gaz dissous".
0 antonyme (sens contraire).
Les mots ou les expressions apparentés à GAZ DISSOUS sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
L'expression GAZ DISSOUS est dans la page 1 des mots en G du lexique du dictionnaire.
Mots en G à proximité
gaz à effet de serre gaz carbonique gaz CFC gaz de schiste gaz de synthèse gaz dissousgaz fossile gaz inerte gaz naturel gaz noble gaz rare
En rapport avec "gaz dissous"
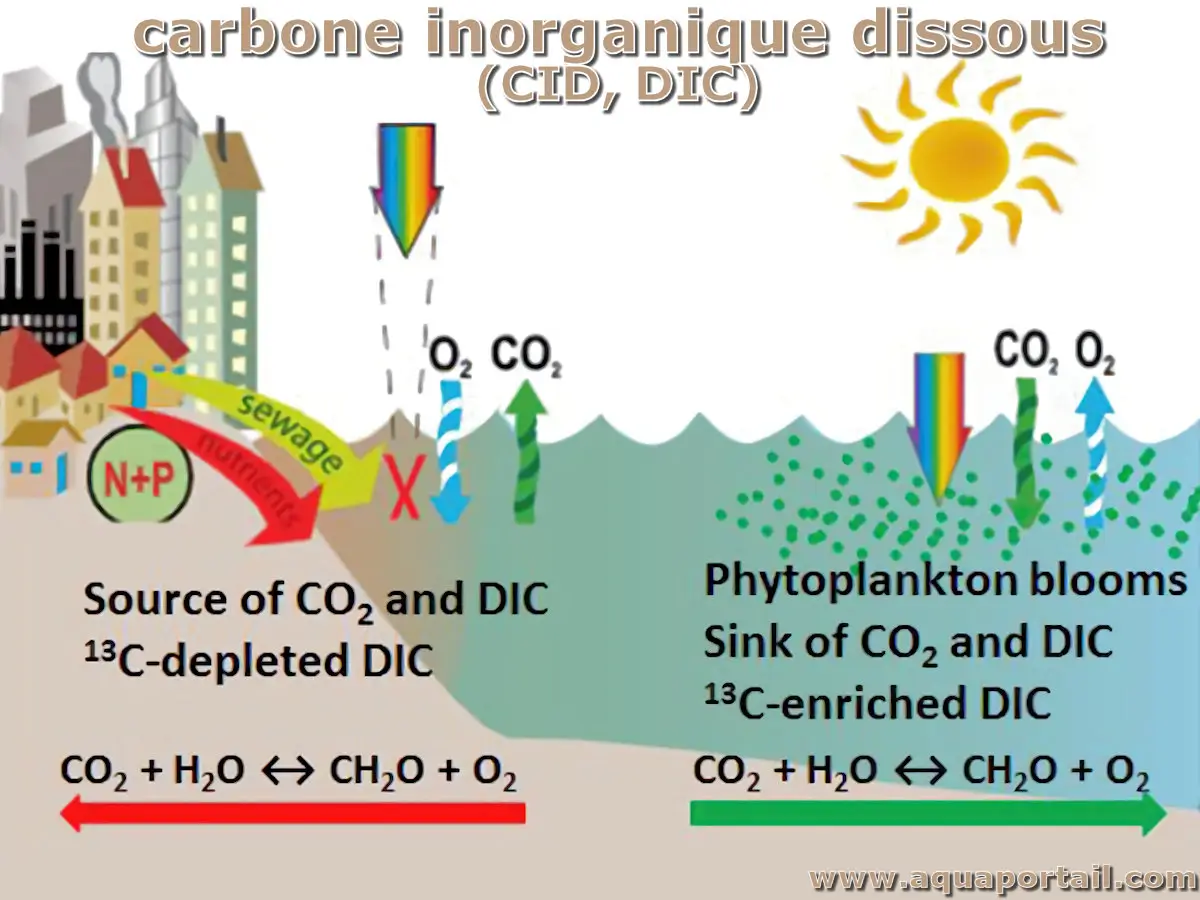
Le carbone inorganique dissous (CID) est l'ensemble du dioxyde de carbone (CO₂), des ions bicarbonate (HCO₃⁻) et des ions carbonate (CO₃²⁻) présents dans...
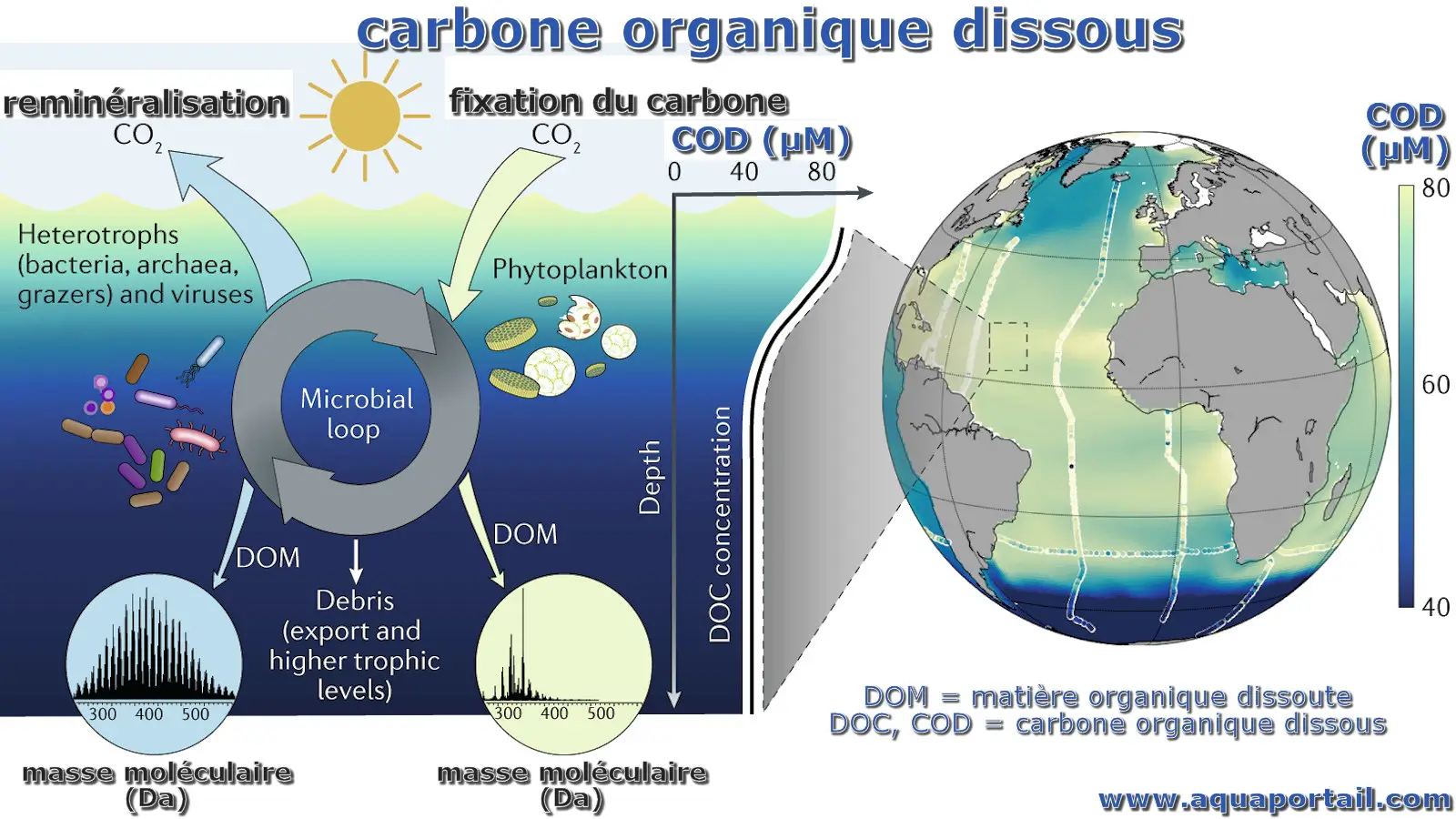
Le carbone organique dissous (COD) est la fraction de matière organique qui est en mesure de traverser un filtre, dont la taille des pores varie généralement...
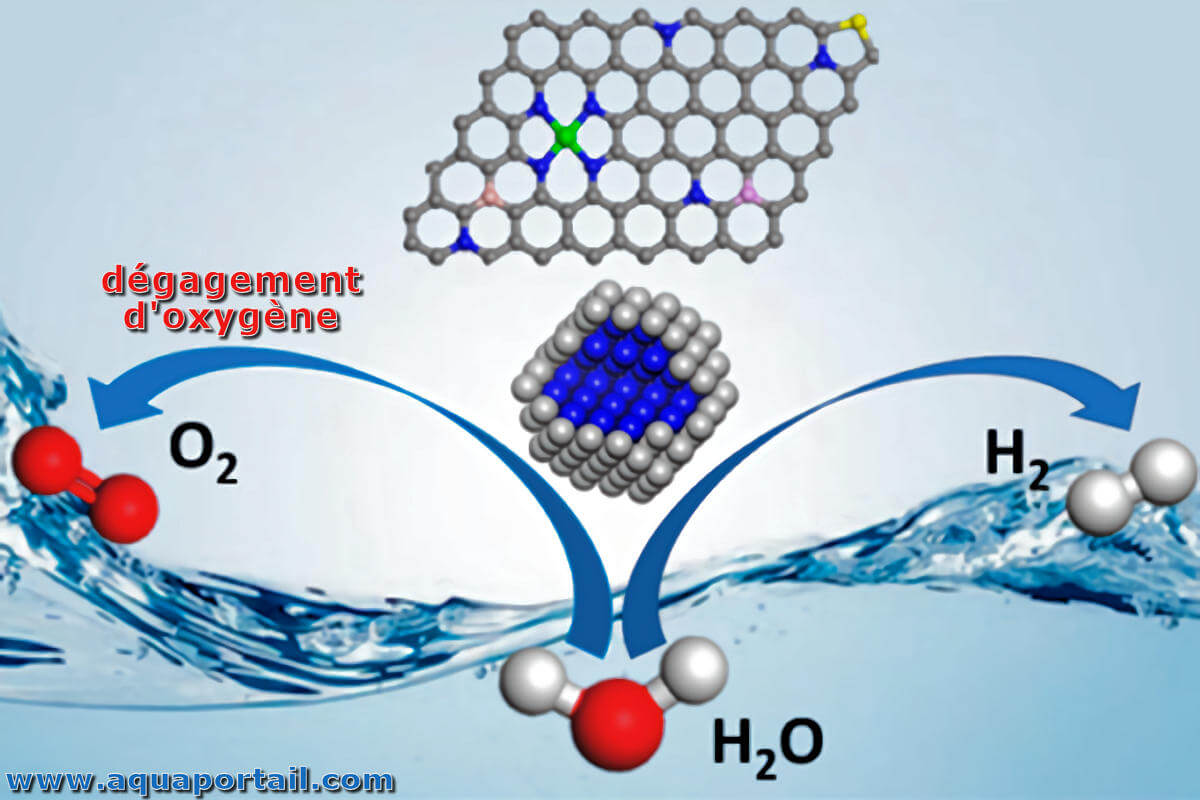
Le dégagement d'oxygène est le processus consistant à générer de l'oxygène moléculaire au travers d'une réaction chimique.

Le dégazage est un transfert mécanique des gaz dissous dans l'eau vers l'air par une action d'agitation de l'eau.
