Spectre d'absorption
Définition
Le spectre d'absorption d'un matériau est la fraction du rayonnement incident absorbé par le matériau sur une plage de fréquences. Les différents éléments ont des spectres différents car ils ont des compositions atomiques différentes.
Voici le spectre d'absorption de la chlorophylle en lumière visible :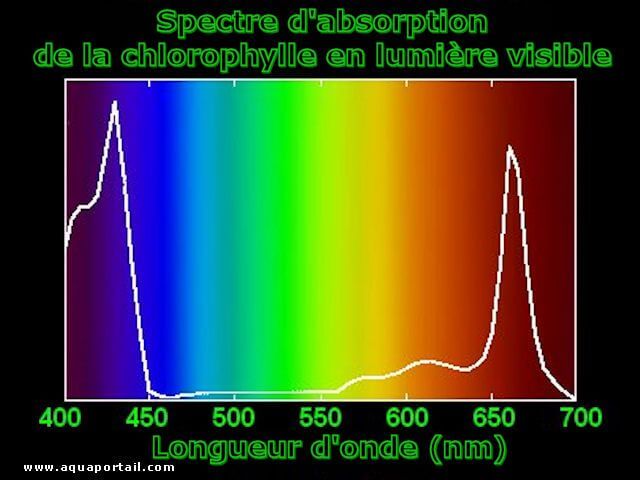
Le spectre d'absorption de la chlorophylle en lumière visible dispose de deux pics. La chlorophylle "a" absorbe principalement dans le bleu (entre 400 et 500 nm) et le rouge (autour de 650 à 680 nm). La chlorophylle "b" absorbe principalement la lumière bleue et jaune.
Explications
Le spectre d'absorption d'un matériau indique la fraction de rayonnement électromagnétique incidente absorbée dans une certaine gamme de fréquences. Il est, en un sens, à l'opposé du spectre d'émission.
Le spectre d'absorption est déterminé par la quantité de lumière absorbée par un composé, en fonction de la longueur d'onde (exprimée en nanomètres). La mesure se réalise par spectroscopie et spécialement la spectroscopie d'absorption pour les éléments spectroscopiques.
Propriétés
Chaque élément chimique possède ses propres lignes d'absorption correspondant aux longueurs d'onde spécifiques et des différences relatives entre les niveaux d'énergie de ses orbitales atomiques.
Par exemple, un objet qui absorbe le bleu, le vert et le jaune apparaîtra rouge lorsqu'il est éclairé par une lumière blanche, en simplifiant aux couleurs fondamentales. Pour cette raison, le spectre d'absorption peut être utilisé pour identifier les éléments présents dans un gaz ou un liquide. Cette méthode est appliquée pour déduire la présence d'éléments en étoiles et d'autres objets gazeux qui ne peuvent pas être mesurés directement.
Voir aussi spectre lumineux, spectre visible, spectre ultraviolet, spectre d'émission, spectre d'action, spectre infrarouge.
La spectroscopie d'absorption regroupe un ensemble de techniques spectroscopiques. La spectroscopie d'absorption est réalisée sur le spectre électromagnétique. Ce type de techniques est basé sur l'absorption d'un rayonnement électromagnétique à différentes longueurs d'onde des matériaux produisant un spectre généralement exprimé en nombre d'ondes et en absorbance ou en facteur de transmission. Les techniques d'absorption comprennent la spectroscopie d'absorption atomique.
Le spectre d'absorption d'un matériau est la fraction du rayonnement incident absorbé par le matériau sur une plage de fréquences. Le spectre d'absorption est principalement déterminé par la composition atomique et moléculaire du matériau. Les radiations sont plus susceptibles d'être absorbées à des fréquences correspondant à la différence d'énergie entre deux états de la mécanique quantique des molécules. L'absorption qui intervient en raison d'une transition entre deux états est appelée raie d'absorption et un spectre est généralement composé de nombreuses raies.
L'absorption photosynthétique avec mesure du taux de photosynthèse en fonction du spectre d'absorption :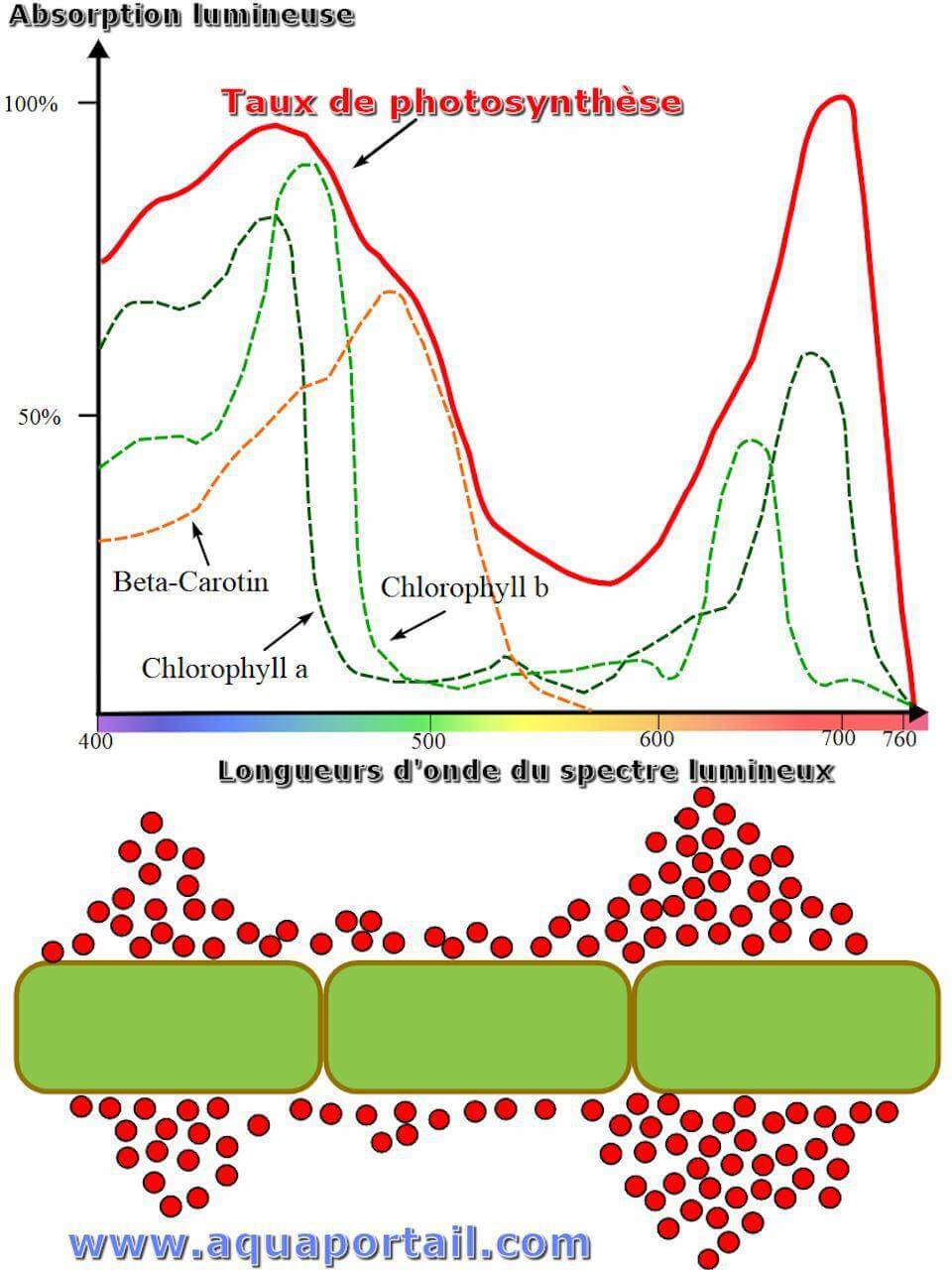
évolution de l'absorption des chlorophylles lors de la photosynthèse.
Les fréquences d'apparition des raies d'absorption, ainsi que leurs intensités relatives, dépendent principalement de la structure électronique et moléculaire de l'échantillon. Les fréquences dépendront également des interactions entre les molécules de l'échantillon, de la structure cristalline dans les solides et de plusieurs facteurs environnementaux (par exemple, la température, la pression, le champ électromagnétique). Les lignes auront également une largeur et une forme qui sont principalement déterminées par la densité spectrale ou la densité d'états du système.
Relation au spectre d'émission
L'émission est un processus par lequel une substance libère de l'énergie sous forme de rayonnement électromagnétique. L'émission peut exister à n'importe quelle fréquence d'absorption, ce qui permet de déterminer les raies d'absorption à partir d'un spectre d'émission. Le spectre d'émission aura typiquement un motif d'intensité assez différent du spectre d'absorption, cependant, les deux ne sont pas équivalents.
Le spectre d'absorption peut être calculé à partir du spectre d'émission en utilisant des modèles théoriques appropriés et des informations supplémentaires sur les états de la mécanique quantique.
Relation au spectre de transmission
Les spectres d'absorption et de transmission représentent des informations équivalentes et l'une peut être calculée à partir de l'autre au moyen d'une transformation mathématique. L'intensité maximale d'un spectre de transmission se situe aux longueurs d'onde où l'absorption est la plus faible, car davantage de lumière est transmise à travers l'échantillon. Un spectre d'absorption aura ses intensités maximales aux longueurs d'onde où l'absorption est la plus forte.
Relation aux spectres de diffusion et de réflexion
Les spectres de diffusion et spectres de réflexion d'un matériau sont influencés à la fois par son indice de réfraction et son spectre d'absorption. Dans un contexte optique, le spectre d'absorption est typiquement quantifié par le coefficient d'extinction, et les coefficients d'extinction et d'indice sont reliés quantitativement par la relation de Kramers-Kronig. Par conséquent, le spectre d'absorption peut être dérivé d'un spectre de diffusion ou de réflexion. Cela nécessite généralement de simplifier des hypothèses ou des modèles. Le spectre d'absorption dérivé est donc une approximation.
Spectre d'absorption de la chlorophylle
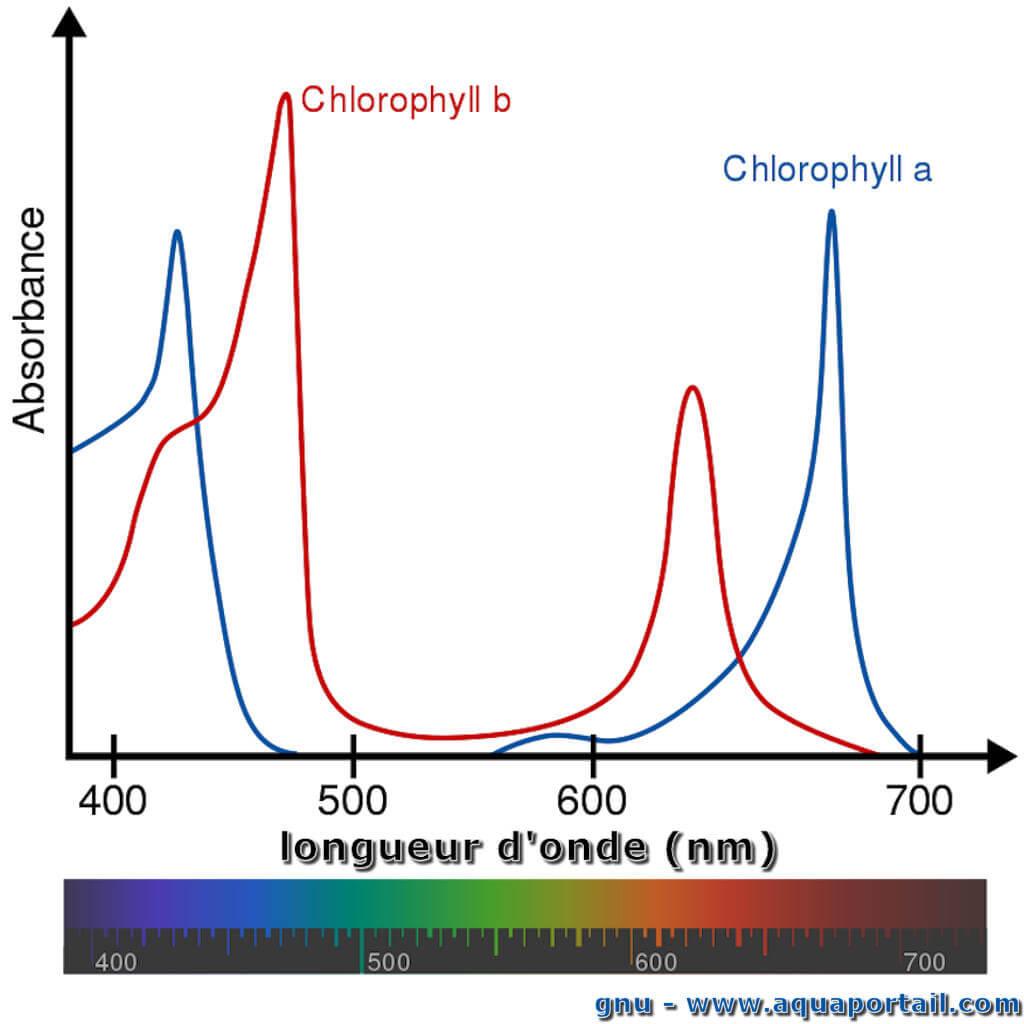
Les spectres d'absorption des chlorophylles en solution dans les solvants ont toujours deux maxima d'absorption distincts, l'un compris entre 600 et 800 nm, appelé bande Qy, et l'autre d'environ 400 nm, appelée bande de Soret. La figure à droite montre ces maxima d'absorption pour la chlorophylle a et b. De plus, la bande Qx existe autour de 580 nm, elle est polarisée perpendiculairement à Qy et s'absorbe généralement très faiblement.
L'absorption dépend du solvant et, par conséquent, la position des maxima d'absorption peut varier de quelques nanomètres selon le type de solvant. Dans l'environnement naturel des chlorophylles, l'environnement protéique, les choses se présentent différemment. L'emplacement des maxima d'absorption dépend de deux facteurs :
- En fonction de la charge partielle des acides aminés environnants et de la flexion des groupes latéraux des molécules de chlorophylle, les maxima d'absorption peuvent être à des longueurs d'onde très différentes.
- Dans les protéines, les chlorophylles sont très proches, de sorte qu'elles interagissent les unes avec les autres (interaction dipôle-dipôle, et à très courte distance, une interaction également). Cette interaction conduit à une baisse des niveaux d'énergie et donc à un redshift des maxima d'absorption. Cela est particulièrement frappant à l'exemple du complexe d'antenne LH2 de bactéries pourpres. Le complexe LH2 est constitué de deux groupes annulaires de molécules de bactériochlorophylle (voir photo à gauche). Le cycle supérieur (B850) contient 18 molécules BChl, qui sont très proches les unes des autres, c'est-à-dire fortement couplées. L'anneau inférieur (B800) est constitué de 9 molécules BChl, beaucoup plus éloignées et donc beaucoup moins couplées.
Le couplage fort fait passer l'absorption de BChla dans l'anneau B850 au rouge. La bande d'absorption est à 850 nm, d'autre part, le BChl a faiblement couplé du cycle B800 absorbe à 800 nm, c'est-à-dire dans la même gamme que les molécules de BChl a solubles dans les solvants. Dans le spectre d'absorption (à droite) du complexe LH2, les bandes d'absorption des molécules B800 et B850-BChl- a sont clairement séparées. De plus, les bandes dérivées des molécules de caroténoïde sont montrées, elles ne sont pas montrées dans la structure.
Il existe plusieurs types de chlorophylle qui diffèrent dans les groupes latéraux de la porphyrine. Ils ont des spectres d'absorption différents et existent chez différents organismes phototrophes.
Spectre d'absorption de l'hydrogène
Le spectre d'absorption de l'hydrogène, dans la partie visible du spectre, a lieu avec des longueurs d'onde de 410 nm (violet), 434 nm (bleu), 486 nm (bleu-vert) et 656 nm (rouge). Chacune des raies d'absorption correspond à un saut électronique spécifique.
Effectivement, lorsque l'atome d'hydrogène absorbe la lumière, l'électron passe à un niveau d'énergie supérieur (un "état excité"). Il peut sauter d'un niveau ou de quelques niveaux en fonction de la quantité d'énergie qu'il absorbe. Mais l'électron ne peut se déplacer que d'un niveau d'énergie à un autre. Il ne peut pas aller à mi-chemin entre les niveaux. De plus, il faut une quantité d'énergie très discrète - ni plus, ni moins - pour déplacer l'électron d'un niveau particulier à un autre.
L'énergie dont un électron a besoin pour sauter jusqu'à un certain niveau correspond à la longueur d'onde de la lumière qu'il absorbe. Autrement dit, les électrons n'absorbent que les photons qui leur donnent exactement la bonne énergie dont ils ont besoin pour sauter des niveaux. Il faut se rappeler que les photons ne transportent que des quantités d'énergie très spécifiques et que leur énergie correspond à leur longueur d'onde.
Ainsi, la lumière de longueur d'onde la plus courte/d'énergie la plus élevée (violet 410 nm) fait sauter l'électron de quatre niveaux, tandis que la lumière de longueur d'onde la plus longue/d'énergie la plus faible (rouge 656 nm) provoque un saut d'un seul niveau.
Synonymes, antonymes
Voir tous les synonymes pour "spectre d'absorption".1 synonyme (sens proche) de "spectre d'absorption" :
1 antonyme (sens contraire) :
Les mots ou les expressions apparentés à SPECTRE D'ABSORPTION sont des termes qui sont directement liés les uns aux autres par leur signification, générale ou spécifique.
L'expression SPECTRE D'ABSORPTION est dans la page 3 des mots en S du lexique du dictionnaire.
Mots en S à proximité
spéciale de claire spéciation spéciation allopatrique spéciation sympatrique spécimen type spectre d'absorptionspectre d'action spectre d'émission spectre lumineux spectre visible spectrine
En rapport avec "spectre d'absorption"

Un antibiotique à large spectre précise la nature de l'efficacité d'un antibiotique pour lutter contre une vaste gamme de bactéries pathogènes à Gram positif...
Le spectre d'action correspond à l'intensité de la photosynthèse effectuée par un organisme photosynthétique, en fonction de la longueur d'onde de la lumière...

Un spectre d'émission est le spectre électromagnétique émis par des atomes, des molécules ou des matériaux sans émission de rayonnement électromagnétique...
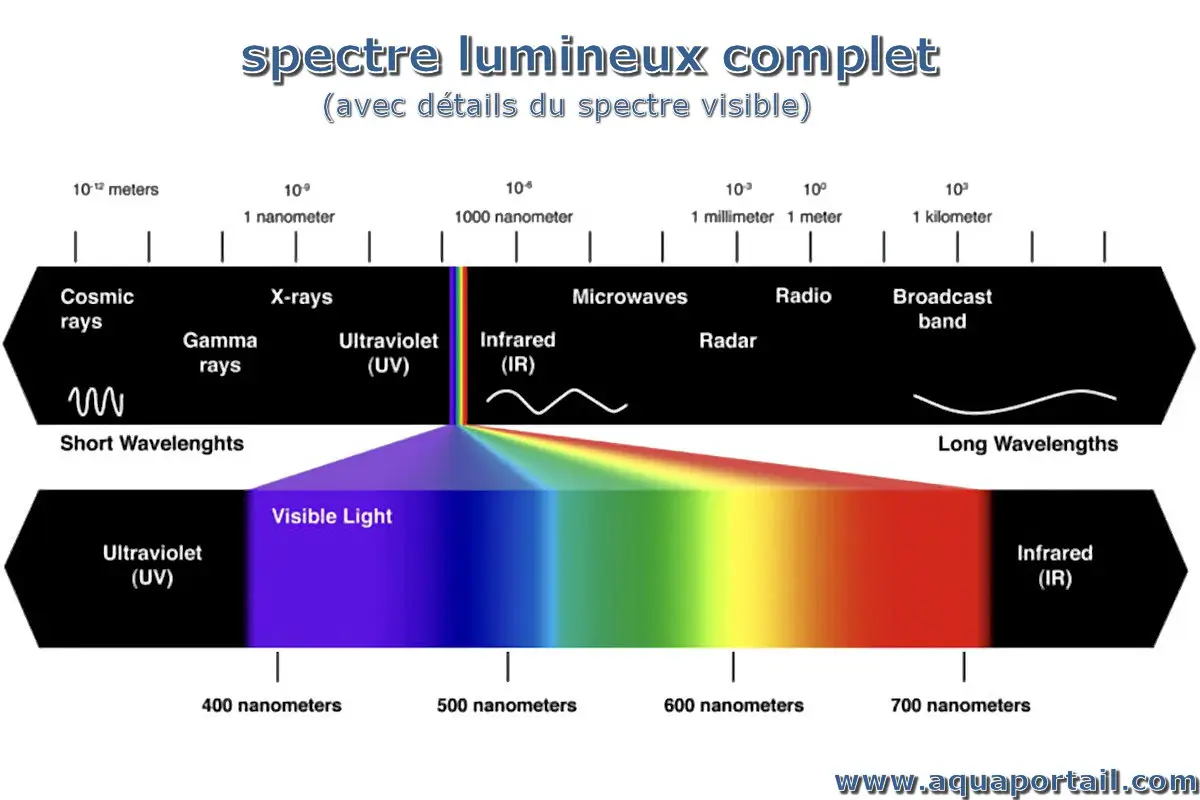
Le spectre lumineux regroupe le rayonnement infrarouge, le rayonnement visible de la lumière et le rayonnement ultraviolet, chacun intégré dans un spectre.
